
【题目】下列离子反应方程式正确的
A. 硫酸铵溶液中加入浓氢氧化钠溶液并加热:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
B. 碳与浓硝酸反应:C+4H++NO3-=CO2↑+2NO↑+2H2O
C. 氨水与FeCl3反应:3OH-+Fe3+=Fe(OH)3↓
D. 向NH4Al(SO4)2溶液中滴入Ba(OH)2使SO42-恰好完全反应:2Ba2++4OH-+Al3++2SO42-=BaSO4↓+AlO2-+2H2O
【答案】A
【解析】
A.硫酸铵溶液中加入浓氢氧化钠溶液并加热,反应生成氨气,反应的离子方程式为NH4++OH-![]() NH3↑+H2O,故A正确;
NH3↑+H2O,故A正确;
B.碳与浓硝酸反应,离子方程式:C+4H++4NO3-![]() CO2↑+4NO2↑+2H2O,故B错误;
CO2↑+4NO2↑+2H2O,故B错误;
C.氨水与FeCl3反应,离子方程式:3NH3H2O+Fe3+=Fe(OH)3↓+3NH4+,故C错误;
D.向NH4Al(SO4)2溶液中滴入Ba(OH)2使SO42-恰好完全反应,铝离子生成氢氧化铝沉淀,铵根离子生成一水合氨,离子方程式:2Ba2++NH4++Al3++2SO42-+4OH-=Al(OH)3↓+2BaSO4↓+NH3H2O+H2O,故D错误。
答案选A。


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:
【题目】硼镁泥是一种工业废料,主要成分是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的流程如下:

(1)实验中需用1mol/L的硫酸480mL,若用18.4mol/L的浓硫酸来配置,量取浓硫酸时需使用的量筒规格为(_______)。
A 10mL B 20mL C 50mL D 100mL
(2)加入的NaClO可与Mn2+反应:Mn2++ClO-+H2O=MnO2↓+2H++Cl-还有一种离子也会被NaClO氧化,该反应的离子方程式为___________________________;滤渣中除含有氢氧化铁、氢氧化铝外还有_________。
(3)在“除钙”前需检验滤液中Fe3+是否被除尽,简述检验方法_____________________。
(4)已知硫酸镁、硫酸钙的溶解度如下表

“除钙”是将;硫酸镁和硫酸钙混合溶液中的硫酸钙除去根据上表数据,采取的操作是_______________、趁热过滤、_________、____________,便得到比较纯净的硫酸镁。
(5)实验中提供的硼镁泥共100g,得到的MgSO4·7H2O为172.2g,则MgSO4·7H2O的产率为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学小组的同学开展测定Na2CO3和NaCl的固体混合物中Na2CO3质量分数的实验,他们提出下列实验方案。
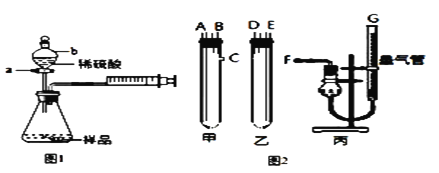
(1)甲同学用图1装置,把m g的混合物样品与足量稀硫酸反应后,测定产生的CO2气体的体积,检查该装置的气密性时,某同学将注射器活塞拉出一定距离,___,说明该装置的气密性好;当锥形瓶内不再产生气泡时立即读数,测定结果 ___(填 “偏大”、“偏小”、“无影响”)。
(2)乙同学用图2装置,Na2CO3、NaCl的固体混合物样品和稀硫酸应分别置于甲和乙中,导管连接方式如下:A连接____,B连接____,C连接_____(填写各接口的字母编号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2(g)、C2H4(g)和C2H5OH(1)的燃烧热分别是-285.8kJ·mol-1、-1411.0kJ·mol-1和-1366.8kJ·mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为( )
A. -44.2kJ·mol-1 B. +44.2kJ·mlo-1
C. -330kJ·mol-1 D. +330kJ·mlo-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把2mol X气体和1mol Y气体混合于2L密闭容器中,发生如下反应:3X(g)+Y(g)=nZ(g)+2W(g),2min内生成0.4mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.2mol·L-1·min-1,试计算:
(1)前2min内,用X表示的平均反应速率______;
(2)化学方程式中Z的化学计量数n______;
(3)2min内Y的转化率______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:(1)Zn(s)+1/2O2(g)=ZnO(s) △H=-348.3kJ·mol-1 ,
(2)2Ag(s)+1/2O2(g)=Ag2O(s) △H=-31.0kJ·mol-1,
则Zn(s)+Ag2O(s)=ZnO(s)+2Ag(s)的△H等于
A. -317.3kJ·mol-1 B. -379.3kJ·mol-1 C. -332.8kJ·mol-1 D. +317.3kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当前,汽车尾气已成为许多城市空气的主要污染源。研究表明,含TiO2的混凝土或沥青可以部分消除汽车尾气中的氮氧化物,其原理如下

下列关于该“消除”过程的叙述不正确的是
A. 部分光能转变为化学能
B. 消除总变化为NO2+O2+H2O→HNO3
C. 消除反应能全天候发生
D. 使用纳米TiO2的消除效率更高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是汽车尾气催化转化装置工作原理示意图:
![]()
![]()
![]()
![]()
![]()
下列说法不正确的是
A. 汽车尾气是雾霾成因之一,主要由CO、NO
B. 该过程中NO2既是生成物又是反应物
C. 整个过程中氧元素被还原,氮元素被氧化
D. 过程②中会有反应:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com