
【题目】我国科技工作者提出的一种OER(氧气析出反应) 机理如图所示下列说法错误的是
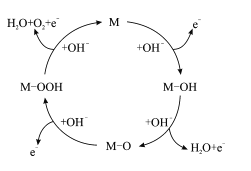
A.物质M不能改变OER反应的趋势
B.每一步反应过程都是氧化还原反应
C.反应过程中只涉及极性键的断裂和形成
D.该总反应方程式为4OH--4e-![]() 2H2O+O2↑
2H2O+O2↑
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】为了更好地表示溶液的酸碱度,科学家提出了酸度(AG)的概念.定义:AG=lgc(H+)/c(OH-),则下列叙述中正确的是( )
A.中性溶液AG=0
B.酸性溶液AG>0
C.常温下0.1mol/L的氢氧化钠溶液的AG=12
D.常温下0.1mol/L的醋酸溶液的AG=12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
(1)参加反应的HNO3和作为氧化剂的HNO3的个数比为________。
(2)若有64 g Cu被氧化,则被还原的HNO3的质量是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列反应的化学方程式,并分别用双线桥法和单线桥法表示电子转移的方向和数目。
(1)用氢气还原氧化铜。__、__。
(2)加热氯酸钾分解制取氧气。__、__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用KMnO4氧化盐酸溶液,反应方程式如2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O,若产生的Cl2在标准状况下体积为56 L,计算:
(1)参加反应的HCl的物质的量________________
(2)反应中被氧化的HCl的物质的量__________________
(3)并用双线桥标出电子转移的方向和数目___________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施或事实不能用勒夏特列原理解释的是( )
A.滴加酚酞的氨水中加入氯化铵固体后红色变浅
B.棕红色的NO2加压后颜色先变深后变浅(已知:2NO2(g)![]() N2O4(g))
N2O4(g))
C.煅烧粉碎的硫铁矿利于SO2的生成
D.工业上生产硫酸的过程中,使用过量的空气以提高SO2的利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,用一定浓度NaOH溶液滴定醋酸溶液,滴定终点附近溶液pH和导电能力的变化分别如下图所示(利用溶液导电能力的变化可判断滴定终点;溶液总体积变化忽略不计)下列说法正确的是
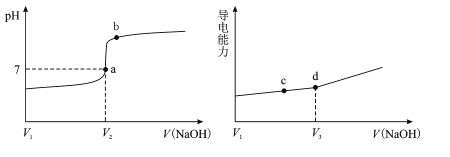
A.a→b过程中,水的电离程度不断增大
B.d点对应的溶液中:c(CH3COO-)+c(CH3COOH)=c(Na+)
C.c→d过程中,溶液导电性增强的主要原因是c(OH-)和c(Na+)增大
D.根据溶液pH和导电能力的变化可判断:V2>V3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A2+3B2 =2AB3在2L的密闭容器中进行,5s后,A2的物质的量增加了0.3mol,则此反应的平均速率可表示为:
A.v (A2)=0.01 mol/(L·s)B.v (B2)=0.08 mol/(L·s)
C.v (AB3)=0.03 mol/(L·s )D.v (AB3)=0.06 mol/(L·s )
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能够确定一溶液中一定含有![]() 的实验事实是( )
的实验事实是( )
A.取少量试样溶液,加入用盐酸酸化过的BaCl2溶液有白色沉淀生成
B.取少量试样溶液,加入用盐酸酸化过的Ba(NO3)2溶液,有白色沉淀生成
C.取少量试样溶液,加入足量盐酸无沉淀,加入BaCl2溶液,有白色沉淀生成
D.取少量试样溶液,加入BaCl2溶液有白色沉淀生成,再加稀盐酸,沉淀不溶解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com