
【题目】某小组为研究金属的腐蚀与防护,设计如图所示装置。下列叙述正确的是
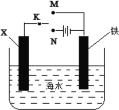
A.若X为碳棒,为减缓铁的腐蚀,开关K应置于M处
B.若X为碳棒,开关K置于N处,会加快铁的腐蚀
C.若X为锌,开关K置于M处,是牺牲阳极的阴极保护法
D.若X为锌,开关K置于N处,铁电极发生的反应为:Fe-2e-=Fe3+
 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
A. 图 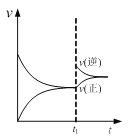 可表示N2+3H2
可表示N2+3H2![]() 2NH3的速率时间图像,t1时刻改变的条件是升高温度
2NH3的速率时间图像,t1时刻改变的条件是升高温度
B. 图 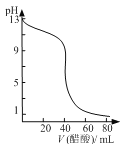 可表示用0.1000 mol·L-1醋酸滴定40.00mL 0.1000mol·L-1NaOH溶液得到的滴定曲线
可表示用0.1000 mol·L-1醋酸滴定40.00mL 0.1000mol·L-1NaOH溶液得到的滴定曲线
C. 图 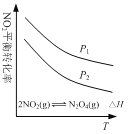 可表示NO2平衡转化率与温度、压强的变化关系,由图可知:△H<0、P1<P2
可表示NO2平衡转化率与温度、压强的变化关系,由图可知:△H<0、P1<P2
D. 图 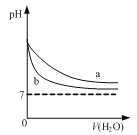 可表示pH相同的NaOH溶液与氨水稀释过程的pH变化,其中曲线a对应氨水
可表示pH相同的NaOH溶液与氨水稀释过程的pH变化,其中曲线a对应氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在实验室研究锌与酸的反应,实验数据如下:
实验序号 | 锌质量 | 锌状态 | c(H2SO4) | V(H2SO4) | 金属消失时间 |
1 | 0.10 g | 颗粒 | 0.5mol·L-1 | 50mL | 500s |
2 | 0.10 g | 粉末 | 0.5mol·L-1 | 50mL | 50s |
3 | a g | 颗粒 | 1.0mol·L-1 | 50mL | 125s |
分析上述数据,回答下列问题
(1)实验1和2表明,_____对反应速率有影响。
(2)实验1和3研究的是反应物浓度对反应速率的影响,则a =________ g。
(3)该同学研究发现:相同的锌粒分别与H2SO4、盐酸反应(操作如下图),现象差异明显(稀盐酸中锌表面产生气泡的速率要比稀硫酸快)。

该同学对产生这一现象的原因,提出两种假设:
a. 氯离子对反应起促进作用,加快了反应的进行;
b. ________,减缓了反应的进行。
为进一步证实自己的猜想,该同学在室温下,分别取5mL 0.2 mol·L-1盐酸溶液,一份加入一定量的固体___________ (填“所加试剂化学式”),另一份作对比实验,再分别同时加入完全相同的锌粒,比较反应速率的大小。
(4)锌粒和稀硫酸反应制取氢气时,往往加入少量CuSO4粉末,可加快产生H2的速率,其原因是___ (结合化学方程式作出合理解释)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实能说明亚硝酸是弱电解质的是
①亚硝酸溶液中存在HNO2分子,呈酸性
②用HNO2溶液做导电性实验,灯泡很暗
③HNO2溶液不与Na2SO4溶液反应
④0.1 mol·L-1 HNO2溶液中,c(H+)=0.015 mol·L-1
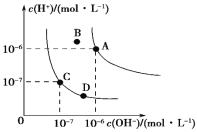
⑤向水中加入亚硝酸钠固体,如图水的电离平衡曲线可以从C点到D点
A.①②③B.②③④C.①②④⑤D.①④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应N2O4(g) ![]() 2NO2(g) ΔH=+57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法不正确的是
2NO2(g) ΔH=+57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法不正确的是
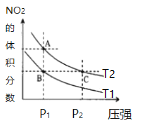
A.A点的反应速率小于C点的反应速率
B.A、C两点气体的颜色:A浅,C深
C.由状态B到状态A,可以用降温的方法
D.A、C两点气体的平均相对分子质量:A<C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用氟硼酸(HBF4,属于强酸)代替硫酸做铅蓄电池的电解质溶液,可使铅蓄电池在低温下工作时的性能更优良,反应方程式为:Pb+PbO2+4HBF4 ![]() 2Pb(BF4)2+2H2O;Pb(BF4)2为可溶于水的强电解质,下列说法正确的是
2Pb(BF4)2+2H2O;Pb(BF4)2为可溶于水的强电解质,下列说法正确的是
A. 放电时,正极区pH增大
B. 充电时,Pb电极与电源的正极相连
C. 放电时的负极反应为:PbO2+4H++2e-=Pb2++2H2O
D. 充电时,当阳极质量增加23.9g时,溶液中有0.2mole-通过
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲测定某NaOH溶液的物质的量浓度,可用0.1000 mol·L-1 HCl标准溶液进行中和滴定(用酚酞作指示剂)。请回答下列问题:
(1)碱式滴定管用蒸馏水洗净后,接下来应该进行的操作是 ______。
(2)若甲学生在实验过程中,记录滴定前滴定管内液面读数为1.10 mL,滴定后液面如图,则此时消耗标准溶液的体积为______________ 。
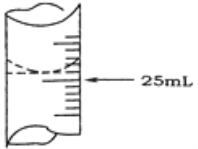
乙学生做了三组平行实验,数据记录如下:
实验序号 | 待测NaOH溶液的体积/mL | 0.1000mol·L-1HCl溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 25.00 | 0.00 | 26.11 |
2 | 25.00 | 1.56 | 33.30 |
3 | 25.00 | 0.22 | 26.31 |
(3)选取上述合理数据,计算出待测NaOH溶液的物质的量浓度为_____________ (小数点后保留四位)。
(4)下列哪些操作会使测定结果偏高(_________) (填序号)。
A.锥形瓶用蒸馏水洗净后,直接注入待测溶液进行滴定
B.滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液
C.碱式滴定管用蒸馏水洗涤后立即取用25.00mL待测液注入锥形瓶中进行滴定
D.滴定前俯视滴定管读数,滴定后平视滴定管读数
(5)滴定达到终点的标志是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】咖啡酸具有较广泛的抑菌作用,其结构简式如图。下列关于咖啡酸的说法不正确的是
![]()
A.分子中含有2种含氧官能团
B.能与FeCl3溶液发生显色反应
C.1mol咖啡酸最多能与3molBr2反应
D.1 mol咖啡酸最多能与3molNaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物 Z 的结构简式为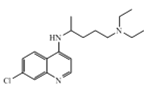 ,常进一步修饰后制成注射液使用,也可制成口服剂。如图为化合物 Z 的一种合成路线,先分别合成化合物F和Y,最后再用F 和 Y 反应获得化合物Z。
,常进一步修饰后制成注射液使用,也可制成口服剂。如图为化合物 Z 的一种合成路线,先分别合成化合物F和Y,最后再用F 和 Y 反应获得化合物Z。
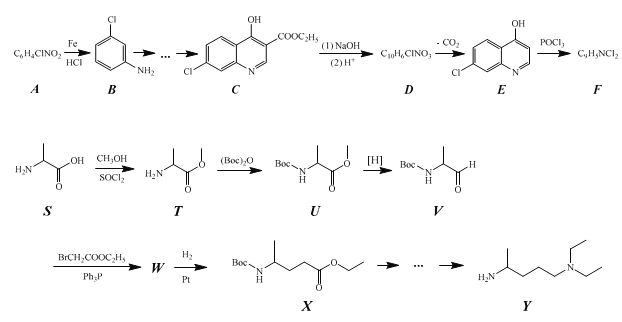
已知:
①![]()
![]()
![]()
②(Boc)2O=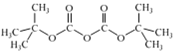 (其中Boc=
(其中Boc=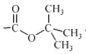 ,作答时建议用缩写符号来表示)
,作答时建议用缩写符号来表示)
③Ph3P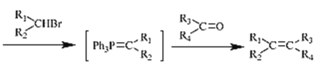 (其中-Ph为苯基,不考虑顺反异构)
(其中-Ph为苯基,不考虑顺反异构)
(1)化合物A 中含氧官能团的名称为__。
(2)生成化合物B的反应类型为__,由化合物F 和 Y 合成化合物Z 的反应类型为__。
(3)化合物C与足量NaOH水溶液反应,即化合物C到化合物D的转化步骤(1)的化学方程式为__。
(4)由化合物T到化合物U的反应还生成了CO2和一种醇,请写出这个醇的结构简式__。将化合物T与(Boc)2O反应制成化合物U再进行后续反应的目的是__。
(5)化合物W 的结构简式为__。
(6)作为药物时,化合物 Z 往往要进一步与磷酸反应制成磷酸盐使用。这么做的原因是:__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com