
����Ŀ��ijͬѧ��ʵ�����о�п����ķ�Ӧ��ʵ����������:
ʵ����� | п���� | п״̬ | c(H2SO4) | V(H2SO4) | ������ʧʱ�� |
1 | 0.10 g | ���� | 0.5mol��L-1 | 50mL | 500s |
2 | 0.10 g | ��ĩ | 0.5mol��L-1 | 50mL | 50s |
3 | a g | ���� | 1.0mol��L-1 | 50mL | 125s |
�����������ݣ��ش���������
(1)ʵ��1��2������_____�Է�Ӧ������Ӱ�졣
(2)ʵ��1��3�о����Ƿ�Ӧ��Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죬��a =________ g��
(3)��ͬѧ�о����֣���ͬ��п���ֱ���H2SO4�����ᷴӦ(��������ͼ)�������������(ϡ������п����������ݵ�����Ҫ��ϡ�����)��

��ͬѧ�Բ�����һ�����ԭ��������ּ��裺
a. �����ӶԷ�Ӧ��ٽ����ã��ӿ��˷�Ӧ�Ľ��У�
b. ________�������˷�Ӧ�Ľ��С�
Ϊ��һ��֤ʵ�Լ��IJ��룬��ͬѧ�������£��ֱ�ȡ5mL 0.2 mol��L-1������Һ��һ�ݼ���һ�����Ĺ���___________ (���������Լ���ѧʽ��)����һ�����Ա�ʵ�飬�ٷֱ�ͬʱ������ȫ��ͬ��п�����ȽϷ�Ӧ���ʵĴ�С��
(4)п����ϡ���ᷴӦ��ȡ����ʱ��������������CuSO4��ĩ���ɼӿ����H2�����ʣ���ԭ����___ (��ϻ�ѧ����ʽ������������)��
���𰸡������������Ӵ������ 0.1 ��������ӶԷ�Ӧ���������� Na2SO4(��K2SO4��(NH4)2SO4) Zn+ CuSO4= Cu+ ZnSO4 ��ͭ��п��ϡ���ṹ��ԭ��أ��ӿ췴Ӧ����
��������
(1)���ݿ��Ʊ�������ʵ��1��2ֻ��п״̬��ͬ��˵�����������Է�Ӧ������Ӱ�죻
(2)ʵ��1��3�о����Ƿ�Ӧ��Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죬���ݿ��Ʊ�������ֻ���������Ũ�Ȳ�ͬ��п������п״̬Ӧ��ͬ������a =0.1g��
(3)����ʵ�飬п��״̬��������ͬ��������Ũ����ͬ��ֻ�������ͬ�����Է�Ӧ���ʲ�ͬ��ԭ������ǣ�a. �����ӶԷ�Ӧ��ٽ����ã��ӿ��˷�Ӧ�Ľ��У� b. ��������ӶԷ�Ӧ���������ã������˷�Ӧ�Ľ��С�
ȡ����5mL 0.2 mol��L-1������Һ��һ�ݼ���һ�����Ĺ��������ƣ���һ�����Ա�ʵ�飬�ٷֱ�ͬʱ������ȫ��ͬ��п�����ȽϷ�Ӧ���ʵĴ�С�������������Ƶ������п��Ӧ����������˵����������ӶԷ�Ӧ���������á�
(4)п����ϡ���ᷴӦ��ȡ����ʱ����������CuSO4��ĩ��������Ӧ��Zn+ CuSO4= Cu+ ZnSO4 �����ɵ�ͭ��п��ϡ���ṹ��ԭ��أ���Ӧ���ʼӿ졣


 ǧ�������������ĩ�����Ծ�����ϵ�д�
ǧ�������������ĩ�����Ծ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ���ͭ�ǻ�����ӡȾ����ҵ����Ҫԭ�ϣ��㷺�����л��ϳɵĴ�����
��.�ײ���CuCl2��2H2O�ȷֽⷨ�Ʊ�CuCl��װ����ͼ��

��1������X��������_______________��C���ձ����Լ�������__________��
��2�������������ͨ���������_______��
��3����Ӧ������ȡ���ò�Ʒ�������������к�������ͭ�������ԭ����______________��
��.����ȡ����CuCl2���������·����Ʊ�CuCl��

��4���������з�Ӧ�����ӷ���ʽΪ___________________��
��5��������������100 mL 10 mol/L�������0.2 mol/L���ᣬ��ͨ��SO2���ް�ɫ�����������Դ��������������ֲ��룺
����һ��c(H��)�����°�ɫ�����ܽ⡣Ϊ��֤�˲��룬ȡ75gCuCl2���塢100 mL0.2 mol/L���ἰ________mL10.0mol/LH2SO4���Ƴ�200 mL��Һ���ٽ��в����ڣ��۲��Ƿ��а�ɫ����������
�������_______________�������ʵ��˵���ò����Ƿ������_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£������Ϊ5 L���ܱ������У�A��B��C������������ʵ���n��mo1����ʱ��t��min���ı仯��ͼ��ʾ��
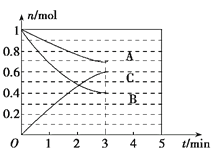
��1���÷�Ӧ�Ļ�ѧ����ʽΪ________���ڴ������£����и�����˵���÷�Ӧ�ﵽƽ��״̬����__��
A.��������ѹǿ���� B.���������ܶȲ���
C.�������������ʵ������� D.��������ƽ����Է�����������
E.C�������������
��2���÷�Ӧ�ķ�Ӧ��������ʱ��t�Ĺ�ϵ��ͼ��ʾ��
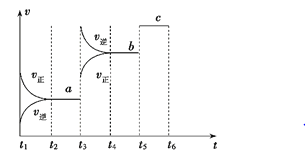
�ٸ���ͼ�жϣ���t3ʱ����θı����������_____��
��a��b��c������C���������������________��
�۸��ε�ƽ�ⳣ�����±���ʾ����K1��K2��K3֮��Ĺ�ϵΪ_______���á�![]() ������
������![]() ����=�����ӣ���
����=�����ӣ���
t2��t3 | t4��t5 | t5��t6 |
K1 | K2 | K3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������չ�ҵ�����ķ���CO2���Լ�����Ⱦ�����Ϊ����
(1)��CO2��������ȼ�ϼ״���
��д���״��Ĺ���������____________��
��֪��CO2(g)+3H2(g) CH3OH(g)+H2O(l) ��H=-49.0kJmol-1��һ�������£�������̶�Ϊ1 L���ܱ������г���1mol CO2��3mol H2 �����CO2��CH3OH(g)��Ũ����ʱ��仯��������ͼ��ʾ��
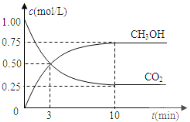
�ڷ�Ӧ��ʼ����3����ʱ����Ӧ����v(H2)��________mol/(L��min)��
�۸������£��÷�Ӧ��ƽ�ⳣ������ʽΪ________��CO2��ƽ��ת������________��
(2)��CO2�ϳɶ�����(CH3OCH3)��
��CO2 ������ϳɶ����ѵĹ�������Ҫ�������з�Ӧ��
��ӦI��CO2(g) + H2(g)CO(g) + H2O(g) H= +41.2 kJmol-1
��ӦII: 2CO2(g) + 6H2(g)CH3OCH3(g) + 3H2O(g) H = - 122.5 kJmol-1
���У���ӦII ������a��b������ɣ���д����Ӧa���Ȼ�ѧ����ʽ��
a��_________
b��2CH3OH(g)CH3OCH3(g) + H2O(g) H = -23.5 kJmol-1
��L(L1��L2)��X�ֱ����ѹǿ���¶ȣ���ͼ��ʾLһ��ʱ����ӦII�ж����ѵ�ƽ�������X�仯�Ĺ�ϵ������X��������������______���ж�L1��L2�Ĵ�С�����������ɣ�________��
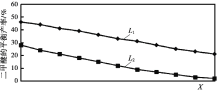
(3) ��ѹʱ����CO2��H2��ʼ��һ���������£�CO2ƽ��ת���ʺ�ƽ��ʱCH3OCH3��ѡ����(CH3OCH3��ѡ����=![]() )���¶ȱ仯����ͼ��
)���¶ȱ仯����ͼ��
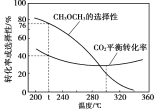
��t��ʱ����ʼͶ��a molCO2��b mol H2���ﵽƽ��ʱ��ӦII���ĵ�H2�����ʵ���Ϊ______mol��
���¶ȸ���300�棬CO2ƽ��ת�������¶����߶������ԭ����_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о�С������ͼװ�ý���SO2��FeCl3��Һ��Ӧ�����ʵ��(�г�װ������ȥ)��
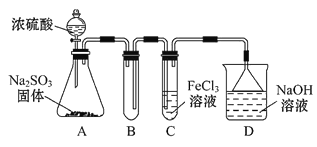
(1)ͨ������SO2ʱC�й۲쵽������Ϊ_____________________________��
(2)������������С��ͬѧ��ΪSO2��FeCl3��Һ����������ԭ��Ӧ����С��ͬѧ��C�Թܷ�Ӧ�����Һ�м��������ữ��BaCl2��Һ�������ְ�ɫ����������֤����Ӧ������SO42��������_______(���������������)��������____________��
(3)Ϊ����֤SO2���л�ԭ�ԣ�ʵ���п��Դ���FeCl3���Լ���________(����ĸ)��
A.Ũ���ᡡ������B.����KMnO4��Һ��������C.��ˮ��������D.NaCl��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ��ȡŨ�Ⱦ�Ϊ0.1mol��L-1�Ĵ�����Һ�Ͱ�ˮ��Һ��20 mL���ֱ���0.1mol��L-1NaOH��Һ��0.1 mol��L-1��������к͵ζ����ζ�������pH��μ���Һ������仯��ϵ��ͼ��ʾ��

����˵����ȷ����
A.����I�еμ���Һ��10 mLʱ��c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
B.����I�еμ���Һ��25 mLʱ��c(NH4+)>c(C1-)>c(H+)>c(OH-)
C.����II�еμ���Һ��10 mL��25 mL֮����ڣ�c(NH4+)=c(Cl-)>c(OH-)=c(H+)
D.����II�еμ���Һ��10mLʱ��c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)]
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��MOH��ROH����һԪ�����Һ�ֱ��ˮϡ��ʱ��pH�仯����ͼ��ʾ��������������ȷ����
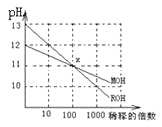
A.MOH��ROH����ǿ��
B.��x�㣬c(M+)=c(R+)
C.ϡ��ǰ��c(ROH)=10c(MOH)
D.�����£�pH֮��Ϊ14�Ĵ����ROH��Һ�������ϣ�������Һ�ʼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС��Ϊ�о������ĸ�ʴ������������ͼ��ʾװ�á�����������ȷ����
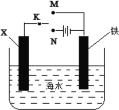
A.��XΪ̼����Ϊ�������ĸ�ʴ������KӦ����M��
B.��XΪ̼��������K����N������ӿ����ĸ�ʴ
C.��XΪп������K����M��������������������������
D.��XΪп������K����N�������缫�����ķ�ӦΪ��Fe-2e-=Fe3+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(NiSO4)��һ����Ҫ�Ļ���ԭ�ϣ��㷺Ӧ���ڵ�ơ�ҽҩ��ӡȾ�ȹ�ҵ���Ժ����ϴ���(��Ҫ��Ni��������Al��Al2O3��Fe�������������ᡢ�������)Ϊԭ������NiSO4��7H2O��������ֹ����������£�
����һ��
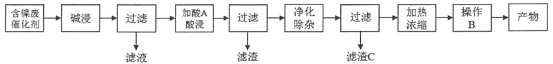
���̶���

��֪�����ֽ������������Ksp����ֵ���±���ʾ��
��ѧʽ | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Ni(OH)2 |
Ksp����ֵ | 10��17 | 10��39 | 10��34 | 10��15 |
�ش��������⣺
(1)����һ��������A�����̶���������X___________(������ͬ����������ͬ��)������һ������C�����̶�������II___________(������ͬ����������ͬ��)�����̶�������I��___________��
(2)����һ���������ʱ������Ӧ�����ӷ���ʽΪ_________________��___________________��
(3)���̶��������������������������������̣���һ��������������H2O2��������Ӧ�����ӷ���ʽ��____________________________________________���ڶ�����������Һ��pH��
(4)�����Ƚ�����һ�в���B�����̶��в���Y�ش����Y��___________��___________�����ˡ�ϴ�ӡ�������ò��
(5)�ɼ�֪��Ϣ��ʽ���㣺�����£�Ni2����ȫ����ʱ��pHֵ___________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com