
【题目】浓硫酸具有:①难挥发性(高沸点);②酸性;③强氧化性;④吸水性;⑤脱水性。下列各项分别表现浓硫酸的什么性质,请将序号填于空白处:
(1)浓硫酸与食盐共热,浓硫酸表现的性质为__。
(2)浓硫酸与铜共热,化学方程式为__,浓硫酸表现的性质是__。
(3)浓硫酸与红热木炭反应,化学方程式为__,浓硫酸表现的性质是__。
(4)可用浓硫酸干燥H2、CO2、HCl等气体,浓硫酸表现的性质为__。
(5)蔗糖中倒入浓硫酸,蔗糖变黑,体积膨胀,且有刺激性气味的气体产生,浓硫酸表现的性质是__。
【答案】①② Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O ②③ C+2H2SO4(浓)
CuSO4+SO2↑+2H2O ②③ C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O ③ ④ ③⑤
CO2↑+2SO2↑+2H2O ③ ④ ③⑤
【解析】
(1)浓硫酸与食盐共热,生成氯化氢气体,浓硫酸表现了酸性和难挥发性,答案为①②;
(2)浓硫酸与铜共热生成硫酸铜、二氧化硫和水,方程式为Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O,体现了浓硫酸的强氧化性和酸性,答案选②③;
CuSO4+SO2↑+2H2O,体现了浓硫酸的强氧化性和酸性,答案选②③;
(3)浓硫酸与红热的木炭反应生成二氧化碳、二氧化硫和水,方程式为C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O;体现了浓硫酸的强氧化性,答案选③;
CO2↑+2SO2↑+2H2O;体现了浓硫酸的强氧化性,答案选③;
(4)利用浓硫酸的吸水性,干燥气体,答案选④;
(5)蔗糖中倒入浓硫酸,浓硫酸按水中H、O比例脱去蔗糖中H、O元素,导致蔗糖碳化,产生大量的热;再与碳反应生成二氧化碳、二氧化硫和水,浓硫酸表现了脱水性和强氧化性,答案选③⑤。


科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是( )
A.向AlCl3溶液中滴加氨水,产生白色沉淀;再加入NaHSO4溶液,沉淀溶解
B.在Cu(NO3)2溶液中加入铜粉,铜粉不溶解;再加入稀硫酸溶液,铜粉溶解
C.用如图所示的装置可以测定黄铜(Cu,Zn合金)中Zn的含量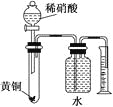
D.在FeCl3溶液中加入KSCN溶液,溶液变红,加入足量铁粉充分振荡,溶液红色褪去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.标准状况下,气体摩尔体积约为22.4 L/mol
B.非标准状况下,1 mol任何气体都不可能为22.4 L
C.标准状况下,22.4 L任何气体的物质的量都约为1 mol
D.标准状况下,1 mol H2O的体积小于22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无机化合物的提纯中,常利用难溶电解质的溶解平衡原理除去某些杂质离子。现有含氯化亚铁杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按如图步骤进行提纯:
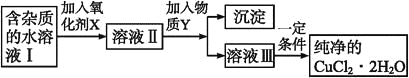
已知某温度下:Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH,见下表:
Fe3+ | Fe2+ | Cu2+ | |
氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
氢氧化物完全沉淀时的pH | 3.2 | 9.0 | 6.7 |
请回答下列问题:
(1)加入氧化剂X的目的是_______________________。
(2)最适合作氧化剂X的是___________(填编号,否则不给分);写出氧化剂X参与的离子反应方程式_________。
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(3)为了除去Fe3+,需加入物质Y_________(填化学式)调节溶液的pH值为___________。
(4)最后能不能直接蒸发结晶得到CuCl2·2H2O晶体?________(填“能”或“不能”);若能,不用回答;若不能,回答该如何操作?____________________。
(5)常温下已知Fe(OH)3的Ksp=1.0×10-35,向500mL 0.2mol/L的FeCl3溶液中加入NaOH固体(溶液体积变化忽略不计)后pH=3.0,则需要加入氢氧化钠固体的质量为________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关热化学方程式书写与对应表述均正确的是( )
A. 稀硫酸与0.1 mol/L NaOH溶液反应:H+(aq)+OH-(aq)= H2O(l)△H = +57.3 kJ·mol-1
B. 在101KPa下氢气的燃烧热△H =-285.5 kJ·mol-1,则水分解的热化学方程式:2H2O(l)=2H2(g)+O2(g) △H = +285.5 kJ·mol-1
C. 已知2C(s)+O2(g)=2CO(g) △H=-221 kJ·mol-1, 则可知C的燃烧热大于110.5 kJ·mol-1
D. 2N2O5(g)![]() 4NO2(g)+O2(g) ΔH>0 反应为熵增反应,任何温度下能自发进行
4NO2(g)+O2(g) ΔH>0 反应为熵增反应,任何温度下能自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是重要的化工原料,目前主要通过石油炼化制备。随着化石燃料资源日益减少,科研工作者正在探索和研发制备乙烯的新方法。
Ⅰ.甲烷在一定条件下脱氢可生成乙烯:2CH4(g)![]() C2H4(g)+2H2(g)△H>0
C2H4(g)+2H2(g)△H>0
(1)活化能Ea正____Ea逆(填“>”、“=”或“<”,下同);k正、k逆表示速率常数,当升高温度时,k正增大的倍数____k逆增大的倍数。
Ⅱ.利用生物无水乙醇催化脱水制备乙烯
主反应 i:C2H5OH(g)![]() C2H4(g)+H2O(g)△H1=+45.5 kJ/mol
C2H4(g)+H2O(g)△H1=+45.5 kJ/mol
副反应 ii:2C2H5OH(g)![]() C2H5OC2H5(g)+H2O(g)△H2=﹣19.0 kJ/mol
C2H5OC2H5(g)+H2O(g)△H2=﹣19.0 kJ/mol
副反应 iii:C2H5OC2H5(g)![]() 2C2H4(g)+H2O(g)△H3
2C2H4(g)+H2O(g)△H3
(2)求△H3=____。
(3)在 2L 恒容密闭容器中充入2mol C2H5OH(g)和一定量的催化剂进行反应,平衡体系中含碳组分的物质的量分数随温度的变化如图所示:
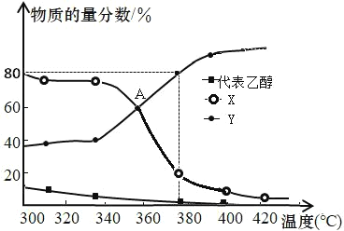
①图中 Y 代表____(填“C2H4”或“C2H5OC2H5”),请解释原因____。
②主反应 i 在 A 点达到平衡状态的标志为____。
a.乙烯浓度不再变化 b.容器内压强不随时间变化
c.混合气体的密度不随时间变化 d.△H 不再变化
③380℃时,假设乙醇完全反应,则反应 iii 的平衡常数 K=____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1个某种氯原子的质量是a g,1个12C原子的质量是b g,用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
①该氯原子的相对原子质量为12a/b ②m g该氯原子的物质的量为m/(aNA) mol ③该氯原子的摩尔质量是aNA g ④a g该氯原子所含的电子数为17 mol
A.①②B.①③C.②③D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、R为五种短周期元素,其原子半径和最外层电子数之间的关系如图所示,其中R元素是短周期中除稀有气体之外原子半径最大的元素。下列说法正确的是
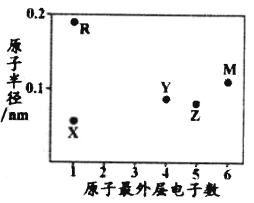
A. M元素在周期表中的位置是第2周期第ⅥA族
B. 元素的最高价氧化物对应水化物的酸性:Z<Y
C. X元素与Y、Z、M三种元素只能各形成一种共价化合物
D. Y、R的单质分别都能与其他物质反应置换出X单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高碘酸钾(KIO4)溶于热水,微溶于冷水和氢氧化钾溶液,可用作有机物的氧化剂。制备高碘酸钾的装置图如下(夹持和加热装置省略)。回答下列问题:
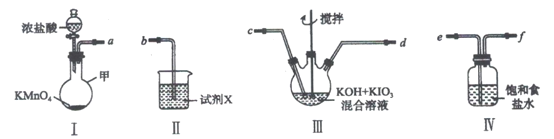
(1)装置I中盛放浓盐酸的仪器名称是___________。
(2)装置I中浓盐酸与KMnO4混合后发生反应的离子方程式是___________。
(3)装置Ⅱ中的试剂X的作用___________。
(4)上述炭置按气流由左至右各接口顺序为___________(用字母表示)。
(5)装置连接好后,将装置Ⅲ水浴加热,通入氯气一段时间,冷却析岀高碘酸钾晶体,经过滤,洗涤,干燥等步骤得到产品。
①写出装置Ⅲ中发生反应的化学方程式:___________。
②洗涤时,与选用热水相比,选用冷水洗涤晶体的优点是___________。
③上述制备的产品中含少量的KIO3,其他杂质忽略,现称取a g该产品配制成溶液,然后加入稍过量的用醋酸酸化的KI溶液,充分反应后,加入几滴淀粉溶液,然后用1.0mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液的平均体积为b L。
已知:KIO3+5KI+6CH3COOH===3I2+6CH3COOK+3H2O;KIO4+7KI+8CH3 COOH===4I2+8CH3COOK+4H2O;I2+2Na2S2O3===2NaI+N2S4O6则该产品中KIO4的百分含量是___________(Mr(KIO3)=214,Mr(KIO4)=230,列出计算式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com