
����Ŀ��H2O2�ֽ������ܶ�������Ӱ�졣ʵ���� 70 ��ʱ��ͬ������H2O2Ũ����ʱ��ı仯��ͼ��ʾ������˵����ȷ����

A. ͼ�ױ���������������ͬʱ��H2O2Ũ��ԽС����ֽ�����Խ��
B. ͼ�ұ���������������ͬʱ����ҺpHԽС��H2O2�ֽ�����Խ��
C. ͼ������������Mn 2+����ʱ����Һ����Խǿ��H2O2�ֽ�����Խ��
D. ͼ����ͼ��������������Һ����Mn2+��H2O2�ֽ����ʵ�Ӱ���

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����13�֣�
TiCl4�����Ѿ�����Ҫ�ɷ�ΪTiO2���Ʊ��ѣ�Ti������Ҫ�м����Ʊ���TiCl4������ʾ��ͼ���£�
![]()
���ϣ�TiCl4�����������Ȼ��������
������ | SiCl4 | TiCl4 | AlCl3 | FeCl3 | MgCl2 |
�е�/�� | 58 | 136 | 181�������� | 316 | 1412 |
�۵�/�� | 69 | 25 | 193 | 304 | 714 |
��TiCl4�е��ܽ��� | ���� | ���� | �� | ���� | |
��1���Ȼ����̣�TiO2��Cl2����ֱ�ӷ�Ӧ����̼����CO��CO2��ʹ��Ӧ���Խ��С�
��֪��TiO2(s)+2 Cl2(g)= TiCl4(g)+ O2(g) ��H1=+175.4 kJ��mol-1
2C(s)+O2(g)=2CO(g) ��H2=-220.9 kJ��mol-1
�� ����¯�м�̼�Ȼ�����TiCl4(g)��CO(g)���Ȼ�ѧ����ʽ��_______________________��
�� �Ȼ�������CO��CO2�����ת����������ͼ�жϣ�CO2����CO��Ӧ�Ħ�H_____0���������������=�������ж����ݣ�_______________��
�� �Ȼ���Ӧ��β���봦�����ŷţ�β���е�HCl��Cl2�����տɵô����ᡢFeCl3��Һ����β��������Һ������__________________________��
�� �Ȼ�������ȴ�����£������˵õ���TiCl4���Һ���������к���_____________��
��2�����ƹ��̣���TiCl4����������ô�TiCl4��ʾ��ͼ���£�
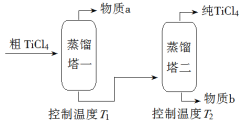
����a��______________��T2Ӧ������_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л����˵����ȷ����
A.�л���ֻ�����������ڲ��ܺϳ�
B.�л��ﶼ��������ˮ���������л��ܼ��Ĺ��ۻ�����
C.��ȫȼ��ֻ����CO2��H2O���л���һ������
D.�л����Ǻ���̼Ԫ�صĻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����100mL��c��H+��=0.3mol/L��������Һ������·��ͨ��0.04mol����ʱ�������������������������ǣ� ��
A. 0.10mol�ML Ag+ B. 0.20mol�ML Cu2+ C. 0.20mol�ML Zn2+ D. 0.20mol�M LPb2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ���ý������˳������͵���
A. ʹ������ˮ����ˮ
B. ����˿������ͭ˿����ɫ��Ӧ��ʵ��
C. ��ҵ�ϳ����Ȼ�ԭ��ұ�������õ�ⷨұ����
D. ��������ǿ����Һ��Ӧ��Ҳ����ǿ����Һ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.ʵ���������������ȼ���Ũ���ᣬ�ټӱ���������Ũ����B.��ȡ�屽������м����ˮ������ϼ���
C.֤���������к�����ԭ�ӣ��ɽ����������� AgNO3 ����Һ��D.ʵ�����ƵõĴ��屽ͨ���ʻ�ɫ������Ϊ�ܽ��������� Br2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ŀǰ���ҹ����л�����Ⱦ�еĴ�����Ⱦ����Ҫ�� �� ��
A��NH3��NO��CO2���� B��CO2��N2��Cl2������
C��SO2��NO2��CO���̳� D��HCl��SO2��N2��ɳ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��(HF)2(g) ![]() 2HF(g) ��H>0��ƽ����ϵ��������m(��)�������ʵ���n(��)֮���ڲ�ͬ�¶�����ѹǿ�ı仯������ͼ��ʾ������˵����ȷ����( )
2HF(g) ��H>0��ƽ����ϵ��������m(��)�������ʵ���n(��)֮���ڲ�ͬ�¶�����ѹǿ�ı仯������ͼ��ʾ������˵����ȷ����( )

A. �¶ȣ�T1< T2
B. ƽ�ⳣ����K(a)=K(b)<K(c)
C. ��Ӧ���ʣ�v(b)>v(a)
D. ��![]() 30g��mol-1ʱ��n(HF)��n[(HF)2]=2:1
30g��mol-1ʱ��n(HF)��n[(HF)2]=2:1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A~D ��ԭ�������� 20 ���ڵ�Ԫ�أ������ʻ�ṹ��Ϣ���±���

����ݱ��е���Ϣ�ش��������⣺
��1��C ���ӵĽṹʾ��ͼ��_____________��B ԭ�ӵĵ���ʽ��______________��
��2��д���� B ���⻯��������������ͬ�� 3 �ָ����������������ֱ��ǣ� �����ӣ�_____��������____________������������_____________��
��3��A Ԫ���� D Ԫ����ɵĻ������зdz���Ҫ����;��д��ʵ�����Ʊ�������Ļ�ѧ����ʽ��______________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com