
【题目】已知反应A(g) + B(g)=== 2C(g)在某段时间内以A的浓度变化表示的化学反应速率为0.5mol L—1 min—1,则此段时间内以C的浓度变化表示的化学反应速率为( )
A. 0.5mol L—1 min—1B. 1 mol L—1 min—1
C. 2 mol L—1 min—1D. 3 mol L—1 min—1
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】5种物质已按沸点由低到高顺序排列),则正己烷最可能插入的位置是( )
① | ② | ③ | ④ | ⑤ |
甲烷 | 乙烯 | 戊烷 | 2-甲基戊烷 | 甲苯 |
A.③④之间B.②③之间C.④⑤之间D.⑤之后
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙基环己烷常用作气相色谱对比样品,也用于有机合成。
(1)乙基环己烷(C8H16)脱氢制苯乙炔(C8H6)的热化学方程式如下:
①C8H16(l)![]() C8H10(l)+3H2(g) ΔH1>0
C8H10(l)+3H2(g) ΔH1>0
②C8H10(l)![]() C8H6(l)+2H2(g) ΔH2=a kJ·mol-1
C8H6(l)+2H2(g) ΔH2=a kJ·mol-1
③C8H6(l)+5H2(g)![]() C8H16(l) ΔH3=b kJ·mol-1
C8H16(l) ΔH3=b kJ·mol-1
则反应①的ΔH1为__________(用含a、b的代数式表示),有利于提高上述反应①的平衡转化率的条件是____(填字母)。
A.高温高压 B.低温低压 C.高温低压 D.低温高压
(2)不同压强和温度下乙基环己烷的平衡转化率如下图所示。

①在相同压强下升高温度,未达到新平衡前,v正____(填“大于”“小于”或“等于”)v逆。
②研究表明,既升高温度又增大压强,C8H16(l)的转化率也升高,理由可能是____。
(3)t ℃,向恒容密闭反应器中充入1.00 mol C8H16(l)进行催化脱氢,测得液态C8H10(l)和C8H6(l)的产率x1和x2(以物质的量分数计)随时间变化关系如下图所示。

①在8 h时,反应体系内氢气的量为_____mol(忽略其他副反应),液态C8H16(l)的转化率是_________。
②x1显著低于x2的原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在体积一定的密闭容器中加入1 mol N2和3 mol H2发生反应:
N2+ 3H2![]() 2NH3(正反应是放热反应)。下列有关说法正确的是( )
2NH3(正反应是放热反应)。下列有关说法正确的是( )
A. 降低温度可以加快反应速率
B. 达到化学反应限度时,生成2mol NH3
C. 向容器中再加入N2可以加快反应速率
D. 1mol N2和3mol H2的总能量低于2mol NH3的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用电解熔融氧化铝的方法制取金属铝。
(1)请写出反应的化学方程式_____________________________________________。
(2)现欲冶炼270吨铝,至少需要多少吨氧化铝?__________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境中常见的重金属污染物有汞、铅、锰、铬、镉。处理工业废水中含有的![]() 和
和![]() 常用的方法是还原沉淀法,该法的工艺流程为
常用的方法是还原沉淀法,该法的工艺流程为![]()
![]()
![]()
![]() Cr3+
Cr3+![]() Cr(OH)3。
Cr(OH)3。
其中第①步存在平衡:2![]() (黄色)+2H+
(黄色)+2H+![]()
![]() (橙色)+H2O。
(橙色)+H2O。
(1)写出第①步反应的平衡常数表达式:_________________________________。
(2)关于第①步反应,下列说法正确的是________(填序号)。
A.通过测定溶液的pH可以判断反应是否已达到平衡状态
B.该反应为氧化还原反应
C.在强酸性环境下,溶液的颜色为橙色
(3)第②步反应中,还原0.1 mol![]() ,需要________mol FeSO4·7H2O。
,需要________mol FeSO4·7H2O。
(4)第③步反应除生成Cr(OH)3沉淀外,还可能生成的沉淀为________。
(5)在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)![]() Cr3+(aq)+3OH-(aq)。常温下,Cr(OH)3的溶度积常数Ksp=10-32,当溶液中Cr3+的浓度降至10-5mol·L-1,认为Cr3+已经完全沉淀。现将第③步反应后溶液的pH调至4,请通过计算说明Cr3+是否沉淀完全(请写出计算过程)。____________
Cr3+(aq)+3OH-(aq)。常温下,Cr(OH)3的溶度积常数Ksp=10-32,当溶液中Cr3+的浓度降至10-5mol·L-1,认为Cr3+已经完全沉淀。现将第③步反应后溶液的pH调至4,请通过计算说明Cr3+是否沉淀完全(请写出计算过程)。____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。如图为RFC工作原理示意图,下列有关说法正确的是
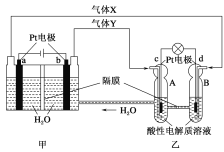
A. 图甲把化学能转化为电能,图乙把电能转化为化学能,水得到了循环使用
B. 当有0.1 mol电子转移时,a极产生0.56 L O2(标准状况下)
C. c极上发生的电极反应为O2+4H++4e-===2H2O
D. 图乙中电子从c极流向d极,提供电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,纤维素与乙酸酐反应可以制取醋酸纤维,同时还有乙酸生成,请写出化学方程式__________________________ ,化学反应类型_________________。已知某纤维乙酸酯的平均相对分子质量为311040,则对应的纤维素分子中平均含有的葡萄糖结构单元数(即聚合度n)是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)写出基态As原子的核外电子排布式________________________。
(2)根据元素周期律,原子半径Ga_____________As,第一电离能Ga____________As。(填“大于”或“小于”)
(3)AsCl3分子的立体构型为____________________,其中As的杂化轨道类型为_________。
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是_____________________。
(5)GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为________________,Ga与As以________键键合。Ga和As的摩尔质量分别为MGa g·mol-1和MAs g·mol-1,原子半径分别为rGa pm和rAs pm,阿伏伽德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为____________________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com