
【题目】分子式为C4H10O并能与金属钠反应放出氢气的有机物有(不含立体异构)( )
A.3 种 B.4 种 C.5 种 D.6 种
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列有关实验操作和实验事故处理不正确的是
A. 用蘸浓盐酸的玻璃棒靠近盛放氨气的装置,检査是否漏气
B. 浓硫酸沾在皮肤上,立刻用稀氢氧化钠溶液冲洗
C. 液溴应保存在棕色磨口玻璃塞的试剂瓶中,并加少量水进行水封
D. 为防止被氧化,FeSO4溶液存放在加有少量铁粉的试剂瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁香醛是常用的一种食用香精。存在下列转化关系:
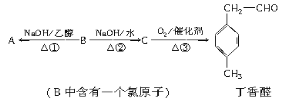
(1)B的分子式为________,C中含氧官能团的名称为________。
(2)反应②的化学方程式为____________________________________。
(3)A发生加聚反应所得产物的结构简式为________________。
(4)与A含有相同官能团的芳香族化合物的同分异构体还有________种(不考虑顺反异构),其中只有一个取代基且不含甲基的物质的结构简式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面给出的是元素周期表的一部分,表中所列小写字母分别代表一种化学元素。
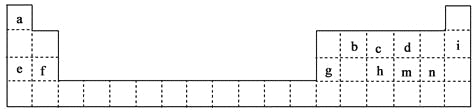
(1)根据上表回答下列问题: ①上述元素中形成物质种类最多的是_________(填元素符号),m的阴离子结构示意图为_________。
②h、m、n所形成的最高价氧化物的水化物的酸性由强到弱的顺序为_________(填化学式)。
③d、e、f、g形成的简单离子的半径由小到大的顺序为_________(用离子符号填写)。
(2)下列能够用来比较m、n两种元素非金属性强弱的有_________。
A.比较这两种元素的气态氢化物的稳定性
B.将这两种元素的单质分别与氢氧化钠溶液反应
C.将n的单质通入到m的氢化物的水溶液中
(3)分别写出下列反应的离子方程式:
g、d形成的化合物 与e、d、a形成化合物的水溶液反应
c的气态氢化物与其最高价氧化物对应的水化物反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是石油化学工业最重要的基础原料,经乙烯为原料可以制得许多工业材料和日用品。乙烯能发生下列转化关系:
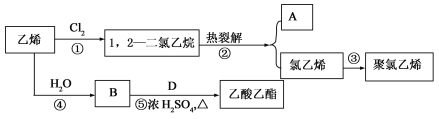
(1)A的分子为 ,化合物D的官能团名称是_____________。
(2)写出反应③、⑤ 的化学方程式 :
③____________________________________________,该反应类型是
⑤_____________________________________________。
(3)上述反应中,以生成有机产物为目标,原子利用率100%的反应有①和 。
(4)甲同学在实验室制得的乙烯中含有少量的二氧化硫,于是设计实验进行验证,将生成的气体依次通过①品红溶液 ②NaOH溶液 ③品红溶液 ④溴的四氯化碳溶液。确定含有乙烯的现象为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.陈年老酒的香气浓是因为乙醇的特殊的香气
B.钠与乙醇的反应比钠与水的反应激烈,发生了取代反应
C.乙烯是重要的化工原料,乙烯的产量可以用来衡量一个国家的石油化工水平
D.乙烯分子所有原子都在同一平面上,丙烯也是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在100 mL 0.8mol/L硝酸溶液中加入足量铜粉,则被溶解的铜的质量为____________g。
(2)在上述溶液中再加入足量稀硫酸,又有_______g铜溶解。此过程中生成的气体在标准状况下的体积为_________L。
(3)若向100 mL 0.8mol/L硝酸溶液中加入铁粉,测得反应后的溶液中Fe2+与Fe3+的浓度之比为1:1,则加入铁的质量为____________g。
(4)向100 mL 0.8mol/L硝酸溶液中加入一定量Fe、FeO、Fe2O3的混合物,充分反应后,放出气体224mL(标准状况下),且测得溶液中铁元素只以Fe2+形式存在,为使Fe2+完全沉淀,可向反应后的溶液中加入0.1mol/L的NaOH溶液___________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锡及其化合物在生产、生活中有着重要的用途。已知: Sn2+易水解、易被氧化;SnCl4极易水解。请按要求回答下列相关问题:
(1)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如下:
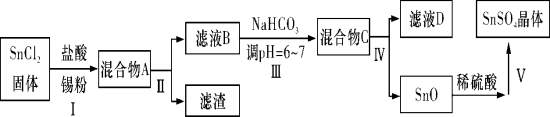
①步骤Ⅰ加入Sn粉的作用: __________________及调节溶液pH。
②步骤Ⅲ生成SnO的离子方程式:____________________________。
③步骤Ⅳ中检验SnO是否洗涤干净的操作是____________ ______,证明已洗净。
④步骤Ⅴ操作依次为____________、____________、过滤、洗涤、低温干燥。
(2)SnCl4蒸气遇氨气及水蒸气呈浓烟状,因而可制作烟幕弹,其反应的化学方程式为:_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com