
【题目】下列有关化学反应速率的说法中,正确的是
A.100 mL 2 mol/L盐酸与锌反应时,加入100 mL氯化钠溶液,生成氢气的速率不变
B.对于可逆反应2CO+2NO![]() N2+2CO2,使用合适的催化剂,CO的生成速率和消耗速率都加快
N2+2CO2,使用合适的催化剂,CO的生成速率和消耗速率都加快
C.二氧化硫的催化氧化是一个放热反应,升高温度,正反应速率减慢
D.用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快氢气的产生
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】磷化铜(Cu3P2)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金,主要用作耐磨零件和弹性原件。
(1)基态铜原子的电子排布式为______;价电子中成对电子数有____个。
(2)磷化铜与水作用产生有毒的磷化氢(PH3)。
①PH3分子中的中心原子的杂化方式是_________。
②P与N同主族,其最高价氧化物对应水化物的酸性:HNO3___H3PO4(填“>”或“<”),从结构的角度说明理由:__________________________。
(3)磷青铜中的锡、磷两元素电负性的大小为Sn___P(填“>”“<”或“=”)。
(4)某磷青铜晶胞结构如图所示。
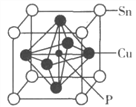
①则其化学式为________。
②该晶体中距离Cu原子最近的Sn原子有______个,这些Sn原子所呈现的构型为_________。
③若晶体密度为8.82g·cm-3,最近的Cu原子核间距为____pm(用含NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学化学中几种常见物质的转化关系如下图(部分严物未列出》。A是一种金属单质,D是一种非金属固体单质。

请回答下列问题:
(1)A、C、E的化学式分别为A________C________E________。
(2)F的浓溶液与A反应过程中,F体现的性质与下列反应中H2SO4体现的性质完全相同的是___________。
A.C+2H2SO4(浓) ![]() CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
B.Fe+H2SO4=FeSO4+H2↑
C.Cu+2H2SO4(浓)=CuSO4+ SO2↑+2H2O
D.FeO+ H2SO4=FeSO4+H2O
(3)写出反应E+H2O2→F的化学方程式:_____________。
(4)若反应F+D→E转移电子数为3.01×1023,,则消耗D的质量为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下某二元弱酸(H2R)电离常数为Ka1=5×10-7,Ka2=5.6×10-11,HClO的Ka=3.0×10-8,回答下列问题:
(1)常温下向NaClO溶液加入少量的H2R溶液发生反应的离子方程式为___________________
(2)常温下pH=3的HClO溶液浓度为C1,pH=4的HClO溶液浓度为C2,则C1____10C2(填“>”、“<”或“=”)
(3)常温下2mol/L的H2R溶液的pH约为_______________
(4)常温下0.1mol/L的NaHR溶液pH__________7(填“>”、“<”或“=”),溶液中的阴阳离子的浓度由大到小的顺序为___________________________________________
(5)常温下,向10 mL 0.1 mol/LH2R溶液中滴加0.1 mol·L-1的KOH溶液V mL
①若混合后的溶液中离子浓度有如下关系:c(K+)=2c(R2-)+c(HR-),V______10(填“>”、“<”或“=”)。
②当混合后的溶液中离子浓度有如下关系:c(K+) = c(R2-)+c(HR-)+c(H2R),则溶液中溶质为_____________,V______10(填“>”、“<”或“=”)。
③当V=30时,混合后的溶液中c(OH-)-c(H+)-c(HR-)-2c(H2R)=________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的数值。乙醚(CH3CH2OCH2CH3)是一种麻醉剂。制备乙醚的方法是2CH3CH2OH![]() CH3CH2OCH2CH3+H2O.下列说法正确的是
CH3CH2OCH2CH3+H2O.下列说法正确的是
A. 18gH218O分子含中子数目为10NA
B. 每制备1molCH3CH218OCH2CH3必形成共价键数目为4NA
C. 10g46%酒精溶液中含H原子个数为1.2NA
D. 标准状况下,4.48L乙醇含分子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2H2(g)+O2(g)===2H2O(l) ΔH=-571.6kJ·mol-1
CO(g)+1/2O2(g)===CO2(g) ΔH=-282.8kJ·mol-1
现有CO、H2、CO2组成的混合气体67.2L(标准状况),经完全燃烧后放出的总热量为710.0kJ,并生成18g液态水,则燃烧前混合气体中CO的体积分数为( )
A. 80% B. 50% C. 60% D. 20%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作、现象与结论均正确的是( )
选项 | 操作 | 现象 | 结论 |
A | 向FeCl3和KSCN混合溶液中,加入少量KCl固体 | 溶液颜色变浅 | FeCl3+3KSCN +3KCl平衡向逆反应方向移动 |
B | 向酸性高锰酸钾溶液中加入过量的FeI2固体 | 反应后溶液变黄 | 反应后溶液中存在大量Fe3+ |
C | 取3mL1 mol·L-1NaOH溶液,先加入3滴1 mol·L-1 MgCl2溶液,再加入3滴1 mol·L-1FeCl3溶液 | 出现红褐色沉淀 | Mg(OH)2的Ksp比Fe(OH)3的Ksp大 |
D | 常温下,向浓度、体积都相同的Na2CO3和NaHCO3溶液中各滴加1滴酚酞 | 变红,前者红色更深 | 结合质子的能力:CO32->HCO3- |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:A2(?)+B2(?) 2AB(?),当温度和压强改变时,n(AB)的变化如下图,下列叙述正确的是

A. A2、B2及AB均为气体,ΔH<0
B. AB为气体,A2、B2至少有一种为非气体,ΔH<0
C. AB为气体,A2、B2有一种为非气体,ΔH>0
D. AB为固体,A2、B2有一种为非气体,ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中充入3 mol A和2 mol B发生如下反应:3A(g)+B(g)![]() xC(g)。该反应达到平衡后,C的体积分数为W%。若维持容器的容积和温度不变,按起始物质的量A 0.6 mol、B 1.2 mol、C 1.6 mol充入容器达到平衡后,C的体积分数还为W%。则x的值( )
xC(g)。该反应达到平衡后,C的体积分数为W%。若维持容器的容积和温度不变,按起始物质的量A 0.6 mol、B 1.2 mol、C 1.6 mol充入容器达到平衡后,C的体积分数还为W%。则x的值( )
A. 只能为2 B. 只能为4 C. 可能为2,可能为4 D. 无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com