
【题目】几种短周期元素的原子半径及主要化合价如表:
元素代号 | X | Y | Z | W | Q |
原子半径 | 160 | 143 | 70 | 66 | 104 |
主要化合价 |
|
|
|
|
|
下列选项正确的是( )
A.X、Y元素的金属性![]()
B.一定条件下,Z单质与W的常见单质直接生成![]()
C.Y的最高价氧化物对应的水化物能溶于氨水
D.Q与W形成的一种化合物可用作纸张漂白剂
【答案】D
【解析】
W化合价为-2价,没有最高正化合价+6价,故W为O元素;
Z元素化合价为+5、+3、-3,Z处于ⅤA族,原子半径与氧元素相差不大,则Z与氧元素处于同一周期,故Z为N元素;
X化合价为+2价,应为ⅡA族元素,Y的化合价为+3价,处于ⅢA族,二者原子半径相差较小,可知两者位于同一周期相邻主族,由于X、Y的原子半径与W、Z原子半径相差很大,则X、Y应在第三周期,所以X为Mg元素,Y为Al元素,结合元素周期律与元素化合物性质解答。
![]() 同周期自左而右金属性减弱,故金属性
同周期自左而右金属性减弱,故金属性![]() ,故A错误;
,故A错误;
B.一定条件下,氮气与氧气反应可以生成NO,故B错误;
C.Y的最高价氧化物对应的水化物为![]() ,
,![]() 能溶于强碱,但不能溶于氨水,故C错误;
能溶于强碱,但不能溶于氨水,故C错误;
D.Q与W形成的一种化合物为![]() ,
,![]() 可用作纸张漂白剂,故D正确;
可用作纸张漂白剂,故D正确;
答案选D。


科目:高中化学 来源: 题型:
【题目】某实验小组用下列装置进行乙醇催化氧化的实验。
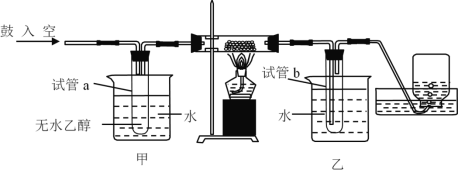
(1)试管a中导管连接方式为___________(填A或B)。
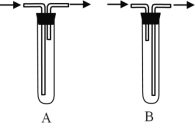
(2)实验过程中铜网出现黑色和红色交替的现象,其中铜丝由黑变红的反应方程式为_________。
(3)反应进行一段时间后,若要检验试管b中收集的物质,进行的操作为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往xg铁铜的混合粉末中加入一定体积某浓度的2.00mol·L-1FeCl3溶液,充分反应后剩余固体的质量与加入FeCl3溶液的体积存在如下关系:
加入FeCl3溶液体积(mL) | 100 | 200 | 300 | 400 |
剩余固体质量(g) | 14.8 | 9.20 | 3.20 | 0 |
下列说法不正确的是
A.x=20.6
B.加入FeCl3溶液300mL充分反应后,剩余固体只有Cu
C.混合粉末中Fe和Cu质量之比为35:16
D.加入FeCl3溶液400mL充分反应后的溶液,还能溶解铁粉8.40g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组测定不同温度下、不同初始浓度的某溶液中R的水解速率,c(R)随时间的变化曲线如图。下列说法不正确的是

A.在0-6min之间,25℃时R的水解速率为0.05 mol·L—1·min—1
B.在0-24min之间,曲线3对应水解速率最小
C.由曲线1可以得出结论:其它条件不变,水解速率随浓度增大而增大
D.由曲线2、3可以得出结论:其它条件不变,水解速率随温度升高而增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面两图均为原电池装置,有关说法错误的是( )
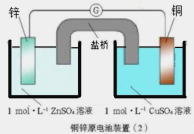
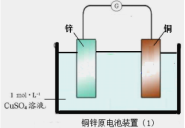
A.锌比铜活泼,锌为负极,发生氧化反应
B.电流从铜电极经导线流向锌电极
C.铜电极发生的反应为:Cu-2e-= Cu2+
D.装置(2)比装置(1)更能清楚揭示出电池中发生的化学反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用0.200 0 mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作如下:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴处充满液体;
③调节液面至“0”或“0”刻度线以下,并记下读数;
④移取20.00 mL待测液注入洁净的还存有少量蒸馏水的锥形瓶中,并加入3滴酚酞试液;
⑤用标准液滴定至终点,记下滴定管液面读数。
请回答下列问题:
(1)以上步骤有错误的是____。
(2)用标准的NaOH溶液滴定待测的盐酸时,左手握_______(填“酸式”或“碱式”)滴定管的活塞,右手摇动锥形瓶,眼睛注视_______________判断滴定终点的现象是____________________。
(3)若测定结果偏高,其原因可能是_____。
a.配制标准溶液的固体NaOH中混有KOH杂质
b.滴定终点读数时,仰视滴定管的刻度,其他操作正确
c.盛装待测液的锥形瓶用蒸馏水洗过后未用待测液润洗
d.滴定管滴定前无气泡,滴定后有气泡
(4)如图是某次滴定时的滴定管中的液面,其读数为_____mL。
![]()
(5)根据下列数据,请计算待测盐酸的浓度:_________mol·L-1。
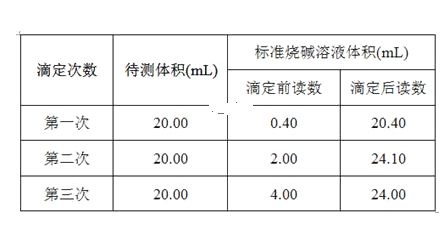
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近几年我国已加大对氮氧化物排放的控制力度。消除氮氧化物污染有多种方法。
(l)用CH4还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
②CH4(g)+4NO (g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol-1
③H2O(g)= H2O(l) △H=-44.0kJ·mol-1
CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(1)的热化学方程式为_________________。
(2)用活性炭还原法也可处理氮氧化物。有关反应为:2C(s)+2NO2(g)=N2(g)+2CO2(g) △H<0,起始时向密闭容器中充入一定量的C(s)和NO2(g),在不同条件下,测得各物质的浓度变化状况如下图所示。

①010min内,以CO2表示的平均反应速率v(CO2)=_______________。
②0~10min,1020 min,3040 min三个阶段NO2的转化率分别为α1、α2、α3,其中最小的为_________,其值是___________________。
③计算反应达到第一次平衡时的平衡常数K=____________。
④第10min时,若只改变了影响反应的一个条件,则改变的条件为______(填选项字母)。
A.增加C(s)的量 B.减小容器体积 C.加入催化剂
⑤20~30min、4050 min时体系的温度分别为T1和T2,则T1_____T2(填“> “<”或“=”), 判断的理由是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,其中X、Y、W、Z为知周期元素,T的单质常温下为液体。下列说法错误的是

A. X、Y的单质均存在同素异形体
B. Y、Z的简单氢化物的稳定性依次递增
C. 工业上电解NaW溶液得W2可使用阴离子交换膜
D. R的单质可用于制造半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图所示的N2(g)和02(g)反应生成NO(g)过程中的能量变化情况判断,下列说法正确的是

A.N2(g)和O2(g)反应生成NO(g)是放热反应
B.2 mol O原子结合生成O2(g)时需要吸收498 kJ能量
C.1 mol NO(g)分子中的化学键断裂时需要吸收632 kJ能量
D.2 mol N(g)和2 mol O(g)的总能量为1444 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com