
【题目】某学生用0.200 0 mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作如下:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴处充满液体;
③调节液面至“0”或“0”刻度线以下,并记下读数;
④移取20.00 mL待测液注入洁净的还存有少量蒸馏水的锥形瓶中,并加入3滴酚酞试液;
⑤用标准液滴定至终点,记下滴定管液面读数。
请回答下列问题:
(1)以上步骤有错误的是____。
(2)用标准的NaOH溶液滴定待测的盐酸时,左手握_______(填“酸式”或“碱式”)滴定管的活塞,右手摇动锥形瓶,眼睛注视_______________判断滴定终点的现象是____________________。
(3)若测定结果偏高,其原因可能是_____。
a.配制标准溶液的固体NaOH中混有KOH杂质
b.滴定终点读数时,仰视滴定管的刻度,其他操作正确
c.盛装待测液的锥形瓶用蒸馏水洗过后未用待测液润洗
d.滴定管滴定前无气泡,滴定后有气泡
(4)如图是某次滴定时的滴定管中的液面,其读数为_____mL。
![]()
(5)根据下列数据,请计算待测盐酸的浓度:_________mol·L-1。
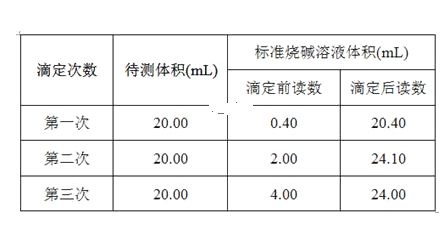
【答案】① 碱式 锥形瓶中的溶液颜色变化 滴入最后一滴NaOH溶液时,溶液刚好由无色变为浅红色,且半分钟内不褪色 ab 22.60 0.200 0
【解析】
(1)根据碱式滴定管在装液前应用所装液体进行润洗;
(2)滴定时标准NaOH应装在碱式滴定管中,眼睛注视锥形瓶内溶液颜色变化,滴定终点时溶液颜色由无色突变为红色,且半分钟内不褪色;
(3)根据![]() 分析不当操作对V(标准)×的影响,以此判断浓度的误差;
分析不当操作对V(标准)×的影响,以此判断浓度的误差;
(4)根据滴定管的结构小数在上、大数在下和精确度为0.01mL解答;
(5)分析表中数据有效性,依据![]() 计算待测液浓度。
计算待测液浓度。
(1)根据碱式滴定管在装液前应用所装液体进行润洗,用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上是错误的,
故答案为:①
(2)滴定时标准NaOH应装在碱式滴定管中,滴定时左手握滴定管,右手摇动锥形瓶,眼睛注视锥形瓶内溶液颜色变化,强碱滴定强酸时达到终点时无色变为浅红色,且半分钟内不褪色,
故答案为:碱式 ; 锥形瓶中的溶液颜色变化; 滴入最后一滴NaOH溶液时,溶液刚好由无色变为浅红色,且半分钟内不褪色;
(3)a.配制标准溶液的固体NaOH中混有KOH杂质,标准溶液中氢氧根离子的浓度偏小,消耗的V(标准)增大,测定结果偏高,故a正确;
b.滴定终点读数时,仰视滴定管的刻度,读取消耗的V(标准)偏大,测定结果偏高,故b正确;
c.盛装待测液的锥形瓶用蒸馏水洗过后未用待测液润洗,测定结果不受影响,故c错误;
d.滴定管滴定前无气泡,滴定后有气泡V(标准)偏小,测定结果偏低,故d错误
故答案选ab。
(4)依据滴定管构造及精确度可知图中液面读数为:22.60;
故答案为:22.60;
(5)三次消耗标准液体积分别为:20.00,22.10,20.00,第二组数据误差较大,应舍弃,则消耗标准液平均体积为:20.00mL,待测液浓度为: 0.2000 mol·L-1×20.00ml÷20.00ml=0.200 0 mol·L-1,
故答案为:0.2000。


科目:高中化学 来源: 题型:
【题目】D是一种催眠药,F是一种香料,它们的合成路线如下:

(1)A的化学名称是___,C中含氧官能团的名称为___。
(2)F的结构简式为___。
(3)A生成B的化学方程式为___。
(4)写出C合成D的第二个反应的化学方程式___。
(5)同时满足下列条件的E的同分异构体有___种(不含立体异构)。
①遇FeCl3溶液发生显色反应 ②能发生银镜反应
(6)以乙炔和甲醛为起始原料,选用必要的无机试剂合成1,3-丁二烯,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。___
HC≡CH![]()

![]()
![]() CH2=CHCH=CH2
CH2=CHCH=CH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,HA的电离常数Ka=1×10-6,向20 mL浓度为0.01 mol·L-1的HA溶液中逐滴加入0.01mol·L-1的NaOH溶液,溶液的pH与加入NaOH溶液的体积之间的关系如图所示,下列说法正确的是( )
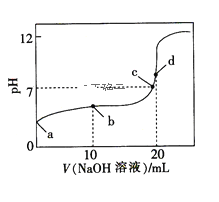
A.a点对应溶液的pH约为4,且溶液中只存在HA的电离平衡
B.b点对应溶液中:c(Na+)>c(A-)>c(HA)>c(H+)>c(OH-)
C.d点对应溶液中:c(OH-)-c(H+)=c(A-)
D.a、b、c、d四点对应的溶液中水的电离程度:a<b<c<d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】几种短周期元素的原子半径及主要化合价如表:
元素代号 | X | Y | Z | W | Q |
原子半径 | 160 | 143 | 70 | 66 | 104 |
主要化合价 |
|
|
|
|
|
下列选项正确的是( )
A.X、Y元素的金属性![]()
B.一定条件下,Z单质与W的常见单质直接生成![]()
C.Y的最高价氧化物对应的水化物能溶于氨水
D.Q与W形成的一种化合物可用作纸张漂白剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国科学家目前开发出了一种新技术,将能放射出![]() 粒子的砹原子装入形状类似DNA螺旋结构的碳纳米管中,这种肉眼看不见的微型“核弹”可以搜索、确认并定向摧毁身体任何部位的癌细胞.下列有关说法中正确的是( )
粒子的砹原子装入形状类似DNA螺旋结构的碳纳米管中,这种肉眼看不见的微型“核弹”可以搜索、确认并定向摧毁身体任何部位的癌细胞.下列有关说法中正确的是( )
A.放射性At原子中,核外电子与核内中子数之差为133
B.根据元素周期律推知:砹单质是![]() 种有色固体,AgAt是一种不溶于水的固体
种有色固体,AgAt是一种不溶于水的固体
C.类似DNA螺旋结构的碳纳米管是一种高分子化合物
D.构成碳纳米管的微粒直径在![]() 之间,它实际上是一种胶体
之间,它实际上是一种胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的数值。则下列有关叙述正确的共有
A.1.4g乙烯与丙烯的混合气体含有NA个碳原子
B.精炼铜,若阳极失去2NA个电子,则阴极增重64g
C.在1L 0.1mol/L的Na2CO3溶液中,阴离子总数小于0.1NA
D.将1L 2mol/L的FeCl3溶液加入到沸水中,加热使之完全反应,所得氢氧化铁胶体粒子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】4种相邻主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性.![]() 称为拟卤素,性质与卤素相似.下列说法不正确的是( )
称为拟卤素,性质与卤素相似.下列说法不正确的是( )
M | N | ||
X | Y |
A.X位于三周期IIA,其单质可采用电解熔融![]() 制备
制备
B.元素最高价氧化物的水化物中,酸性最强的是![]()
C.气体分子![]() 的电子式为
的电子式为![]()
D.![]() 其与氢氧化钠溶液反应的化学方程式为
其与氢氧化钠溶液反应的化学方程式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t ℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。又知t ℃时AgCl的Ksp=4×10-10 mol2·L-2,下列说法不正确的是
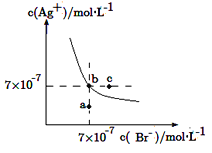
A.在t ℃时,AgBr的Ksp为4.9×10-13 mol2·L-2
B.在AgBr饱和溶液中加入NaBr固体,可使溶液由b点到c点
C.图中a点对应的是AgBr的不饱和溶液
D.在t ℃时,AgCl(s)+Br-(aq)![]() AgBr(s)+Cl-(aq)的平衡常数K≈816
AgBr(s)+Cl-(aq)的平衡常数K≈816
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com