
【题目】氨气是一种重要的化工产品及工业原料。
某温度下,合成氨反应的平衡常数K=3.0×103(mol/L)-1,
(1)写出其对应的化学方程式________________________
(2)某温度下,如果在体积恒定为10L的密闭容器中充入:0.1molN2、0.1molH2和2molNH3则反应_______(填“正向进行”或“逆向进行”或“达到平衡”)。
(3)该温度下,在体积恒定为10L的四个密闭容器中分别充入下列物质,反应达到平衡后,N2的转化率最大的是____________(填字母代号)。
A.10mol N2、30mol H2和20mol NH3
B.10mol N2和30mol H2
C.20mol N2和60mol H2
D.10mol N2和28mol H2
【答案】(1)1/2N2+3/2H2![]() NH3;(2)正向进行;(3)C。
NH3;(2)正向进行;(3)C。
【解析】
试题分析:(1)根据化学平衡常数的定义,达到化学平衡,生成物浓度的幂之积与反应物浓度的幂之积的比值,根据平衡常数的单位,推出其反应方程式为:1/2 N2 + 3/2 H2 ![]() NH3;(2)c(NH3)=2/10mol·L-1=0.2mol·L-1,c(N2)=0.1/10mol·L-1=0.01mol·L-1,c(H2)=0.1/10mol·L-1=0.01mol·L-1,K=c(NH3)/K=c(NH3)/[c1/2(N2)×c3/2(H2)]=2000<3000,平衡向正反应方向移动;(3)A和B对比,A比B多NH3,A达到平衡所用时间小,消耗N2的量少,因此B中N2的转化率大于A中N2转化率,B和D相比,D比B少2mol氢气,B可以看作在D的基础上增加2molH2,平衡向正反应方向移动,N2的转化率:B>D,C可以看作在B的基础上增大压强,增大压强,平衡向正反应方向移动,即C中N2的转化率大于B中,故氮气转化率最大的是选项C。
NH3;(2)c(NH3)=2/10mol·L-1=0.2mol·L-1,c(N2)=0.1/10mol·L-1=0.01mol·L-1,c(H2)=0.1/10mol·L-1=0.01mol·L-1,K=c(NH3)/K=c(NH3)/[c1/2(N2)×c3/2(H2)]=2000<3000,平衡向正反应方向移动;(3)A和B对比,A比B多NH3,A达到平衡所用时间小,消耗N2的量少,因此B中N2的转化率大于A中N2转化率,B和D相比,D比B少2mol氢气,B可以看作在D的基础上增加2molH2,平衡向正反应方向移动,N2的转化率:B>D,C可以看作在B的基础上增大压强,增大压强,平衡向正反应方向移动,即C中N2的转化率大于B中,故氮气转化率最大的是选项C。


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
【题目】在Na2SO4 和 Al2(SO4)3的混合溶液中,测得Al3+浓度为0.1mol/L,SO42-浓度为0.3mol/L,则混合溶液中Na+的浓度为
A.0.15mol/L B.0.45mol/L C.0.6mol/L D.0.3mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了一组实验来探究元素周期律。甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律。图2中,A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸。已知常温下浓盐酸与高锰酸钾能反应生成氯气。
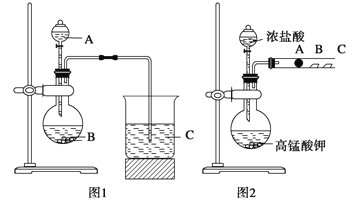
(1)甲同学实验(如图1)中选用的三种物质名称分别为:______________________________;
(2)乙同学实验(如图2)中:A处反应的离子方程式为:_______________________________;
B处的实验现象为:___________________________;
该实验不能完全证明卤素性质的递变规律,请简述原因:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高聚物的合成与结构修饰是制备具有特殊功能材料的重要过程。下图是合成具有特殊功能高分子材料W(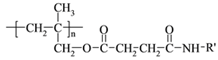 )的流程:
)的流程:
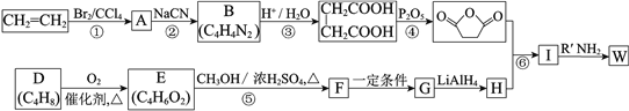
已知:(R、R1、R2代表烃基)
I、![]()
![]() RCH2OH
RCH2OH
II、![]()
⑴反应①的反应类型是_______________。
⑵反应②是取代反应,其化学方程式是___________________________________________。
⑶D的核磁共振氢谱中有两组峰且面积之比是1:3,不存在顺反异构。D的结构简式是______。
⑷反应⑤的化学方程式是__________________________________________________。
⑸G的结构简式是__________________。
⑹反应⑥的化学方程式是__________________________________________________。
⑺工业上也可用![]() 合成E。由上述①~④的合成路线中获取信息,完成下列合成路线(箭头上注明试剂和反应条件,
合成E。由上述①~④的合成路线中获取信息,完成下列合成路线(箭头上注明试剂和反应条件,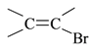 不易发生取代反应)__________________
不易发生取代反应)__________________
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(N2H4)和亚硝酸钠在化工生产及航天工业中具有十分广泛的应用,下图是以液氨为原料生产肼和亚硝酸钠的工艺流程(肼能与水混溶,形成稳定的N2H4H2O):
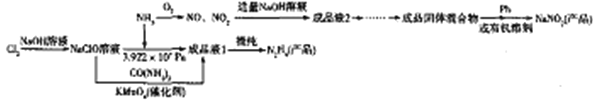
回答下列问题:
(1)NaNO2中N的化合价为_______。
(2)写出在NaClO溶液中通入NH3得到成品液1的化学反应方程式:______________。
(3)由成品液2得到成品固体混合物需经过的操作步骤为________________。
(4)亚硝酸钠在一定条件下能与无水肼反应生成一种钠氮化合物和水,生成的钠氮化合物中钠的质量分数为35.38%。则反应中氧化剂与还原剂的物质的量之比为_____;该反应中的氧化产物是___________________。
(5)已知所得成品固体混合物中含有2种钠盐,若要获得NaNO2产品,则需要除去的物质为_______(填化学式);使用Pb进行处理时,杂质能转变为NaNO2,而Pb转化成PbO,则这一处理过程发生反应的化学方程式为___________;已知,NaNO2在邻苯二甲酸二丁酯中溶解度远大于在水中的溶解度,而另一钠盐则不具有该性质,若用有机溶剂邻苯二甲酸二丁酯处理成品固体混合物水溶液时,NaNO2 与另一钠盐通过_____(填操作名称)被分离。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酱油是一种常用调味剂,根据国标要求酱油中NaCl的含量不应低于15 g /100 mL。莫尔法是较简单的一种测量Cl-含量的方法。现采用该法测量某市售酱油是否符合NaCl含量标准要求。实验原理如下(25℃):Ag++ Cl-=" AgCl" (白色)Ksp(AgCl)=1.8×l0-10
2 Ag++ Cr042-= Ag2Cr04(砖红色)Ksp(Ag2Cr04)=1.2×10-12
准确移取酱油样品5.00 mL稀释至100 mL,从其中取出10.00 mL置于锥形瓶中,再向其中加入适量的铬酸钾溶液,以0.1000 mol/L的硝酸银标准溶液滴定,重复实验三次。
(1)样品稀释过程中,用 移取酱油样品,应在 中定容,还需用到的玻璃
仪器有_____________。
(2)标准硝酸银溶液用棕色滴定管盛装的原因是__________。滴定中眼睛应注视 ,出现 即达到滴定终点。

(3)滴定结束时,滴定管中液面如上图所示,则读数为_____________。
(4)若三次消耗硝酸银标准溶液的平均体积为12.50 mL,则稀释后的酱油中NaCl的浓度为 mol/L,该市售酱油是否符合NaCl含量标准 (填“符合”或“不符合”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
①0.1 mol·L-1NaAlO2溶液:H+、Na+、Cl-、SO![]()
②pH=11的溶液中:CO32-、Na+、AlO2-、NO3-、S2-、SO32-
③水电离的H+浓度为10-12mol·L-1的溶液中:Cl-、CO32-、NO3-、SO32-
④加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、K+、SO42-、NO3-
⑤使甲基橙变黄的溶液中:Fe2+、MnO4-、NO3-、Na+、SO42-
⑥中性溶液中:Fe3+、Al3+、NO3-、Cl-
A.②④⑥ B.②⑥ C.② D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平衡,使镁原电池越来越成为人们研制绿色原电池的关注焦点。其中一种镁原电池的反应为xMg+Mo3S4![]() MgxMo3S4;在镁原电池放电时,下列说法错误的是 ( )
MgxMo3S4;在镁原电池放电时,下列说法错误的是 ( )
A.Mg2+向正极迁移
B.正极反应为:Mo3S4+2xe-===Mo3S![]()
C.Mo3S4发生氧化反应
D.负极反应为:xMg-2xe-===xMg2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com