
����Ŀ��ij���жԴ������м�⣬���ָ�����Ҫ��Ⱦ��Ϊ�����������PM2.5(ֱ��С�ڵ���2.5��m������������)������Ҫ��ԴΪȼú��������β���ȡ���ˣ���PM2.5��SO2��NOx�Ƚ����о�������Ҫ���塣��ش��������⣺
��1��PM2.5��ɢ�ڿ������γɵķ�ɢϵ__(����������������������)���塣
��2����PM2.5����������ˮ�����Ƴɴ�������������ø���������ˮ���������ӵĻ�ѧ��ּ���ƽ��Ũ�����±���
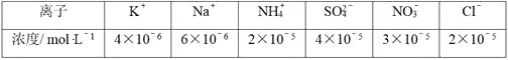
���ݱ��������жϴ�������Ϊ__(����������������)�ԣ���ʾ����������Ե�c(H��)��c(OH��)=__mol��L-1��
��3��úȼ���ŷŵ���������SO2��NOx���γ����꣬��Ⱦ����������NaClO2��Һ�ڼ��������¿ɶ�������������������Ч���dz��á�������ж������������̵����ӷ���ʽ��
__ClO2-��__NO��__=__Cl-��__NO3-��__
��4��Ϊ����SO2���ŷţ�����ȡ�Ĵ�ʩ�У�
�ٽ�úת��Ϊ�������ȼ�ϡ�д����̿��ˮ������Ӧ�Ļ�ѧ����ʽ��__��
��ϴ�Ӻ�SO2���������������ʿ���ϴ�Ӽ�����__(����ĸ)��
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
��5������β����NOx��CO�����ɼ�ת����
�����������������¶�Խ�ߣ���λʱ����NO�ŷ���Խ��д������������NO�Ļ�ѧ����ʽ��__��
������ȼ�Ͳ���ȫȼ��ʱ����CO��Ŀǰ��������β��ϵͳ��װ�ô�ת�����ɼ���CO��NO����Ⱦ���仯ѧ��Ӧ����ʽΪ__��
���𰸡������� �� 10-4 3 4 4OH- 3 4 2H2O C��H2O(g)![]() CO��H2 ab N2+O2
CO��H2 ab N2+O2![]() 2NO 2CO+2NO
2NO 2CO+2NO![]() 2CO2+N2
2CO2+N2
��������
��1������ķ�ɢϵ�з�ɢ�ʵ�ֱ����1��100nm��
��2���۲�����з������к���![]() ��
��![]() ˮ�������ԣ�PM2.5��Ϊ���ԣ�
ˮ�������ԣ�PM2.5��Ϊ���ԣ�
��3����Ӧ��NԪ�ػ��ϼ���+2�۵�NO����Ϊ![]() ��+5�ۣ�������3�ۣ�ClԪ����
��+5�ۣ�������3�ۣ�ClԪ����![]() ��+3�۽���Ϊ1�ۣ�������4�ۣ����ϼ�������С������Ϊ12����
��+3�۽���Ϊ1�ۣ�������4�ۣ����ϼ�������С������Ϊ12����![]() ϵ��Ϊ3����NOϵ��Ϊ4�����õ���غ㼰Ԫ���غ���ƽ���ʵ�ϵ����
ϵ��Ϊ3����NOϵ��Ϊ4�����õ���غ㼰Ԫ���غ���ƽ���ʵ�ϵ����
��4����̼��ˮ������Ӧ����һ����̼���������ڶ�������Ϊ������������ն���������Լ��Ͷ�����������Ӧ��
��5�������������������¶�Խ�ߣ���λʱ����NO�ŷ���Խ������������NO�ǿ����е����������ŵ�����һ����������������β��ϵͳ��װ�ô�ת�����ɼ���CO��NO����Ⱦ��һ����̼��һ�����������������ɵ����Ͷ�����̼��
��1������ķ�ɢϵ�з�ɢ�ʵ�ֱ����1��100nm��PM2.5��ָ������ֱ���ӽ���2.5��106m�Ŀ����ֱ������100nm����ϸ�������ɢ�ڿ������γɵķ�ɢϵ���ǽ��壬
�ʴ�Ϊ�������ڣ�
��2���۲�����з���![]() ˮ�������ԣ�PM2.5�������Ϊ���ԣ�������pHֵ������Һ�е���غ����õ���
ˮ�������ԣ�PM2.5�������Ϊ���ԣ�������pHֵ������Һ�е���غ����õ���![]() ����������ֵ��������ʽ�ӿɵ�c(H+)=1.0��104mol/L��������Ũ��Ϊ104mol/L��
����������ֵ��������ʽ�ӿɵ�c(H+)=1.0��104mol/L��������Ũ��Ϊ104mol/L��
�ʴ�Ϊ���104��
��3����Ӧ��NԪ�ػ��ϼ���+2�۵�NO����Ϊ![]() ��+5�ۣ�������3�ۣ�ClԪ����
��+5�ۣ�������3�ۣ�ClԪ����![]() ��+3�۽���Ϊ1�ۣ�������4�ۣ����ϼ�������С������Ϊ12����
��+3�۽���Ϊ1�ۣ�������4�ۣ����ϼ�������С������Ϊ12����![]() ϵ��Ϊ3����NOϵ��Ϊ4������ݵ���غ㡢Ԫ���غ㼰��Ӧ�ڼ��������½��У�����ƽ�õķ���ʽΪ��
ϵ��Ϊ3����NOϵ��Ϊ4������ݵ���غ㡢Ԫ���غ㼰��Ӧ�ڼ��������½��У�����ƽ�õķ���ʽΪ��![]() ��
��
�ʴ�Ϊ��3��4��4OH��3��4��2H2O��
��4���ٽ�̿��ˮ������Ӧ����ˮú���Ļ�ѧ����ʽΪ��C��H2O(g)![]() CO��H2��
CO��H2��
�ʴ�Ϊ��C��H2O(g)![]() CO��H2��
CO��H2��
��a������������������������Ծ��������������ͨ�ԣ��ܹ���Ӧ��SO2+Ca(OH)2=CaSO3��+H2O����a��ȷ��
b����������ˮ��Һ�������ᣬ����Ҳ�ܹ���̼���Ʒ�Ӧ��SO2+Na2CO3=Na2SO3+CO2�������Կ�����̼������Һ��ϴ�Ӽ�����b��ȷ��
c�������������Ȼ�����Һ����Ӧ����c����
d��SO2��������������Һ�е��ܽ�Ⱥ�С�����Բ�����������������Һ��ϴ��Һ����d����
�ʴ�Ϊ��ab��
��5���٣�����������NO�ǿ����е����������ŵ�����һ����������Ӧ�Ļ�ѧ����ʽΪ��N2+O2![]() 2NO��
2NO��
�ʴ�Ϊ��N2+O2![]() 2NO��
2NO��
�ڣ�������β��ϵͳ��װ�ô�ת�����ɼ���CO��NO����Ⱦ��һ����̼��һ�����������������ɵ����Ͷ�����̼����Ӧ�Ļ�ѧ����ʽ��2CO+2NO![]() 2CO2+N2��
2CO2+N2��
�ʴ�Ϊ��2CO+2NO![]() 2CO2+N2��
2CO2+N2��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����ѧϰС����ճ������в���ȱ�ٵĵ�ζƷM����̽������֪C����D��ȼ�շ�����ɫ���档M���������ʵ�ת����ϵ��ͼ1��ʾ(���ֲ�������ȥ)��
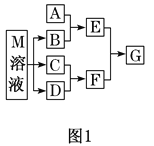
(1)д��B�ĵ���ʽ________��
(2)��A��һ�ַǽ������ʣ��ҿ���������뵼����ϣ�д��A��Bˮ��Һ��Ӧ�����ӷ���ʽ__________________________��
(3)��A��CO2���壬A��B��Һ�ܹ���Ӧ����Ӧ�����õ���Һ�������ᷴӦ�����ɵ�CO2���ʵ������������������ͼ2��ʾ����A��B��Һ��Ӧ����Һ���������ʵĻ�ѧʽΪ_____________��c(HCl)=________mol/L��
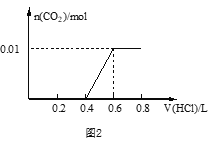
(4)��A��һ�ֳ����������ʣ���A��B��Һ�ܹ���Ӧ��������F��Һ��μ���E��Һ���ӱ�����������ʵ��������______________________________________��
(5)��A��һ�ֿ����������ʵĻ�����, A��B��Ӧ����������E��E��F��E��D������ð���̣�������E��D�ķ�Ӧ��������D�Ĺܵ��Ƿ�й¶��д��E��D��Ӧ�Ļ�ѧ����ʽΪ___________________��
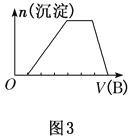
(6)��A��һ����Һ�����ܺ���H����NH![]() ��Mg2����Fe3����Al3����CO32-��SO42-�е�ijЩ���ӣ��������Һ�м���B��Һʱ�������ɳ��������ʵ�����B��Һ����������仯��ͼ3��ʾ���ɴ˿�֪������Һ�п϶����е�������_____________________�����ǵ����ʵ���Ũ��֮��Ϊ______________��
��Mg2����Fe3����Al3����CO32-��SO42-�е�ijЩ���ӣ��������Һ�м���B��Һʱ�������ɳ��������ʵ�����B��Һ����������仯��ͼ3��ʾ���ɴ˿�֪������Һ�п϶����е�������_____________________�����ǵ����ʵ���Ũ��֮��Ϊ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£�Na2S��Һ�д���ˮ��ƽ�⣺S2����H2O![]() HS����OH��������˵����ȷ����(����)
HS����OH��������˵����ȷ����(����)
A. ϡ����Һ��ˮ��ƽ�ⳣ������B. ����CuSO4���壬HS��Ũ�ȼ�С
C. �����¶ȣ�c(HS��)/c(S2��)��СD. ����NaOH���壬��ҺpH��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Q��W��X��Y��Z���ֶ�����Ԫ�������ڱ��е����λ������ͼ��ʾ������W�ĵ�����һ����Ҫ�뵼����ϡ�
|
|
| Y |
|
Q | W | X |
| Z |
�밴Ҫ��ش��������⣺
(1)Y��ԭ�ӽṹʾ��ͼΪ________����һ��˵��Z�ķǽ����Ա�X�ķǽ�����ǿ����ʵ��________��
(2)W��X��Y��ԭ�Ӱ뾶�ɴ�С����![]() ��Ԫ�ط���
��Ԫ�ط���![]() ________��W��Z�γɵĻ��������ʽΪ________��
________��W��Z�γɵĻ��������ʽΪ________��
(3)��Z�ĵ���ͨ�뵽�������ʵ���FeBr2��Һ�г�ַ�Ӧ�����ӷ���ʽΪ________��
(4)��֪�� 2Na(s)+![]() Y2(g)=Na2Y(s)H=-414kJ/mol��2Na(s)+Y2(g)=Na2Y2(s)H=-511kJ/mol����Na2Y(s)ת��ΪNa2Y2(s)�ķ�Ӧһ�����������Է����е�������________����0.2mol Na2Y2���뵽100mL1mol/L��QZ3�У���ַ�Ӧ�Ļ�ѧ����ʽΪ________��
Y2(g)=Na2Y(s)H=-414kJ/mol��2Na(s)+Y2(g)=Na2Y2(s)H=-511kJ/mol����Na2Y(s)ת��ΪNa2Y2(s)�ķ�Ӧһ�����������Է����е�������________����0.2mol Na2Y2���뵽100mL1mol/L��QZ3�У���ַ�Ӧ�Ļ�ѧ����ʽΪ________��
(5)R��Wͬ���ڣ���֪����T��ʱKsp[R(OH)2]��ֵΪ4.0��10-12����R(OH)2������Һ��c(OH-)=________mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���Է�Һ����H+��Fe3+��Ni2+��NO3����F-��Cr2O72-�ȡ���ͼ�Ǹ÷�Һ���ۺ����ù������̣������裺 F����������ӵ���Ϸ�Ӧ��Ӱ��������Ӧ�ͼ��㣩
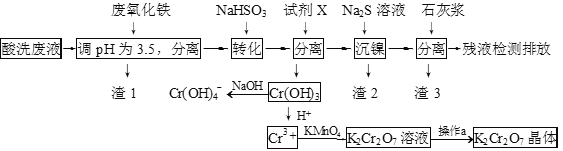
��֪���������ӿ�ʼ�����ͳ�����ȫʱ��pH��
Fe3+ | Ni2+ | Cr3+ | |
��ʼ���� | 1.5 | 6.7 | 4.0 |
������ȫ | 3.4 | 9.5 | 6.9 |
Ni2+��������ˮ�ķ�ӦΪ��Ni2+��6NH3 ![]() [Ni(NH3)6]2+��[Ni(NH3)6]2+Ϊ�ѵ����������ӣ�
[Ni(NH3)6]2+��[Ni(NH3)6]2+Ϊ�ѵ����������ӣ�
��1������1����Ҫ�ɷ�Ϊ��____________��
��2���Լ�X������������ˮ���������ǣ�____________ ��������ţ�
A��Ni(OH)2 B��Cr2O3 C��Fe2O3 D��NaOH
��3�����Լ�X��������ˮ���������������ӷ���ʽΪ��____________��
��4������⣬���IJ�Һ��c(Ca2+)��1.0��10��5 molL-1�����Һ��F��Ũ��____________���� �����������������������ŷű�[��֪Ksp(CaF2)=4��10-11�������ŷű�Ҫ�������Ũ��С��10 mgL��1]��
��5����(Ni)���仯����㷺Ӧ����������ء���ƺʹ���������
��ij���ط�ӦΪNiO2��Fe��2H2O![]() Fe(OH)2��Ni(OH)2,�ŵ�ʱ�����·��ת��0.6mol��������������____g��
Fe(OH)2��Ni(OH)2,�ŵ�ʱ�����·��ת��0.6mol��������������____g��
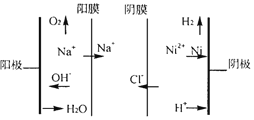
��ͼΪ˫Ĥ���ҵ�ⷨ����������ˮ���ս�������ԭ��ʾ��ͼ�������ĵ缫��ӦʽΪ____���������У���Ҫ������ҺpHֵΪ4���ң�ԭ����_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʮ�Ŵ������Ҫ����Ӯ���챣��ս������ζ�Ŷ���Ⱦ���αȹ�ȥҪ����ߡ�ij������������Һʵ�ַ��硢������λһ���ϵ�װ��ʾ��ͼ���£�����װ�ù���ʱ������˵����ȷ����
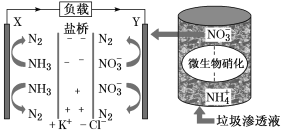
A.������Cl-��Y���ƶ�
B.��·������7.5 mol����ʱ����������״����N2�����Ϊ16.8L
C.������X���ص�������Y��
D.Y�������ķ�ӦΪ2NO3-��10e-��6H2O===N2����12OH������ΧpH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���CO2ͨ��2LpH=12��KOH��Һ�У���Һ��ˮ�����OH-����Ũ��(��)��ͨ���CO2�����(V)�Ĺ�ϵ����ͼ��ʾ��������������ȷ����

A��a����Һ�У�ˮ�������c(H+)=1��10-12mol/L
B��b����Һ�У�c(H+)=1��10-7mol/L
C��c����Һ�У�c(K+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)]
D��d����Һ�У�c(K+)=2c(CO32-)+c(HCO3-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.�����£�1mol��L-1��CH3COOH��Һ��1mol��L-1��NaOH��Һ�������Ϻ����û��Һ�У�c(Na��)��c(CH3COO-)��c(H��)��c(OH-)
B.�ں��з�̪��0.1mol/L��ˮ�м���������NH4Cl���壬��Һ��ɫ��dz
C.������ĵ��뷽��ʽΪ��H2S![]() 2H++S2��
2H++S2��
D.0.1mol/LNa2CO3��Һ�У�2c(Na��)=c(CO32-)+c(HCO3-)+c(H2CO3)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Һ�ĵ絼��Խ��������Խǿ����0.1mol��L��1��NaOH��Һ�ֱ�ζ������Ϊ10.00mL��Ũ�Ⱦ�Ϊ0.1mol��L��1�������CH3COOH��Һ�����ô�������õζ���������Һ�ĵ絼����ͼ��ʾ������˵������ȷ���ǣ� ��
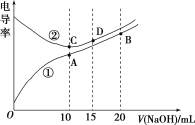
A.���ߢٴ����ζ�CH3COOH��Һ������
B.A����Һ�У�c(CH3COO��)��c(OH��)��c(H��)��0.05mol��L��1
C.����ͬ�¶��£�A��B��C������Һ��ˮ�����c(H��)��B<A��C
D.D����Һ�У�c(Cl��)��2c(OH��)��2c(H��)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com