
【题目】电解质溶液的电导率越大,导电能力越强。用0.1mol·L-1的NaOH溶液分别滴定体积均为10.00mL、浓度均为0.1mol·L-1的盐酸和CH3COOH溶液,利用传感器测得滴定过程中溶液的电导率如图所示。下列说法不正确的是( )
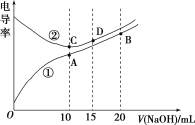
A.曲线①代表滴定CH3COOH溶液的曲线
B.A点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.05mol·L-1
C.在相同温度下,A、B、C三点溶液中水电离的c(H+):B<A=C
D.D点溶液中:c(Cl-)=2c(OH-)-2c(H+)
【答案】C
【解析】
A.浓度相同的醋酸和盐酸,醋酸电离程度小于盐酸,则c(H+)盐酸大于醋酸,c(H+)越大溶液导电性越强,所以相同浓度的盐酸和醋酸,盐酸导电性大于醋酸,根据图知导电性①<②,所以①代表滴定CH3COOH溶液的曲线,选项A正确;
B.A点醋酸和NaOH恰好完全反应生成醋酸钠,溶液中存在电荷守恒c(CH3COO-)+c(OH-)- c(H+)=c(Na+),二者等体积混合时c(Na+)是原来的一半,所以A点溶液中:c(CH3COO-)+ c(OH-)- c(H+)=0.05 mol.L-1,选项B正确;
C.相同温度下,A点溶液中溶质为醋酸钠、B点溶液中溶质为等物质的量浓度的醋酸和醋酸钠、C点溶液中溶质为NaCl,酸或碱抑制水电离,含有弱离子的盐促进水电离,所以B点抑制水电离、A点促进水电离、C点不促进也不抑制水电离,则在相同温度下,A、B、C三点溶液中水电离的c(H+):B<C<A,选项C错误;
D.D点溶液中溶质为NaCl和NaOH,且c(NaCl)=2c(NaOH),溶液中存在物料守恒和电荷守恒,根据电荷守恒得c(Cl-)+ c(OH-)= c(H+)+ c(Na+),根据物料守恒得3c(Cl-)=2 c(Na+),所以得c(Cl-)=2 c(OH-)-2 c(H+),选项D正确;
答案选C。


科目:高中化学 来源: 题型:
【题目】已知甲为恒压容器、乙为恒容容器。相同条件下充入等物质的量的NO2气体,且起始时体积相同。发生反应:2NO2(g)![]() N2O4(g)△H<0。一段时间后达到平衡状态,下列说法中正确的是
N2O4(g)△H<0。一段时间后达到平衡状态,下列说法中正确的是
A.该反应的平衡常数表达式K=![]()
B.达到平衡所需时间,甲与乙相等
C.平衡时NO2体积分数:甲<乙
D.若两容器内气体的压强保持不变,均说明反应已达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A. 苯酚钠溶液中通入少量的二氧化碳,产物是苯酚和碳酸钠
B. 苯的同系物中,苯环和侧链相互影响,使得二者均易被氧化
C. ![]() 在核磁共振氢谱中出现两组峰,其氢原子数之比为3∶2
在核磁共振氢谱中出现两组峰,其氢原子数之比为3∶2
D. 苯甲酸、苯乙烯分子中的所有原子可能处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W四种短周期元素的位置如下图所示,X形成的单质约占空气体积的![]() ,四种元素原子核外共有56个电子,请回答下列问题:
,四种元素原子核外共有56个电子,请回答下列问题:

(1)Y的元素符号是_______。
(2)X与Na形成淡黄色固体化合物的化学式是__,该化合物与二氧化碳反应的化学方程式是__。
(3)ZX2能使品红溶液褪色,ZX2的化学式是______,说明ZX2具有_______性。
(4)W2与氢氧化钠溶液反应的离子方程式是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《茉莉花》是一首脍炙人口的江苏民歌。茉莉花香气的成分有多种,乙酸苯甲酯是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成。一种合成路线如下:

(1)A的结构式为 ________________;C的结构简式为_________________;
(2)写出反应①的化学方程式_________________;
(3)反应③的反应类型为__________________;
(4)C通常有三种不同类别的芳香族同分异构体,试写出另两种不同类别的同分异构体的结构简式(各写一种)______________;_______________。
(5)反应 ________(填序号)原子的理论利用率为100%,符合绿色化学的要求。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、X、Y、Z原子序数依次增大,A元素所处的周期数、主族序数、原子序数均相等,B的气态氢化物是天然气的主要成分,Y的最外层电子数是其内层电子数的3倍 ,Z单质可制成半导体材料,B、Z同主族。
①写出Z的原子结构示意图_______________________。
②元素Y在周期表中的位置________________________。
③A与X可形成电子总数为10的微粒,其中形成的分子的结构式为_______________,形成的离子的化学式为_________________。
④较化合物BY2与ZY2的熔点高低:___________>___________(填化学式),因为ZY2属于________晶体(填晶体类型),熔化时需破坏___________(填“共价键”、“离子键”或“分子间作用力”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法不正确的是( )
A.向0.1mol·L-1 CH3COONa溶液中加入少量水,溶液中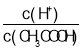 减小
减小
B.将FeCl3溶液和Fe2(SO4)3溶液分别加热、蒸干、灼烧,所得固体成分不同
C.向盐酸中加入氨水至中性,溶液中![]() =1
=1
D.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中![]() 不变
不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,表中所列的字母分别代表一种化学元素。
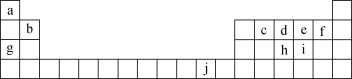
回答下列问题:
(1)写出元素f的基态原子核外电子排布式:____。
(2)写出元素h的基态原子核外电子轨道表示式:________。
(3)基态b原子电子占据最高能级的电子云轮廓图为_________
(4)ce2分子的电子式为____。
(5)d、g、h的原子半径由小到大的顺序是_______(用元素符号表示)
(6)用一个化学方程式证明e、i的非金属性的强弱_________。
(7)d的简单氢化物比h的简单氢化物沸点____(填“高”或“低”),请分析其原因____,写出j的原子结构示意图_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知酸性:H2SO4>![]() >H2CO3>
>H2CO3>![]() > HCO3—,综合考虑反应物的转化率和原料成本等因素,将
> HCO3—,综合考虑反应物的转化率和原料成本等因素,将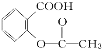 转变为
转变为![]() 的方法有
的方法有
A. 与足量的NaOH溶液共热后,再加入适量H2SO4
B. 与足量的NaOH溶液共热后,再通入足量CO2
C. 与稀H2SO4共热后,加入足量的NaHCO3溶液
D. 与稀H2SO4共热后,加入足量的Na2CO3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com