
����Ŀ�����⻯��(NaBH4)����ǿ��ԭ�ԣ��ڹ�ҵ�����Ϲ㷺���ڷǽ������������ϵĻ�ѧ��Ĥ����������ա���ҵ��ˮ�����ȡ���ҵ�ϲ��õ�Bayer���Ʊ�NaBH4ͨ��������(��ͼ)������˵���������
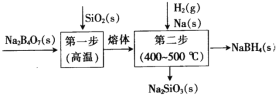
A.��B2O3����Na2B4O7Ҳ���Ƶ�NaBH4
B.�������ܷ�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ2��1
C.��SiO2����������õ����������
D.��ͼ��֪�ù��չ���������Ⱦ�����ʲ�����������ɫ��ѧ����
���𰸡�B
��������
���ݹ������̿�֪����ҵ�ϲ��õ�Bayer���Ʊ�NaBH4��һ��Ϊ��Na2B4O7���ɱ�ʾΪNa2O��2B2O3������SiO2�ڸ����·�Ӧ�õ����壬�ڶ�������������Na��H2��400![]() ~500
~500![]() �����·�����Ӧ����NaBH4��Na2SiO3�Ĺ��̣����������ԭ��Ӧ�Ĺ��ɡ�Ӱ�컯ѧ��Ӧ���ʵ����ء���ɫ��ѧ�ĸ����֪ʶ��������
�����·�����Ӧ����NaBH4��Na2SiO3�Ĺ��̣����������ԭ��Ӧ�Ĺ��ɡ�Ӱ�컯ѧ��Ӧ���ʵ����ء���ɫ��ѧ�ĸ����֪ʶ��������
A. Na2B4O7�ɱ�ʾ��Na2O��2B2O3�������ʽ�������Ʊ�NaBH4�����У�Ҳ����B2O3����Na2B4O7��ԭ�ϣ���A��ȷ��
B. �������ܷ�Ӧ��BԪ�ػ��ϼ�δ�䣬������HԪ�ػ��ϼ۴�0�۽��͵�-1�ۣ�����ԭ������������NaԪ�ػ��ϼ۴�0�����ߵ�+1�ۣ�����������ԭ�������������뻹ԭ�������ʵ���֮��Ϊ1:2����B����
C. ��SiO2���飬������Ӧ�й���ĽӴ�������Ӷ�������õ���������ʣ���C��ȷ��
D. ��ͼ��֪�ù��չ��������Ʊ�����������Ⱦ�����ʲ������������ɫ��ѧ�����D��ȷ��
��ѡB��


 �߽�������ϵ�д�
�߽�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�ΪԪ�����ڱ���һ���֣���ش��й����⣺
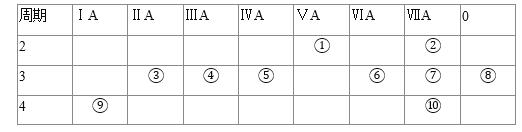
(1)�ٺ͢ݵ�Ԫ�ط����� ______ �� ______ ��
(2)��������õĽ����� ______ ���ǽ�������ǿ��Ԫ���� ______ ![]() ��дԪ�ط���
��дԪ�ط���![]()
(3)�������γ��������������Ԫ���� ______ ![]() ��дԪ�ط���
��дԪ�ط���![]() ���ֱ�д����Ԫ�ص�����������ޢ�����������ˮ���ﷴӦ�Ļ�ѧ����ʽ�� ______ �� ______ ��
���ֱ�д����Ԫ�ص�����������ޢ�����������ˮ���ﷴӦ�Ļ�ѧ����ʽ�� ______ �� ______ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
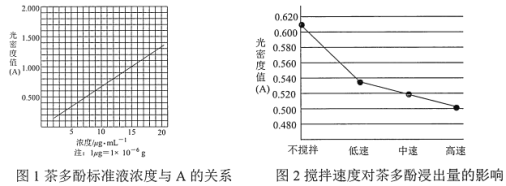
����Ŀ����Ҷ�еIJ�����һ����Ȼ�����������俹���������� VC �� 5��10 ��������������ˮ���Ҵ��������������������ȷ¡������Խ����У������ܽ� Fe3+��ԭΪ Fe2+��Fe2+�� K3Fe(CN)6���ɵ�����ɫ��λ������ KFe[Fe(CN)6]���ض�����������ճ̶ȣ��ù��ܶ�ֵ A ��ʾ���������һ��Ũ�ȷ�Χ�ڳ����ȡ�A ����ӱ�ҺŨ�ȵĹ�ϵ��ͼ 1 ��ʾ��
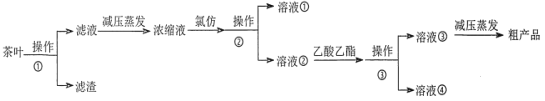
ijʵ��С���������ʵ�����̴Ӳ�Ҷ����ȡ���ӣ�
��ش��������⣺
(1)��������ˮ��ȡ����ʱ��ʵ��С�鷢�ֽ����ٶȶԲ��ӽ�������Ӱ����ͼ 2 ��ʾ��ԭ����____�������Ҵ���ȡ���Ӳ������£���ȡ 10 g ��Ҷĩ������ֽ���ã�װ���ѹ��Һ©���У�Բ����ƿ�ڼӷ�ʯ�������Ҵ�����ͼ 3 ��װ�� ͨ����ˮ���������ȣ����Ҵ������ȷ��ں��Ƽ������¶��� 90�档Ϊʹ��ѹ©����Һ��߳���Ҷ��Լ 0.5 cm��������Լ 1 h�����еIJ���������________��
(2)��ѹ���������һ���������ŵ���________���ȷµ�������________��
(3)�����й�ʵ�������������ȷ����________��
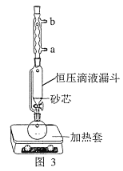
A��ͼ 3 ������ˮ����Ϊ a �� b ��
B����Һ©��ʹ��ǰ������Ƿ�©ˮ��ϴ������
C�������ٹ���ʱ�����ò������ʵ������Լӿ�����ٶ�
D����ȡ�����У�����ҡ����������Һ©��������Ȧ��������Һ
(4)��ȡ 1.25 g �ֲ�Ʒ��������ˮ�ܽⲢ������ 1000 mL����ȡ����Һ 1.00 mL���ӹ��� Fe3+�� K3Fe(CN)6 ������Һ��������ˮ������ 100 mL �����Һ���ܶ�ֵ A=0.800�����Ʒ�Ĵ�����_____ ��������������ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������װ��ͼ���й�˵����ȷ���ǣ� ��
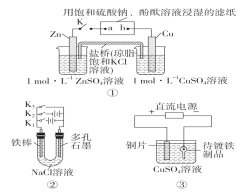
A.װ�â���K���պ�ʱ��Ƭ�̺�CuSO4��Һ��c(Cl-)����
B.װ�â���K���պ�ʱ��Ƭ�̺�ɹ۲쵽��ֽa����ɫ
C.װ�â�������ʴ�������ɴ�С˳���ǣ�ֻ�պ�K1>ֻ�պ�K3>ֻ�պ�K2>���Ͽ�
D.װ�â��е�����Ʒ������1.6gͭʱ����Դ��������ĵ�����Ϊ0.025NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����������ͼ��ʾװ����ȡ����İ�����

(1)д��A��������Ӧ�Ļ�ѧ����ʽ�� __________________________________________��
(2)�ܷ�����ˮ���ռ�������Ϊʲô��________________________________________________________________________��
(3)�����Թ�C�а����Ƿ���������ʪ��ĺ�ɫʯ����ֽ�⣬���ɲ������ּ�����(��������������ͽ���)?________________________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������к͵ζ�����ѧ��ѧ�Ķ�������ֶ�֮һ��С����ѧϰ������ݺ���һ�����⣺�ܲ��ܼ������ð״��д����Ũ�ȡ���������������²���(����״���ֻ�д��������������Ʒ�Ӧ����
��1������100mL1mol/L�������Ʊ���Һ���˹�������Ҫ�IJ�������Ϊ___��
��2����___�����������ƣ���ˮϴ�������������Ʊ���Һ��ϴ�����������Ʊ���Һ����̶ȣ��̶��ڵζ��ܼ��ϣ���___�����������ƣ�ȷ��ȡ20.00ml�״�������ƿ�У�������ƿ�м���������̪��Һ��
��3�����еζ�����д���ζ��յ�ʱ������___��
��4����βⶨ��ƽ�������������Ƶ����Ϊ16.00mL����״��д���Ũ��Ϊ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����H+(aq)+OH-(aq)=H2O(l) ��H1=-57.3kJ��mol-1����H2(g)+![]() O2(g)=H2O(g) ��H2=-241.8kJ��mol-1�������й�˵����ȷ���ǣ� ��
O2(g)=H2O(g) ��H2=-241.8kJ��mol-1�������й�˵����ȷ���ǣ� ��
A.��0.1molNaOH����Һ�м���һ�������0.1mol��L-1�Ҷ��ᣬ��Ӧ�е������仯��ͼ��ʾ
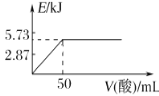
B.H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l) ��H=-114.6kJ��mol-1
C.������ȼ����Ϊ ��H=-241.8kJ��mol-1
D.������ȼ����Ϊ ��H=-483.6kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����0.5mol��L1CH3COONa��Һ��0.5mol��L1CuSO4��Һ�Լ�H2O��pH���¶ȱ仯��������ͼ��ʾ������˵������ȷ���ǣ� ��

A.���¶�Ϊ50��ʱ����ˮ��c(H+)=c(OH)
B.���¶����ߣ�CuSO4��Һ��c(H+)����
C.���¶����ߣ�CH3COONa��Һ��pH�仯��Kw�ı��й�
D.���¶����ߣ�CH3COONa��Һ��CuSO4��Һ��pH�����ͣ�����ΪCH3COO-��Cu2+ˮ��ƽ���ƶ�����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ��Ʊ��빤ҵ�����������
A.N2![]() NO
NO![]() HNO3
HNO3
B.ŨHCl![]() Cl2
Cl2![]() Ư��
Ư��
C.MgCl2(aq)![]() ��ˮMgCl2
��ˮMgCl2![]() Mg
Mg
D.����NaCl(aq)![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com