
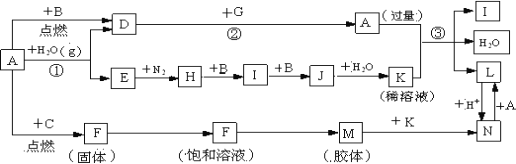
【题目】下图是中学化学常见物质的转化关系(某些反应条件及部分产物已略去),A、G为日常生活中的常见金属。B、C、E、I、J为气体,其中C为黄绿色气体,M为红褐色胶体。
(1)已知A为第26号元素,请写出A元素在周期表中的位置__________。
(2)D与G反应的化学方程式____________________。实验室引发该反应的操作___________。
(3)反应③离子方程式__________________________。
(4)H→I的化学方程式_______________。
(5)现将一试管J气体倒立于水槽中一段时间后,水面上升但不充满;若使水充满整个试管,应向试管中通入一定量__________(填气体的化学式),此时试管中溶液的浓度为________mol/L(气体体积按标准状况计算)(保留两位有效数字)。
【答案】 第四周期 第VIII族 8Al+ 3Fe3O4![]() 4Al2O3 + 9Fe 在铝热剂表面放一层氯酸钾,插一根镁条,点燃镁条 3Fe + 8H+ + 2NO3— = 3Fe2+ + 2NO↑+ 4H2O
4Al2O3 + 9Fe 在铝热剂表面放一层氯酸钾,插一根镁条,点燃镁条 3Fe + 8H+ + 2NO3— = 3Fe2+ + 2NO↑+ 4H2O ![]() O2 0.045
O2 0.045
【解析】A为26号元素,则A为Fe;C为黄绿色气体,则C为Cl2;M为红褐色胶体,则M为Fe(OH)3;A(Fe)与C(Cl2)点燃得到F,则F为FeCl3;A(Fe)与H2O(g)反应生成D和E,A(Fe)与气体B反应也得到D,则D为Fe3O4,E为H2,B为O2;E(H2)+N2→H,则H为NH3;H+B→I,I+B→J,J+H2O→K,则J为NO2;I为NO;K为HNO3;过量的A(Fe)和K(HNO3)反应生成硝酸亚铁、NO、水,则L为Fe(NO3)2;N+A(Fe)→L,则N为Fe(NO3)3;D+G→A,即Fe3O4+G→Fe,又G为常见金属,则G为Al。
(1)A为Fe,原子序数是26,在周期表中的位置为:第四周期 第ⅤⅢ族;
(2)“D+G→A”即“Fe3O4+Al→Fe”,反应的化学方程式:8Al+3Fe3O4![]() 4Al2O3+9Fe;该反应为铝热反应,实验室中引发铝热反应的操作方法是:在铝热剂表面放一层氯酸钾,插一根镁条,点燃镁条。
4Al2O3+9Fe;该反应为铝热反应,实验室中引发铝热反应的操作方法是:在铝热剂表面放一层氯酸钾,插一根镁条,点燃镁条。
(3)反应③为过量的Fe与稀硝酸反应,离子方程式:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O;
(4)“H→I”为NH3与O2反应生成NO和H2O,反应方程式为4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
(5)将一试管气体J(NO2)倒立于水槽中,若使水充满整个试管,则应向试管中通入一定量氧气,发生反应:4NO2+O2+2H2O=4HNO3。设原试管中NO2体积为VL,n(HNO3)=n(NO2)= ![]() ;c(HNO3)=
;c(HNO3)= ![]() =
= ![]() =0.045mol/L。故答案为:O2;0.045mol/L。
=0.045mol/L。故答案为:O2;0.045mol/L。


科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素最外层电子数与原子序数的关系图. 
请回答下列问题:
(1)画出Z的原子结构示意图 .
(2)原子半径:YZ(填“>”、“<”).
(3)Y的最高价氧化物的水化物与氢氧化钠溶液反应的化学方程式为 .
(4)X的最高价氧化物的水化物的化学式为 .
(5)画出W的氢化物的电子式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示的装置中,观察到电流计指针偏转,M棒变粗,N棒变细,并测得电解质溶液的质量减小,由此判断下表中所列M、N、P物质,其中可以成立的是( )

M | N | P | |
A | Zn | Cu | 稀硫酸溶液 |
B | Cu | Fe | 稀盐酸 |
C | Ag | Zn | 硝酸银溶液 |
D | Zn | Fe | 硫酸亚铁溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是金属镁和卤素单质(X2)反应的能量变化示意图.下列说法正确的是( ) 
A.由MgCl2制取Mg是放热过程
B.热稳定性:MgI2>MgBr2>MgCl2>MgF2
C.常温下氧化性:F2<Cl2<Br2<I2
D.由图可知此温度下MgBr2(s)与Cl2(g)反应的热化学方程式为:MgBr2(s)+Cl2(g)═MgCl2(s)+Br2(g),△H=﹣117kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为二氧化锰的有关转化关系图,有关说法中不正确的是()

A. 反应①—⑥均属于氧化还原反应
B. 反应②中Cl2既是氧化剂又是还原剂
C. 反应①中氧化剂与还原剂的物质的量之比为1∶4
D. 相同条件下生成等量的O2,反应③和④转移的电子数之比为1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于胶体的叙述中不正确的是( )
A.丁达尔现象可用来区别胶体与溶液
B.胶体能透过半透膜
C.胶体的性质主要有:丁达尔现象、电泳、聚沉
D.溶液、胶体、浊液的根本区别是分散质微粒直径的大小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,2﹣二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验中可以用图9所示装置制备1,2﹣二溴乙烷.其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有浓溴(表面覆盖少量水).请填写下列空白:
(1)烧瓶a要求温度迅速升高到170℃发生反应,写出该反应的化学方程式;该反应类型为 .
(2)写出制备1,2﹣二溴乙烷的化学方程式 .
(3)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请写出发生堵塞时瓶b中的现象 .
(4)容器c中NaOH溶液的作用是;e装置内NaOH溶液的作用是 .
(5)某学生做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超出许多,如果装置的气密性没有问题,试分析其可能的原因(至少2点) . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,某反应达到平衡,平衡常数K= ![]() .恒容时,温度升高,H2浓度减小.下列说法正确的是( )
.恒容时,温度升高,H2浓度减小.下列说法正确的是( )
A.升高温度,逆反应速率减小
B.该反应的焓变为正值
C.恒温恒容下,增大压强,H2浓度一定减小
D.该反应的化学方程式为CO+H2O ![]() CO2+H2
CO2+H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com