
【题目】利用氟磷灰石[(Ca5(PO4)3F)]生产磷铵[(NH4)3PO4]并制取硫酸、联产水泥。其工艺流程如下图所示:
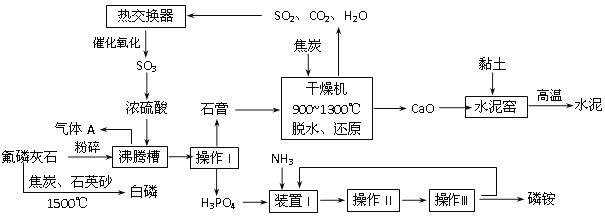
(1)操作I的名称________________;在实验室中操作II包括___________、____________。
(2)沸腾槽的材质是_______________(从“玻璃”、“钢铁”、“附有聚偏氟乙烯防腐层的石墨”中选择),选择的理由是__________________________________________________
(3)工业上还可以用氟磷灰石与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,同时逸出SiF4和CO,反应方程式为:_________________________________________。
(4)黏土中有一种成分为石脂(Al2[OH]4Si2O5·nH2O),其用氧化物表示为____________。
(5)已知SO2的催化氧化反应为2SO2(g)十O2(g) ![]() 2SO3(g) △H<0。
2SO3(g) △H<0。
从化学反应原理的角度说明催化氧化时使用热交换器的原因__________________。
(6)制硫酸所产生的尾气除了含有N2、O2外,还含有SO2、微量的SO3和酸雾。拟用下图所示的装置测定硫酸尾气中SO2的含量:

若下列各组中的试剂,前者浓度为0.1mol·L-1,后者适量,溶液体积为5mL;通入尾气10L(已换算为标准状况)时反应管中的溶液恰好变色。判断下列试剂组能否测定硫酸尾气中SO2的体积分数。能者,确定SO2的体积分数;不能者,说明原因。
编号 | 试剂组 | 结论 |
① | NaOH溶液、酚酞试液 | |
② | Na2CO3溶液、酚酞试液 | |
③ | 碘水、淀粉溶液 | |
④ | KMnO4溶液、稀硫酸 |
【答案】(1)过滤;蒸发浓缩、冷却结晶
(2)附有聚偏氟乙烯防腐层的石墨;因为酸性且加热,钢铁易被溶解,反应产生HF,HF能腐蚀玻璃
(3)4Ca5(PO4)3F+21SiO2+30C ![]() 20CaSiO3+3P4+SiF4↑+30CO↑
20CaSiO3+3P4+SiF4↑+30CO↑
(4)Al2O3·2SiO2·(n+2)H2O
(5)移去反应中放出的热量,使反应后的气体降温并预热未反应的气体
(6) ①不能,因为SO2和CO2均可以与NaOH溶液反应,且产物Na2SO3、NaCO3的溶液仍然为碱性,不能确定反应终点②不能,因为SO2可以与Na2CO3溶液反应生成Na2SO3,反应后溶液仍然为碱性,不能确定反应终点③0.112%④0.28%
【解析】
试题分析:(1)操作Ⅰ得到的是H3PO4液体和石青固体,所以是过滤;在实验室中操作II的目的是从溶液中得到晶体,包括蒸发浓缩、冷却结晶,故答案为:过滤;蒸发浓缩、冷却结晶;
(2)因为沸腾槽中的反应是在酸性且加热的条件下进行的,此条件下钢铁易被酸溶解,反应产生了HF,HF能腐蚀玻璃。聚偏氟乙烯防腐层不用热硫酸和HF反应,故沸腾槽应选用附有聚偏氟乙烯防腐层的石墨材质,故答案为:附有聚偏氟乙烯防腐层的石墨;因为酸性且加热,钢铁易被溶解,反应产生HF,HF能腐蚀玻璃;
(3)工业上还可以用氮磷灰石与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,同时逸出SiF4和CO,可以先写出:Ca5 (PO4) 3F+SiO2+C ![]() CaSiO3+P4+SiF4↑+CO↑,再配平,故答案为:4Ca5(PO4)3F+21SiO2+30C
CaSiO3+P4+SiF4↑+CO↑,再配平,故答案为:4Ca5(PO4)3F+21SiO2+30C ![]() 20CaSiO3+3P4+SiF4↑+30CO↑;
20CaSiO3+3P4+SiF4↑+30CO↑;
(4)石脂(Al2[OH]4Si2O5·nH2O),它可以用氧化物表示为Al2O3·2SiO2·(n+2)H2O,故答案为:Al2O3·2SiO2·(n+2)H2O;
(5)催化氧化时使用热交换器的原因是移去反应中放出的热量,使反应后的气体降温,有利于平衡正向移动,并预热未反应的气体,从而加快初始反应速率,故答案为:移去反应中放出的热量,使反应后的气体降温并预热未反应的气体;
(6)①不能,因为SO2和CO2均可以与NaOH溶液反应,且产物Na2SO3, Na2CO3的溶液仍然为碱性,不能确定反应终点;
②不能,因为SO2可以与Na2CO3溶液反应生成Na2SO3,反应后溶液仍然为碱性,不能确定反应终点;
③用淀粉作指示剂,可以证明I2反应完全:I2+SO2+2H2O=H2SO4+2HI,n(SO2)=n(I2) =0. 1mo1/L×5×10-3L=0. 5×10-3mol, V (SO2)=0. 5×10-3mo1×22. 4 L/mol=1. 12×10-2L,故尾气中SO2的体积分数是0.112%,故答案为:0.112%;
④高锰酸钾溶液本身的紫色可以作终点指示,故可以用来测定硫酸尾气中SO2的体积分数。由于5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4,按反应关系可以得到尾气中SO2的体积分数是0.28%,故答案为:0.28%。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知氨气可以与灼热的氧化铜反应得到氮气和金属铜,用下图中的装置可以实现该反应。

请回答下列问题:
(1)A中加入的物质是________,发生反应的化学方程式是______________________。
(2)B中加入的物质是________,其作用是_________________________________。
(3)实验时在C中观察到的现象是__________________________________,
发生反应的化学方程式是_________________________________________。
(4)实验时在D中观察到的现象是________________________________________,
D中收集到的物质是________,检验该物质的方法和现象是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)请正确表示下列化学用语:
乙炔(结构式) ;甲烷(空间构型) ;羟基(电子式) ;
C22-(电子式) _________ ;1,3-丁二烯(实验式) 。
(2)高分子化合物![]() 是由三种单体通过加聚反应而制得的。这三种单体的结构简式是 、 、 ;
是由三种单体通过加聚反应而制得的。这三种单体的结构简式是 、 、 ;
(3)提纯下列物质(括号内为杂质)
①NaCl(KNO3)固体中提取NaCl固体: 。
②KNO3(NaCl)溶液中得KNO3固体: 。
③乙醇(水)混合物中得无水乙醇: 。
④溴苯(溴)混合物中得溴苯: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组为了制取、收集纯净干燥的氯气并探究氯气的性质,他们设计了如图所示的实验装置:

请回答下列问题:
(1)整套实验装置的连接顺序是f接( )( )接( )( )接( )(填各接口处的字母代号)。
(2)E装置中制取氯气的离子方程式是 。
(3)A装置中试剂X是 。
(4)C装置中的现象是 产生此现象的原因是 (用离子方程式和必要的文字解释)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下面的反应线路及所给信息填空。

(1)A的结构简式是 ,B的结构简式是 ;
(2)①的反应类型是 ;②的反应类型是 ;
(3)反应④的条件是 ;
(4)写出反应④的化学方程式________________ ___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是一种重要的化工产品,是氮肥工业、有机合成工业以及制造硝酸、按盐和纯碱等的原料。
(1)以氨为燃料,氧气为氧化剂可以设计制造氨燃料电池,因产物无污染,在很多领域得到广泛应用。若电极材料均为惰性电极,KOH 溶液作电解质溶液,则该电池负极电极反应式为_______________;正极反应式为______________。
(2)下列措施可以加快合成氨反应速率的是______________。
A.通过缩小容器的容积增大压强 B.及时将氨液化分离出去
C.适当升温 D.添加合适的催化剂
E.恒温恒容时,再充入一定体积的氮气
(3)某化学研究性学习小组模拟工业合成氨的反应。在容积固定为2L的密闭容器内充入lmolN2 和3molH2,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下:
反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
压强/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
则①从反应开始到25min时,以N2表示的平均反应速率为________;
②H2的平衡转化率为_______________;
(4)以CO2与NH3为原料合成尿素[化学式为CO(NH2)2]的主要反应如下,已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s);△H=-159.47kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g);△H=+116kJ·mol-1
③ H2O(l)=H2O(g);△H=+44kJ·mol-1
写出CO2 与NH3 合成尿素和液态水的热化学反应方程式_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源问题是人类社会面临的重大课题,甲醇是未来重要的绿色能源之一。
(1)利用工业废气CO2可制取甲醇,己知常温常压下下列反应的能量关系如图:

则CO2与H2反应生成液态CH3OH 的热化学方程式为_______________________。
(2)CH4 和H2O(g)通过下列转化也可以制得CH3OH:
I.CH4(g)+H2O(g)![]() CO(g)+3H2(g); △H1>0
CO(g)+3H2(g); △H1>0
II.CO(g)+2H2(g)![]() CH3OH(g); △H2<0
CH3OH(g); △H2<0
将1.0molCH4 和3.0molH2O (g)通入反应室(容积为100L)中,在一定条件下发生反应I,CH4的转化率与温度、压强的关系如下图所示。

① 图中的P1___P2(填“<”、“>”或“=”) ,判断的理由是________________。
② 若反应II在恒容密闭容器进行,下列能判断反应II达到平衡状态的是______(填序号)。
A.生成CH3OH 的速率与消耗CO 的速率相等 B.混合气体的密度不变
C.混合气体的总物质的量不变 D.CH3OH、CO、H2的浓度都不再发生变化
③在某温度下,将一定量的CO和H2投入10L的密闭容器中发生反应II,5min时达到平衡,各物质的物质的浓度(mol· L-1)变化如下表所示:
2min | 5min | 10min | |
CO | 0.07 | 0.06 | 0.05 |
H2 | 0.14 | 0.12 | 0.20 |
CH3OH | 0.03 | 0.04 | 0.05 |
若5min时只改变了某一条件,则所改变的条件是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有前四周期六种元素X、Y、Z、E、F、G,它们的原子序数依次增大,除G外,其他五种元素都是短周期元素。X、Y、E三种元素组成的化合物是实验室常用燃料,也是一种家庭常见饮品的主要成分。取F的化合物做焰色反应实验,其焰色呈黄色,G的单质是生活中常见的一种金属,GE是黑色固体。G2E是红色固体。请回答下列问题:
(1)写出基态G原子电子排布式: ;Y、Z、E、F、G的第一电离能由小到大的顺序为 (用元素符号表示)。
(2)X、Y、Z形成3原子分子M,每个原子价层电子均达到稳定结构。M分子的结构式为 。1molM含![]() 键数目为 。
键数目为 。

(3)根据价层电子对互斥理论(VESPR)推测:ZE2—的立体构型为 ,YE32—的中心原子杂化类型为 。
(4)Y、E、Z分别与X形成的简单化合物沸点由高到底的顺序为 (用化学式表示) 。
(5)G晶胞结构如图所示。已知立方体的棱长为apm,G 晶体密度为bg·cm-3,则阿伏加德罗常数NA= (用含a、b的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的结构可用“键线式”简化表示。CH3-CH=CH-CH3可简写为![]() 。有机物X的键线式为
。有机物X的键线式为
(1)有机物Y是X的同分异构体,且属于芳香烃, Y在一定条件能发生聚合反应,写出其化学方程式____________________________________________ 。
(2)X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有___________ 种。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com