
元素X的原子最外层电子数是其内层的3倍。元素Y基态原子的3p轨道上有4个电子。元素Z位于第四周期,IIB族。
(1)Y与X可形成YX2
①YX2分子是 (填“极性”或“非极性”)分子。
②写出与YX2互为等电子体的分子的化学式: 。
③Y的一种单质,能溶于CS2,熔点112.8℃,沸点444.6℃。则其晶体类型为 。
(2)在X的氢化物(H2X)分子中,X原子轨道的杂化类型是 。
 (3)Z与Y所形成化合物晶体的晶胞如右图所示。
(3)Z与Y所形成化合物晶体的晶胞如右图所示。
①在1个晶胞中,Z离子的数目为 。
②该化合物的化学式为 。
③1个Y周围距离最近且相等的Z有 个。
科目:高中化学 来源: 题型:
食品安全是社会关注的热点。市场上已检测出一些矿泉水中含有高浓度的致癌物“溴酸盐”,而这个“行业秘密”在人们的眼皮底下被隐藏了10多年。实验室中制备“溴酸盐”过程如下:

根据上述转化关系回答下列问题:
(1)反应①的化学方程式为______________________________。
(2)已知反应②是复分解反应,该反应的化学方程式为
___________________________________________。
(3)已知在酸性条件下溴酸盐可发生如下离子反应:
Ⅰ.2BrO +10Cl-+12H+===5Cl2↑+Br2+6H2O
+10Cl-+12H+===5Cl2↑+Br2+6H2O
Ⅱ.6BrO +5Cl-+6H+===5ClO
+5Cl-+6H+===5ClO +3Br2+3H2O
+3Br2+3H2O
Ⅲ.BrO +5Br-+6H+===3Br2+3H2O
+5Br-+6H+===3Br2+3H2O
①上述反应所涉及的粒子中,氧化性最强的是________。
②在KCl和KBr的酸性混合溶液中,加入过量的KBrO3,其氧化产物为________,还原产物为________。
③将12 mL 0.4 mol·L-1 KBrO3溶液和10 mL 0.6 mol·L-1 KCl溶液在稀H2SO4中混合,充分反应后,产物KClO3和Cl2的物质的量之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,充分燃烧一定量的丁烷放出热量161.9 kJ,经测定完全吸收生成的CO2需消耗5 mol·L-1的KOH溶液100 mL,恰好生成正盐,则此条件下热化学方程式:
C4H10(g)+13/2O2(g)===4CO2(g)+5H2O(g)的ΔH为
A.+2 590.4 kJ·mol-1 B.-2 590.4 kJ·mol-1
C.+1 295.2 kJ·mol-1 D.-1 295.2 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质性质的应用正确的是
A.液氨汽化时要放出大量的热,可用作制冷剂
B.二氧化硫可广泛用于食品的漂白
C.生石灰能与水反应,可用来干燥氯气
D.氧化铝是一种电解质,可用于制铝
查看答案和解析>>
科目:高中化学 来源: 题型:
已知次氯酸能跟乙烯发生加成反应:CH2=CH2+HClO→CH2(OH)CH2Cl。又2R-CHO+O2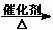 2R-COOH。以乙烯为原料制取聚氯乙烯(PVC)等产品的转化关系如图所示。
2R-COOH。以乙烯为原料制取聚氯乙烯(PVC)等产品的转化关系如图所示。
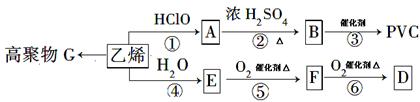
试回答下列问题:
(1)写出有机物B和G的结构简式:B____________,G_________;
(2)⑥的反应类型是________________;
(3)写出D的一种同分异构体的结构简式_______________________;
(4)写出反应⑤的化学方程式__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述合理的是( )
A.用干燥的pH试纸检测碳酸钠溶液、氯水、稀醋酸的pH
B.铜与浓硫酸反应时,可用蘸有浓溴水的棉花放在导管口检验逸出的气体
C.需用某浓度的NaOH溶液450 mL,则配制时应选用450 mL的容量瓶
D.将液溴 、浓硝酸保存在棕色试剂瓶中,放置于冷暗处
查看答案和解析>>
科目:高中化学 来源: 题型:
近年来,高锰酸钾在饮用水和工业污水处理领域的消费需求增长较快。实验室可用二氧化锰为主要原料制备高锰酸钾。其部分流程如下:
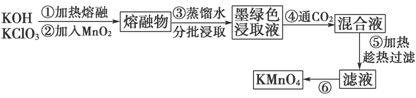
(1)第①步中采用铁坩埚而不用瓷坩埚的原因是(用化学方程式表示)_______________________________________________________________。
(2) KOH、KClO3和MnO2共熔反应生成墨绿色K2MnO4的化学方程式为________________________________________________________________。
(3)第④步通入CO2,可以使MnO 发生反应,生成MnO
发生反应,生成MnO 和MnO2。则K2MnO4完全反应时,转化为KMnO4的百分率约为____________________(精确到0.1%)。
和MnO2。则K2MnO4完全反应时,转化为KMnO4的百分率约为____________________(精确到0.1%)。
(4)第⑤步趁热过滤的目的是________________________________。
(5)第⑥步加热浓缩至液面有细小晶体析出时,停止加热,冷却结晶、___________、洗涤、干燥。干燥过程中,温度不宜过高,因为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某学习小组设计用如图装置验证二氧化硫的化学性质。

(1)能说明二氧化硫具有氧化性的实验现象为_________________________。
(2)为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验。
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀
上述方案中合理的是________(填“Ⅰ”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为____________________________________________。
(3)当通入二氧化硫至试管c中溶液显中性时,该溶液中c(Na+)=________(用含硫微粒浓度的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列的排序不正确的是( )
A.晶体熔点由低到高:CF4 < CCl4 < CBr4 < CI4 B.沸点由高到低:Na>Mg>Al
C.硬度由大到小:金刚石 > SiC >晶体硅 D.晶格能由大到小: MgF2> NaCl > NaBr
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com