
【题目】能正确表达下列反应的离子方程式为( )
A.用醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O
B.硫化亚铁与浓硫酸混合加热:2H++FeS=H2S↑+ Fe2+
C.向硫酸铝溶液中滴加碳酸钠溶液:2Al3++3 ![]() =Al2(CO3)3↓
=Al2(CO3)3↓
D.用氢氧化钠溶液吸收工业废气中的NO2:2NO2+2OH= ![]() +
+ ![]() + H2O
+ H2O
【答案】D
【解析】解:A.碳酸钙和醋酸都需要保留化学式,正确的离子方程式为CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO﹣ , 故A错误;B.硫化亚铁与浓硫酸混合加热,离子方程式为2FeS+20H++7SO42﹣=2Fe3++9SO2↑+10H2O,故B错误;
C.铝离子水解显酸性,碳酸根离子水解显碱性,混合后水解相互促进生成氢氧化铝和二氧化碳,反应的离子方程式为2Al3++3CO32﹣+3H2O=2Al(OH)3↓+3CO2↑,故C错误;
D.用氢氧化钠溶液吸收工业废气中的NO2 , +4价的氮发生歧化反应,生成硝酸钠、亚硝酸钠,离子方程式为2NO2+2OH﹣=NO3﹣+NO2﹣+H2O,故D正确;
故选D.


科目:高中化学 来源: 题型:
【题目】有机物A的相对分子质量184.5,其结构如图1所示,(﹣R﹣代表某种烷基),A在一定条件下还有如图2所示的反应关系,D不能发生银镜反应.
(1)C中含有的官能团为 , E→F的反应类型为;
(2)写出A的结构简式;
(3)写出C→E的化学方程式;
(4)H的同分异构体很多,其中属于酯类,含苯环,且水解产物中含有乙酸的同分异构体有种
(5)G显酸性,M(B),M(G)分别表示B、G的相对分子质量,试求:M(G)﹣M(B)= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,密闭容器中X,Y,Z三种气体的起始浓度和平衡浓度如表,下列说法错误的是( )
物质 | X | Y | Z |
初始浓度/molL﹣1 | 0.1 | 0.2 | 0 |
平衡浓度/molL﹣1 | 0.05 | 0.05 | 0.1 |
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y2Z,平衡常数为1600
C.其他条件不变时,增大压强可使平衡常数增大
D.改变温度可以改变该反应的平衡常数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于物质分类的正确组合是
碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
A | Na2CO3 | H2SO4 | Na2SO4 | SiO2 | CO2 |
B | NaOH | HCl | NaCl | Na2O | CO2 |
C | NaHCO3 | CH3COOH | MgCl2 | CuO | SO2 |
D | KOH | HNO3 | CaCO3 | CaO | CO |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中药在世界医学界越来越受到关注.中药药剂砒霜(主要成分As2O3)可用于治疗急性白血病,为此,砷及其化合物的提取再次引起关注.
(1)As的原子结构示意图为 ![]() ,则其在周期表中的位置是 .
,则其在周期表中的位置是 .
(2)N元素非金属性比As强,下列说法正确的是 . ①NH3的热稳定性比AsH3差
②HNO3的酸性比H3AsO4强
③N的原子半径比As的原子半径小
(3)根据如图写出As2O5分解为As2O3的热化学方程式 . 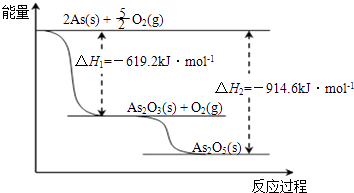
(4)查文献得知,可以从硫化砷(As2S3)废渣中提取As2O3 , 提取的工艺流程简图如下: 
①As2S3、Na3AsS3中的S均为﹣2价,碱浸过程中发生的反应(填“是”或“不是”)氧化还原反应.
②过程Ⅲ的系列操作包括 .
③写出过程Ⅲ的离子方程式 ,
过程Ⅲ中,酸性越强,As2O3的产率越高,请解释其原因 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒定温度为T1℃时,在容积为10L的密闭容器中充人1.0mol X和0.80mol Y,发生反应:
2X(g)+Y(g)2Z(g),X的转化率随时间的变化关系如图所示.
(1)第2min时的反应速率v1(X)(填“大于”、“小于”或“等于”)第8min时的反应速率可v2(X),原因是 .
(2)反应在0~10min内Y的平均反应速率v(Y)=molL﹣1min﹣l .
(3)T1℃温度下反应的平衡常数K1为 , 若在第10min后压缩容器容积,X的转化率(填“增大”、“减小”或“不变”,下同),平衡常数 .
(4)若升高温度到T2℃( T2>T1),平衡时X的转化率减小,则该反应的△H0(填“大于”或“小于”).
(5)不改变各物质起始量的情况下,无论如何改变条件,Y的转化率一定小于 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、F是家庭中常见的有机物,A可以用来除去暖瓶或水壶中的水垢;E是石油化工发展水平的标志,F是一种常见的高分子材料。根据下面转化关系回答下列问题:
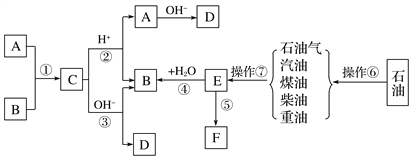
(1)操作⑥、操作⑦的名称分别为________________、________________。
(2)E的结构简式为_________。
(3)B的官能团名称为________,对B的描述正确的是________。
①有毒 ②无色无味 ③密度比水小 ④与酸性高锰酸钾溶液反应使其褪色
⑤在海带提碘实验中作萃取剂从碘水中提取碘单质
⑥在热Cu丝作用下生成相对分子质量比它小2的有机物
A.①③⑤ B.②③④ C.③④⑥ D.④⑤⑥
(4)写出下列反应的化学方程式:
①写出不含18O的A与用18O标记的B在一定条件下发生反应的化学方程式(注明条件和18O的位置):
_______________________________________________________________________,
④E和水反应生成B的方程式(注明条件):
_______________________________________________________________________,
⑤作为家庭中常见的物质,高分子化合物F给我们带来了极大的方便,同时也造成了环境污染,反应⑤的方程式为:___________________________________________________________,
写出有机物B遇到红热的铜丝在空气中反应的化学方程式:
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用软锰矿(主要含MnO2,还含有少了SiO2、Al2O3 、Fe2O3等杂质)模拟工业制高锰酸钾流程如下。试回答下列问题。

(1)配平焙烧时MnO2参与的化学反应:□MnO2+□_____+□O2 ![]() □K2MnO4+□H2O;第二次通入过量CO2时发生反应的离子方程式为:______________________。
□K2MnO4+□H2O;第二次通入过量CO2时发生反应的离子方程式为:______________________。
(2)滤渣I、II的成分中能与NaOH 反应的是__________________ (填化学式)。产生滤渣II时不能用稀盐酸代替CO2,因为______________________。
(3)将滤液Ⅲ进行一系列操作可得到KMnO4晶体。由下图可知,从滤液Ⅲ得到KMnO4需经过____、____洗涤等操作。

(4)用重结晶提纯的产品配制成0.10mol·L-1 的酸性KMnO4溶液来测定某草酸样品的纯度(杂质不参与反应,草酸为弱酸,分子式H2C2O4)。
①试给出反应的离子方程式:_______________________。
②若某测定大致共需要230毫升酸性KMnO4溶液,配制时所需玻璃仪器为:___、___烧杯、胶头滴管等。
③取草酸样品5 克,配成100mL溶液,取20mL于适当容器中,用前述所配酸性KMnO4溶液滴定,至反应结束消耗KMnO4溶液20mL,则样品的纯度为: ___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com