
| A. | c(Z)=0.4 mol/L | B. | c(X2)=0.2mol/L | ||
| C. | c(Y2)=0.4mol/L | D. | c(X2)+c(Y2)+c(Z)=0.6mol/L |
分析 可逆反应的特点:反应不能进行到底.可逆反应无论进行多长时间,反应物不可能100%地全部转化为生成物;全部转到一边,求算各物质浓度的取值范围,依此得出正确结论.
解答 解:Z全部转化时,X2的物质的量浓度为:0.1+$\frac{0.2}{2}$=0.2 mol•L-1,Y2的物质的量浓度为:0.3+$\frac{0.2}{2}$=0.4mol•L-1,故c(X2)的取值范围为:0<c(X2)<0.2 mol•L-1;
当X2全部转化时,Z的物质的量浓度为:0.2+0.1×2=0.4mol•L-1,Y2的物质的量浓度为:0.3-0.1=0.2mol•L-1,故c(Y2)的取值范围为:0.2mol•L-1<c(Y2)<0.4 mol•L-1,c(Z)的取值范围为:0<c(Z)<0.4 mol•L-1;
A.c(Z)的取值范围为:0<c(X2)<0.4 mol•L-1,故A错误;
B.c(X2)的取值范围为:0<c(X2)<0.2 mol•L-1,故B错误;
C.c(Y2)的取值范围为:0.2mol•L-1<c(Y2)<0.4 mol•L-1,故C错误;
D.因为反应前后系数相等,所以总物质的量不变,则c(X2)+c(Y2)+c(Z)=0.1mol/L+0.3mol/L+0.2mol/L=0.6mol/L,故D正确,
故选D.
点评 本题考查可逆反应的特点,难度不大.要注意对于可逆反应,反应物不可能100%地全部转化为生成物.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a>7时,水溶液一定不是中性 | B. | a>7时,水的电离受到抑制 | ||
| C. | a<7时,溶液的pH一定为a | D. | a>7时,溶液的pH一定为14-a |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将过量的Na投入到AlCl3溶液中 | B. | 将过量的Al投入到NaOH溶液中 | ||
| C. | 将过量的Na投入到MgCl2溶液中 | D. | 将过量的Na2O2投入到FeCl2溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
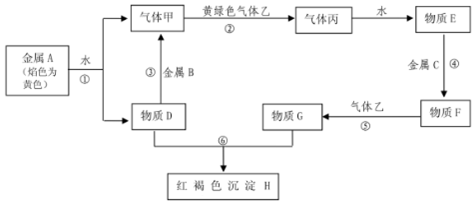
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com