
| A、vA=0.15mol/(L?min) |
| B、vB=0.6 mol/(L?min) |
| C、vC=0.4 mol/(L?min) |
| D、vD=0.005 mol/(L?s) |
| vA |
| 1 |
| vB |
| 4 |
| vC |
| 1 |
| vD |
| 1 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
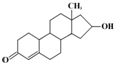 “诺龙”属于国际奥委会明确规定的违禁药品中合成代谢类的类固醇,其结构简式如图下列关于“诺龙”的说法中不正确的是( )
“诺龙”属于国际奥委会明确规定的违禁药品中合成代谢类的类固醇,其结构简式如图下列关于“诺龙”的说法中不正确的是( )| A、分子式是C18H26O2 |
| B、能在NaOH醇溶液中发生消去反应 |
| C、既能发生加成反应,也能发生酯化反应 |
| D、既能发生氧化反应,也能发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、该反应的化学平衡常数表达式是K=
| ||
| B、此时,B的平衡转化率是35% | ||
| C、增大该体系的压强,平衡向右移动,化学平衡常数增大 | ||
| D、增加C,B的平衡转化率不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al3+ Na+NO3- Cl- |
| B、K+ Na+Cl- NO3- |
| C、K+ Na+ Cl-AlO2- |
| D、K+ NH4+ SO42-NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠块沉在乙醇液面的下面 |
| B、反应较为和缓 |
| C、钠块在乙醇的液面上游动 |
| D、钠块表面有气体放出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
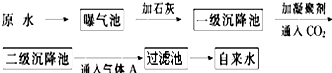
| pH | Ca2+、Mg2+总浓度 | 细菌总数 |
| 6.5~8.5 | <0.0045mol?L-1? | <100个?mL-1? |
查看答案和解析>>
科目:高中化学 来源: 题型:
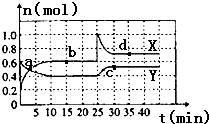 已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入容积为2L的恒温密闭容器中,各组分物质的量随时间变化关系如图所示.
已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入容积为2L的恒温密闭容器中,各组分物质的量随时间变化关系如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com