
A、该反应的化学平衡常数表达式是K=
| ||
| B、此时,B的平衡转化率是35% | ||
| C、增大该体系的压强,平衡向右移动,化学平衡常数增大 | ||
| D、增加C,B的平衡转化率不变 |
| 4 |
| 5 |
| 4 |
| 5 |
| c2(D) |
| c3(A)?c2(B) |
| 0.8mol |
| 2mol |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、②③④⑥ |
| C、②③④⑤ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
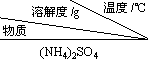 | 10 | 20 | 30 | 40 | 50 | 70 |
| (NH4)2SO4 | 73.3 | 75.4 | 78.0 | 81.0 | 84.5 | 91.9 |
| FeSO4?7H2O | 40.0 | 48.0 | 60.0 | 73.3 | - | - |
| (NH4)2SO4?FeSO4?6H2O | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 | 38.5 |
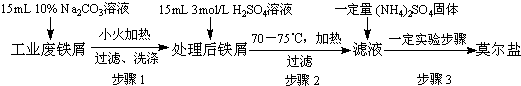

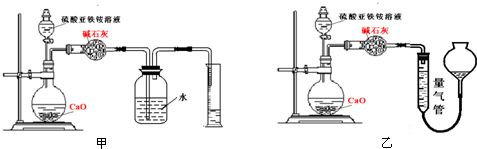
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol/LCH3COOH溶液中:c(CH3COO-)+c(CH3COOH)=0.1mol/L |
| B、CH3COONa溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| C、Na2S溶液中:2 c(Na+)=c(S2-)+c(HS-)+c(H2S) |
| D、NaHCO3溶液中:c(OH-)=c(H+)+c(H2CO3)-c(CO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、vA=0.15mol/(L?min) |
| B、vB=0.6 mol/(L?min) |
| C、vC=0.4 mol/(L?min) |
| D、vD=0.005 mol/(L?s) |
查看答案和解析>>
科目:高中化学 来源: 题型:
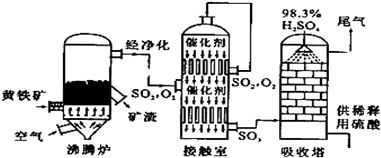
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com