
【题目】Cu2O是一种在涂料、玻璃等领域应用非常广泛的红色氧化物。它不溶于水和醇,溶于盐酸、氯化铵、氨水,易被O2、 硝酸等氧化。一种以硫化铜矿石(含CuFeS2、Cu2S 等) 为原料制取Cu2O 的工艺流程如下:
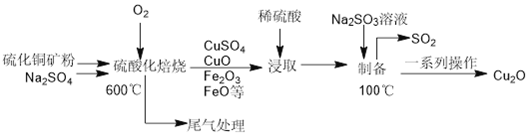
(1) “硫酸化焙烧”时:CuS 与O2反应生成CuSO4等物质的化学方程式为________________;在100℃时,发生反应的离子方程式为________________________________。
(2)加入Na2SO4的作用除减小物料间黏结外,另一主要作用是_____________________。
(3) “浸取”时为提高铜的浸取率,除需控制液固物质的量之比外,还需控制________________ (至少列举两点)。
(4)得到产品Cu2O的一系列操作主要是___________________________________。
(5)下列有关说法正确的是______________
A.焙烧时得到的尾气可用碱液加以处理
B.Cu2O露置至于空气中会变黑
C.经一系列操作得到产品Cu2O后的副产品,经处理后可作净水剂
D.“制备”时,溶液的pH越小,Cu2O 的产率越高
【答案】 2Cu2S+5O2![]() 2CuSO4+2CuO 2Cu2++3SO32-
2CuSO4+2CuO 2Cu2++3SO32-![]() Cu2O↓+SO42-+2SO2↑ 提高焙烧产物中CuSO4比例 浸取温度、浸取时间、硫酸的浓度等(答出两点即可) 抽滤、洗涤、干燥 ABC
Cu2O↓+SO42-+2SO2↑ 提高焙烧产物中CuSO4比例 浸取温度、浸取时间、硫酸的浓度等(答出两点即可) 抽滤、洗涤、干燥 ABC
【解析】(1)CuS与O2反应生成CuSO4和氧化铜,反应的化学方程式为:2Cu2S+5O2![]() 2CuSO4+2CuO;100℃时,发生反应的离子方程式为2Cu2++3SO32-
2CuSO4+2CuO;100℃时,发生反应的离子方程式为2Cu2++3SO32-![]() Cu2O↓+SO42-+2SO2↑。
Cu2O↓+SO42-+2SO2↑。
(2)加入Na2SO4的作用除减小物料间黏结外,另一主要作用是:提高焙烧产物中CuSO4比例。
(3)“浸取”时为提高铜的浸取率,除需控制液固物质的量之比外,还需控制浸取温度、浸取时间、硫酸的浓度等。
(4)A.焙烧时得到的尾气为SO2可用碱液加以处理,故A正确;B.Cu2O露置至于空气中会氧化为黑色CuO,故B正确;C.经一系列操作得到产品Cu2O后的副产品硫酸铁,水解产生Fe(OH)3可用作净水剂,故C正确;D.Cu2O在酸溶液中会发生自身氧化还原反应生成Cu和Cu2+,故D错误;本题选ABC。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】常温下,浓度均为0.1mol/L的4种钠盐溶液pH如下:
溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
pH | 11.6 | 9.7 | 10.3 | 5.2 |
下列说法不正确的是
A. 四种溶液中,Na2CO3溶液中水的电离程度最大
B. NaHSO3溶液显酸性的原因是:电离程度大于水解程度
C. 常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最小的是H2SO3
D. 向氯水中加入少量Na2CO3(s),可以增大氯水中次氯酸的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁可以和CO2发生反应:Fe(s)+CO2(g)![]() FeO(s)+CO(g)。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示.下列说法中正确的是
FeO(s)+CO(g)。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示.下列说法中正确的是

A. a点为平衡状态
B. b点和c点的化学平衡常数K相同
C. 该反应的化学平衡常数表示为K =[CO]·[FeO]/[CO2]·[Fe]
D. 若温度升高,该反应的化学平衡常数K增大,则该反应的 ΔH < 0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用固体硫酸亚铁制取颜料铁红(Fe2O3)反应原理是:2FeSO4![]() Fe2O3+SO2↑+SO3↑,某学生欲检验该反应所产生的气态物质,依次将气体通过盛有A、B、C三个装置。
Fe2O3+SO2↑+SO3↑,某学生欲检验该反应所产生的气态物质,依次将气体通过盛有A、B、C三个装置。

(1)B中盛放的溶液可以是_________________。
(2)A中放冰的作用是_______________________。
(3)设计一个简单的实验方案探究A中得到的沉淀的成分。___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究不溶性盐X(仅含5种元素)的组成和性质,设计并完成如下实验(所加试剂均过量,气体体积均在标准状况下测定)。

请回答:
(1)X的组成元素为H、O和______(用元素符号表示),气体C的电子式为_______。
(2)写出反应①的离子方程式:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是:
A. 将铜丝插入稀硝酸中:Cu+4H++2NO![]() ===Cu2++2NO2↑+H2O
===Cu2++2NO2↑+H2O
B. 向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe===2Fe2+
C. 向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3·H2O===Al(OH)3↓+3NH![]()
D. 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+===H2SiO3↓+2Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4mol A气体和2molB气体置于2L密闭容器中,混合后发生如下反应:2A(g)+B(g)2C(g)+ D(s),若经2s后测得C的浓度为0.6molL-1,下列说法正确的是( )
A. 用物质A表示的反应速率为0.6mol(Ls)-1 B. 2s时物质B的含量为23.3%
C. 2s时物质A的转化率为30% D. 2s时物质B的浓度为0.3molL-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲乙两个烧杯中各盛有200mL 3mol/L的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积之比为1:2,则加入的铝粉的质量为( )
A. 2.7g B. 3.6g C. 5.4g D. 10.8g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com