
【题目】甲乙两个烧杯中各盛有200mL 3mol/L的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积之比为1:2,则加入的铝粉的质量为( )
A. 2.7g B. 3.6g C. 5.4g D. 10.8g
【答案】D
【解析】
根据铝的质量相同,盐酸和氢氧化钠溶液中溶质的物质的量相同,反应结束后测得生成的气体体积比为甲:乙=1:2,由Al+6HCl═2AlCl3+3H2↑、 2Al+2NaOH+2H2O═2NaAlO2+3H2↑可知,酸与金属反应时酸不过量,碱与金属反应时碱过量来计算解答。
盐酸和氢氧化钠溶液中溶质的物质的量均为0.2L×3mol/L=0.6mol,又两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙=1:2,设铝与酸反应时酸完全反应,生成的氢气的物质的量为x,
则 2Al+6HCl═2AlCl3+3H2↑
6 3
0.6mol x
![]() =
=![]() ,解得x=0.3mol,
,解得x=0.3mol,
一定条件下,气体的物质的量之比等于体积之比,则碱与金属铝反应生成的氢气的物质的量为0.3mol×2=0.6mol,碱与金属铝反应时铝完全反应,设与碱反应的铝的物质的量为y,
则2Al+2NaOH+2H2O═2NaAlO2+3H2↑
2 3
y 0.6mol
![]() =
=![]() ,解得y=0.4mol,则铝的质量为0.4mol×27g/mol=10.8g,故选D。
,解得y=0.4mol,则铝的质量为0.4mol×27g/mol=10.8g,故选D。


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:
【题目】Cu2O是一种在涂料、玻璃等领域应用非常广泛的红色氧化物。它不溶于水和醇,溶于盐酸、氯化铵、氨水,易被O2、 硝酸等氧化。一种以硫化铜矿石(含CuFeS2、Cu2S 等) 为原料制取Cu2O 的工艺流程如下:
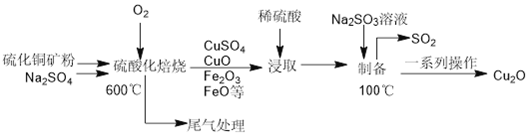
(1) “硫酸化焙烧”时:CuS 与O2反应生成CuSO4等物质的化学方程式为________________;在100℃时,发生反应的离子方程式为________________________________。
(2)加入Na2SO4的作用除减小物料间黏结外,另一主要作用是_____________________。
(3) “浸取”时为提高铜的浸取率,除需控制液固物质的量之比外,还需控制________________ (至少列举两点)。
(4)得到产品Cu2O的一系列操作主要是___________________________________。
(5)下列有关说法正确的是______________
A.焙烧时得到的尾气可用碱液加以处理
B.Cu2O露置至于空气中会变黑
C.经一系列操作得到产品Cu2O后的副产品,经处理后可作净水剂
D.“制备”时,溶液的pH越小,Cu2O 的产率越高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。回答下列问题:
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为_____、_____(填标号)。
A.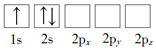 B.
B.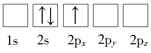
C.![]() D.
D.![]()
(2)Li+与H具有相同的电子构型,r(Li+)小于r(H),原因是______。
(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是______、中心原子的杂化形式为______。LiAlH4中,存在_____(填标号)。
A.离子键 B.σ键 C.π键 D.氢键
(4)Li2O是离子晶体,其晶格能可通过图(a)的BornHaber循环计算得到。
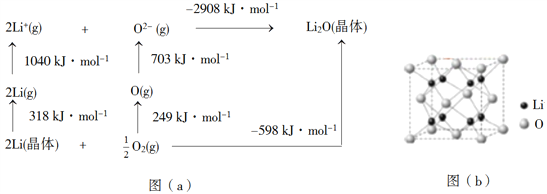
可知,Li原子的第一电离能为________kJ·mol1,O=O键键能为______kJ·mol1,Li2O晶格能为______kJ·mol1。
(5)Li2O具有反萤石结构,晶胞如图(b)所示。已知晶胞参数为0.4665 nm,阿伏加德罗常数的值为NA,则Li2O的密度为______g·cm3(列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源、环境与生产生活和社会发展密切相关。
(1)一定温度下,在两个容积均为2L的密闭容器中,分别发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1。相关数据如下:
CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1。相关数据如下:
容器 | 甲 | 乙 |
反应物投入量 | 1molCO2(g)和3molH2(g) | 1molCH3OH(g)和1molH2O(g) |
平衡时c(CH3OH) | c1 | c2 |
平衡时能量变化 | 放出29.4kJ | 吸收akJ |
①下列情况能说明该反应一定达到平衡状态的是_________(填字母)。
a.v(CO2)消耗=v(CH3OH)生成 b.气体的密度不再随时间改变
c.CO2和CH3OH的浓度之比不再随时间改变 d.气体的平均相对分子质量不再随时间改变
②其他条件不变,达到平衡后,下列不能提高H2转化率的操作是_________(填字母)。
a.降低温度 b.充入更多的H2 c.移除甲醇 d.增大容器体积
③cl_________c2(填“>”、“<”或“=”),a=_________。
④该温度下反应的平衡常数K=_________;若甲中反应10s时达到平衡,则0~10s内甲中的平均反应速率v(H2)=_________。
(2)已知反应:2NO2(红棕色)![]() N2O4(无色)△H<0。将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是__________(填字母)。
N2O4(无色)△H<0。将一定量的NO2充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是__________(填字母)。
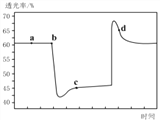
A.b点的操作是压缩注射器
B.d点:v正>v逆
C.c点与a点相比,c(NO2)增大,c(N2O4)减小
D.若不忽略体系温度变化,且没有能量损失,则Tb>Tc
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将w1 g样品加热,其质量变为w2 g,则该样品中Na2CO3的纯度(质量分数)是
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为五个椭圆交叉构成的图案,椭圆内分别写了C2H5OH、CO2、Fe2O3、FeCl3和NaOH五种物质,图中相连的两种物质均可归为一类,相交的部分A、B、C、D为其相应的分类标准代号。请回答下列问题:
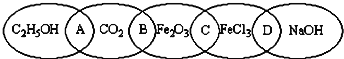
(1)两种物质混合能发生反应且都是电解质的是________(填分类标准代号,下同),两种物质都是氧化物的是________。
(2)分类标准代号A表示______________(多项选择)
a.两物质都是非电解质 b.两物质都是有机物
c.两物质都是含碳化合物 d.两物质都是氧化物
(3)上述五种物质中的某一物质能与某种强酸反应生成上述物质中的另一种物质,该反应的离子方程式为:__________________________________。
(4)用洁净的烧杯取25 mL蒸馏水,加热至沸腾,向烧杯中逐滴加入上述五种物质中的某一物质的饱和溶液,加热得红褐色胶体,该反应的化学方程式为: ____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示的一些物质或概念间的从属关系中不正确的是( )
![]()
A. X为含氧酸、Y为酸、Z为化合物
B. X为氧化物、Y为化合物、Z为纯净物
C. X为强碱、Y为碱、Z为化合物
D. X为非金属氧化物、Y为酸性氧化物、Z为氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 分子中一定存在化学键
B. 分子中若含有化学键,则一定存在σ键
C. p和p轨道不能形成σ键
D. 含π键的物质不如只含σ键的物质稳定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com