
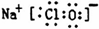 .
.分析 (1)次氯酸钠是离子化合物,氧原子和氯原子共用1对共用电子对;
(2)A.F、Cl、Br、I的电负性依次减弱,电负性越大,酸性越弱;
B.原子半径越大,共价键键长越大,键能越小;
C.四种物质都是分子晶体,根据氢键和分子间作用力的大小判断;
D.元素的非金属性越强,对应氢化物的还原性越弱.
(3)常温下,0.1mol/L的NaClO溶液的pH=9.7,溶液显碱性,次氯酸钠溶液中次氯酸根离子水解显碱性,Kh=$\frac{c(O{H}^{-})•c(HClO)}{c(Cl{O}^{-})}$=$\frac{c(O{H}^{-})•c(HClO)}{c(Cl{O}^{-})}$×$\frac{c({H}^{+})}{c({H}^{+})}$=$\frac{{K}_{w}}{{k}_{a}}$,洁厕液与84消毒液混合后会生成有毒的氯气,是洁厕净中盐酸和84消毒液中氯离子、次氯酸根离子发生氧化还原反应生成氯气;
(4)①在碱性条件下,利用NaClO氧化硝酸铁,制得Na2FeO4,结合电荷守恒和原子守恒配平书写离子方程式;
②选择的洗涤剂应能抑制K2FeO4的水解,并注意减少K2FeO4的溶解.
解答 解:(1)次氯酸钠是离子化合物,氧原子和氯原子共用1对共用电子对,电子式为: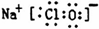 ,故答案为:
,故答案为: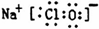 ;
;
(2)A.F、Cl、Br、I的电负性依次减弱,电负性越大,酸性越弱,故其氢化物的酸性依次增强,故A错误;
B.原子半径越大,共价键键长越大,键能越小,原子半径:F<Cl<Br<I,则共价键的键长:H-F<H-C1<H-Br<H-I,键能:H-F>H-Cl>H-Br>H-I,故B正确;C.四种物质都是分子晶体,组成和结构相似,分子的相对分子质量越大,分子间作用力越大,则其熔沸点越高,但是HF中氢键熔点反常,比卤素的其他氢化物熔点高,所以熔点由低到高:HCl<HBr<HI<HF,故C错误;
D.元素的非金属性越强,对应氢化物的还原性越弱,因为非金属性:F>Cl>Br>I,故还原性:HF<HCl<HBr<HI,故D正确,
故选:AC;
(3)常温下,0.1mol/L的NaClO溶液的pH=9.7,溶液显碱性,次氯酸钠溶液中次氯酸根离子水解显碱性,反应的离子方程式为:ClO-+H2O?HClO+OH-,
常温下,0.1mol/L的NaClO溶液的pH=9.7,ClO-+H2O?HClO+OH-,Kh=$\frac{c(O{H}^{-})•c(HClO)}{c(Cl{O}^{-})}$=$\frac{c(O{H}^{-})•c(HClO)}{c(Cl{O}^{-})}$×$\frac{c({H}^{+})}{c({H}^{+})}$=$\frac{{K}_{w}}{{k}_{a}}$,则Ka=$\frac{1{0}^{-14}×0.1}{1{0}^{-4.3}×1{0}^{-4.3}}$=10-6.4,
次氯酸钠有强氧化性,盐酸有强还原性,两者发生氧化还原反应生成氯气,方程式为:NaClO+2HCl═NaCl+Cl2↑+H2O,离子方程式为:ClO-+Cl-+2H+=Cl2↑+H2O,
故答案为:次氯酸根离子水解溶液显碱性,ClO-+H2O?HClO+OH-;10-6.4;ClO-+Cl-+2H+=Cl2↑+H2O;
(4)①在碱性条件下,利用NaClO氧化硝酸铁,制得Na2FeO4,该反应的离子反应方程式为2Fe3++3ClO-+10OH-=2FeO42-+5H2O+3Cl-,
故答案为:2Fe3++3ClO-+10OH-=2FeO42-+5H2O+3Cl-;
②为抑制K2FeO4的水解,应在碱性条件下洗涤,可用CH3COONa,为防止K2FeO4的溶解,可用异丙醇洗涤,故答案为:d.
点评 本题综合考查氯的化合物的性质以及卤素的性质比较,题目较为综合,难度较大,注意把握题给信息,尤其是化学平衡常数的运用.


科目:高中化学 来源: 题型:选择题
| A. | BaCl2 NaOH NaHCO3 | B. | AlCl3 NH3•H2O NaOH | ||
| C. | Ba(OH)2 CaCl2 Na2SO4 | D. | Na2CO3 MgCl2 H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、SO32-、Cl-、NO3- | B. | H+、NH4-、Al3+、SO42- | ||
| C. | Na+、S2-、OH-、SO42- | D. | Na+、Ca2+、CH3COO-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
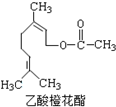 某食用香料乙酸橙花酯的结构简式如图所示,关于该有机物的下列叙述中正确的是( )
某食用香料乙酸橙花酯的结构简式如图所示,关于该有机物的下列叙述中正确的是( )| A. | ①②③ | B. | ①②④ | C. | ①②⑤ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠的水解反应:CO32-+H2O?HCO3-+OH- | |
| B. | 粗铜精炼时,与电源正极相连的是粗铜,电极反应式为:Cu-2e-═Cu2+ | |
| C. | 钢铁发生电化学腐蚀的负极反应式:Fe-2e-═Fe2+ | |
| D. | 碱性氢氧燃料电池负极反应式:O2+2H2O+4e-═4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
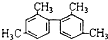 的烃,下列说法正确的是( )
的烃,下列说法正确的是( )| A. | 分子中至少有9个碳原子处于同一平面上 | |
| B. | 分子中至少有11个碳原子处于同一平面上 | |
| C. | 该有机物不能使酸性KMnO4溶液褪色 | |
| D. | 该烃属于苯的同系物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com