
【题目】在碱性条件下使用鸟粪石[Mgx(NH4)y(PO4)z·nH2O]处理氨氮废水具有加热时间短,氨逸出彻底等优点。反应原理如下:
yNa++yOH-+Mgx(NH4)y(PO4)z·nH2O![]() Mgx(Na)y(PO4)z+yNH3↑+(n+y)H2O
Mgx(Na)y(PO4)z+yNH3↑+(n+y)H2O
Mgx(Na)y(PO4)z+y![]() +nH2O
+nH2O![]() yNa++Mgx(NH4)y(PO4)z·nH2O↓
yNa++Mgx(NH4)y(PO4)z·nH2O↓
(1)上述氨氮废水处理过程中鸟粪石所起的作用是__________。
(2)其它条件不变,若鸟粪石化学式中的z保持不变,x越大,处理相同量的氨氮废水所需的时间就_________(填:“越长”“越短”“不变”)。
(3)为测定鸟粪石的组成,进行下列实验:
①取鸟粪石2.45 g与足量的NaOH溶液混合,加热,收集到标准状况下的气体224mL
②另取鸟粪石2.45 g溶于稍过量盐酸,用蒸馏水配成100.00 mL溶液A;
③取25.00 mL溶液A,调节pH=10,用浓度为0.1000 mol·L-1的EDTA标准溶液滴定Mg2+,滴定至终点,消耗EDTA标准溶液25 mL(已知Mg2+与EDTA反应的化学计量比1∶1);
④取25.00 mL溶液A,加入0.005mol的BiCl3,调节溶液pH生成Mg3(PO4)2和BiPO4沉淀,过滤,滤液中的Bi3+用EDTA标准溶液滴定为![]() mol。通过计算确定鸟粪石的化学式_____________(写出计算过程)。
mol。通过计算确定鸟粪石的化学式_____________(写出计算过程)。
【答案】催化剂 越长 n(![]() )=n(NH3)=
)=n(NH3)=![]() =0.01mol
=0.01mol
n(Mg2+)=n(EDTA)×![]() =0.1000 mol·L-1×25.00 mL×10-3×
=0.1000 mol·L-1×25.00 mL×10-3×![]() =0.01mol
=0.01mol
n(![]() )=0.01mol×
)=0.01mol×![]() +(0.005mol-
+(0.005mol-![]() mol)×4=0.01mol
mol)×4=0.01mol
n(H2O)=![]() =0.06mol
=0.06mol
n(![]() ):n(Mg2+):n(
):n(Mg2+):n(![]() ):n(H2O)=0.01mol:0.01mol:0.01mol:0.06mol=1:1:1:6
):n(H2O)=0.01mol:0.01mol:0.01mol:0.06mol=1:1:1:6
故鸟粪石的化学式为MgNH4PO4·6H2O
【解析】
根据所给方程式判断鸟粪石在反应中的作用;根据定量分析中所给出的数据计算各粒子的物质的量,随后根据各粒子的物质的量的比确定鸟粪石的化学式。
(1)将上述两个方程式相加得![]() +OH-=NH3↑+H2O,说明第一个反应消耗多少鸟粪石第二个反应就生成多少鸟粪石,故鸟粪石在处理氨氮废水的过程中起到催化剂的作用;
+OH-=NH3↑+H2O,说明第一个反应消耗多少鸟粪石第二个反应就生成多少鸟粪石,故鸟粪石在处理氨氮废水的过程中起到催化剂的作用;
(2)根据鸟粪石化学式[Mgx(NH4)y(PO4)z·nH2O],当z保持不变,x越大时,鸟粪石中铵根含量降低,可以处理的氨氮废物的量减小,处理相同量的氨氮废水所需的时间就越长;
(3)n(![]() )=n(NH3)=
)=n(NH3)=![]() =0.01mol
=0.01mol
n(Mg2+)=n(EDTA)×![]() =0.1000 mol·L-1×25.00 mL×10-3×
=0.1000 mol·L-1×25.00 mL×10-3×![]() =0.01mol
=0.01mol
n(![]() )=0.01mol×
)=0.01mol×![]() +(0.005mol-
+(0.005mol-![]() mol)×4=0.01mol
mol)×4=0.01mol
n(H2O)=![]() =0.06mol
=0.06mol
n(![]() ):nspan>(Mg2+):n(
):nspan>(Mg2+):n(![]() ):n(H2O)=0.01mol:0.01mol:0.01mol:0.06mol=1:1:1:6
):n(H2O)=0.01mol:0.01mol:0.01mol:0.06mol=1:1:1:6
故鸟粪石的化学式为MgNH4PO4·6H2O。


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案科目:高中化学 来源: 题型:
【题目】在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙(粒子直径在1~100nm之间)。如图所示A~E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题。
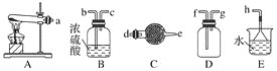
(1)实验室制取、收集干燥的NH3,需选用上述仪器装置的接口连接顺序是(选填字母):a接__、___接__,__接h;实验室用A装置制取NH3的化学方程式为___。
(2)向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入的气体是___,试写出制纳米级碳酸钙的化学方程式:___。
(3)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】广东河源市东源县某村土壤的主要成份是Al2O3、Fe3O4及SiO2,广州大学附属东江中学“探险号”化学兴趣小组设计以下流程提取金属铝:
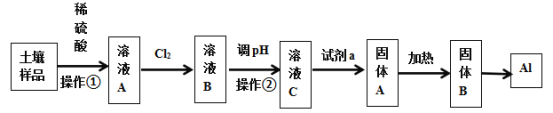
信息提示:氧化铝在电解条件下可得金属铝;Fe(OH)3、Al(OH)3、Fe(OH)2开始沉淀与完全沉淀的pH数据表:
Fe(OH)3 | Al(OH)3 | Fe(OH)2 | |
开始沉淀的pH | 2.7 | 3.3 | 5.9 |
完全沉淀的pH | 3.2 | 5.2 | 8.4 |
(1)溶液A含有的金属阳离子为_________________固体B的化学式为_______________________
(2)步骤中通入氯气时的离子方程式为___________________________________________________
(3)溶液C的pH范围是_____________________,操作②的名称是_________________________
(4)通入试剂a的离子方程式为_________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如右,电解总反应为:2Cu+H2O![]() Cu2O+H2↑。下列说法正确的是
Cu2O+H2↑。下列说法正确的是
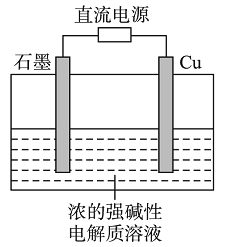
A. 石墨电极上产生氢气
B. 铜电极发生还原反应
C. 铜电极接直流电源的负极
D. 当有0.1 mol电子转移时,有0.1 mol Cu2O生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,Ka1 (H2SO3)=1.5×10-2,Ka2=1.0×10-7,Kb (NH3·H2O) =1.76×10-5,设H2SO3溶液中c(总)=c(![]() )+c(
)+c(![]() )+c(H2SO3)。室温下将氨气通入25.00 mL 0.1000 mol·L1H2SO3溶液中(忽略溶液体积变化),下列说法正确的是
)+c(H2SO3)。室温下将氨气通入25.00 mL 0.1000 mol·L1H2SO3溶液中(忽略溶液体积变化),下列说法正确的是
A.溶液中始终存在:c(![]() )+c(H+ )=c(
)+c(H+ )=c(![]() )+c(
)+c(![]() )+c(OH)
)+c(OH)
B.在NH4HSO3溶液中:c(![]() )>c(
)>c(![]() )>c(NH3·H2O)>c(H2SO3)
)>c(NH3·H2O)>c(H2SO3)
C.pH=7的溶液:c(![]() )=2c(
)=2c(![]() )+c(
)+c(![]() )
)
D.c(![]() )=2c(总)的溶液中:c(NH3·H2O)+c(OH)=c(H+ )+c(
)=2c(总)的溶液中:c(NH3·H2O)+c(OH)=c(H+ )+c(![]() )+2c(H2SO3)
)+2c(H2SO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】每次取20 g海水,严格按照过滤、蒸发、冷却、称量、计算的实验步骤规范操作,连续实验三次,平均得固态盐a g。该海水中含氯化钠的质量分数是( )
A.大于5a%
B.小于5a%
C.等于5a%
D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t℃时,A的溶解度是Sg·100g-1,其饱和溶液密度为dg·cm-3、物质的量浓度为cmol·L-1。溶液的质量分数为w,A的摩尔质量为Mg·mol-1,实验测得向一定量含A的溶液中加入mg无水A或蒸发掉ng水后恢复到t℃,均为饱和溶液,下列关系式正确的是( )
A.S=![]()
B.c=![]()
C.S=![]()
D.c%=![]() 100%
100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】.在一定温度下的恒容容器中,当下列物理量不再发生变化时,不能表明反应: A(s)+3B(g)![]() 2C(g)+D(g)已达平衡状态的是
2C(g)+D(g)已达平衡状态的是
A. 混合气体的压强B. 混合气体的密度
C. 3v逆(C)=2v正(B)D. 气体的平均相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:浓硫酸易使有机物脱水,如图是用实验室制得的乙烯(C2H5OH![]() CH2=CH2↑+H2O)与溴水作用制取1,2-二溴乙烷的部分装置图,根据图示判断下列说法正确的是
CH2=CH2↑+H2O)与溴水作用制取1,2-二溴乙烷的部分装置图,根据图示判断下列说法正确的是

A. 装置①和装置③中都盛有水,其作用相同
B. 装置②和装置④中都盛有NaOH溶液,其吸收的杂质相同
C. 产物可用分液的方法进行分离,1,2-二溴乙烷应从分液漏斗的上口倒出
D. 制备乙烯时温度计水银球位置应在反应液的液面下
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com