
塑化剂DBP(邻苯二甲酸二丁酯)主要应用于PVC等合成材料中作软化剂。
合成反应原理为:
实验步骤如下:
步骤1:在三口烧瓶中放入14.8g邻苯二甲酸酐、25mL正丁醇、4滴浓硫酸,开动搅拌器(反应装置如图)。
步骤2:缓缓加热至邻苯二甲酸酐固体消失,升温至沸腾。
步骤3:等酯化到一定程度时,升温至150℃
步骤4:冷却,倒入分漏斗中,用饱和食盐水和5%碳酸钠洗涤。
步骤5:减压蒸馏,收集200~210℃2666Pa馏分,即得DBP产品
(1)搅拌器的作用 。
(2)图中仪器a名称及作用是 ;步骤3中确定有大量酯生成的依据是 。
(3)用饱和食盐水代替水洗涤的好处是 。
(4)碳酸钠溶液洗涤的目的是 。
(5)用减压蒸馏的目的是 。
(1)使反应物充分接触
(2)分水器,及时分出反应生成的水,有利于反应向生成DBP方向移动;分水器中有大量的水产生。
(3)可避免酯的损失,同时避免洗涤过程中的乳化现象
(4)中和产品中游离酸
(5)避免蒸馏过程中有机物脱水碳化现象
解析试题分析:(1)搅拌可以使反应物充分混合反应;(2)酯化反应有水生成,移出产物有利于平衡正向进行;生成水越多生成酯的量也就越多;(3)有机物在盐溶液中的溶解度小,减少酯的溶解损失;(4)碳酸钠能反应掉酯中溶解的杂质酸,同时溶解除去乙醇;(5)减压蒸馏可以降低有机物的沸点,使其在较低的温度下分离出来,避免温度过高出现有机物脱水碳化现象。
考点:考查化学实验中仪器的识别、实验原理分析、实验方案评价等有关问题。


科目:高中化学 来源: 题型:问答题
(10分)(1)下列四种烃分别在氧气中完全燃烧:(填字母序号)
①若烃的物质的量相等,则消耗氧气最多的是 ;
②若烃的质量相等,则消耗氧气最多的是 ;
③若反应前后(150℃)气体的物质的量不发生变化,则该烃可能是 。
A.C2H6 B.C2H4 C.C4H10 D.C5H10
(2)下列各组化合物中,不论二者以什么比例混合,完全燃烧时:
①若总质量不变,耗O2量不变的是 ;生成水的质量不变的是 。
②若总的物质的量不变,则耗O2量不变的是 ;生成CO2的质量不变的是 。
A. C2H4、C3H6 B. HCHO、CH3COOH
C. CH4、CH3COOH D. CH2==CH2、CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某实验小组用燃烧分析法测定某有机物中碳和氢等元素的含量,随后又对其进行了性质探究。将已称量的样品置于氧气流中,用氧化铜作催化剂,在高温条件下样品全部被氧化为水和二氧化碳,然后分别测定生成的水和二氧化碳。实验可能用到的装置如下图所示,其中A装置可以重复使用。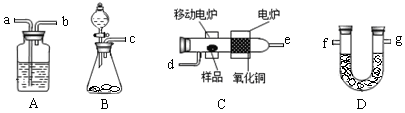
请回答下列问题:
(1)请按气体流向连接实验装置 → → →d→ → → → g(用仪器接口编号填写)。
(2)B装置中制O2时所用的药品是 。实验中,开始对C装置加热之前,要通一段时间的氧气,目的是 ;停止加热后,也要再通一段时间的氧气,目的是 。
(3)已知取2.3g的样品X进行上述实验,经测定A装置增重2.7g,D装置增重4.4g。试推算出X物质的实验式 。 (4)该小组同学进一步实验测得:2.3g的 X与过量金属钠反应可放出560mLH2(已换算成标准状况下),且已知X分子只含一个官能团。查阅资料后,学生们又进行了性质探究实验:
(4)该小组同学进一步实验测得:2.3g的 X与过量金属钠反应可放出560mLH2(已换算成标准状况下),且已知X分子只含一个官能团。查阅资料后,学生们又进行了性质探究实验:
实验一:X在一定条件下可催化氧化最终生成有机物Y.
实验二:X与Y在浓硫酸加热条件下生成有机物Z.
则①写出实验二中反应的化学方程式 。
②除去Z中混有的Y所需的试剂和主要仪器是 、 。
(5)若已知室温下2.3g液态X在氧气中完全燃烧生成二氧化碳气体和液态水时可放出68.35kJ的热量,写出X在氧气中燃烧的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某校化学课外兴趣小组的学生为了验证乙醇的分子结构,设计如下实验程序:乙醇组成元素的测定、分子式的测定、分子结构的测定。
(1)他们决定用燃烧乙醇分析产物来确定乙醇中含有C、H两种元素。简要说明他们的具体操作:①证明含有氢元素的操作是________________________________________________________ _
________________________________________________________________________________________;
②证明含有碳元素的操作是________________________________________________
_______________________________________________________________________
(2)要用燃烧分析产物证实乙醇中还含有氧元素时,需取得一些实验数据,这些数据应该是________________________。
(3)为确定乙醇的分子式,除(2)中数据外,还需不需要测定乙醇的相对分子质量?
_______________________________________________________________________
(4)为测定乙醇分子结构,他们用了无水乙醇和金属钠反应收集生成氢气的方法,选用了如下图所示的仪器(有的仪器配用双孔橡皮塞)。
①装置的连接顺序是______接______接______接______接_______接_______。
②已知无水酒精的密度为0.789 g·cm一3,移取2.0mL酒精,反应完全后(钠过量),收集390 mL气体。则乙醇分子中能被钠取代出的氢原子数为_______,由此可确定乙醇的结构为______________________而不是______________。
(5)实验所测定的结果偏高,可能引起的原因是(填写编号)。______________
A.本实验在室温下进行
B.无水酒精中混有微量甲醇
C.无水酒精与钠反应不够完全
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
已知:苯甲酸在水中的溶解度为:0.18g(4℃)、0.34g(25℃)、6.8g(95℃)。乙醚的沸点为34.6℃。实验室常用苯甲醛制备苯甲醇和苯甲酸,其原理为:2C6H5―CHO+NaOH C6H5―CH2OH+C6H5―COONa
C6H5―CH2OH+C6H5―COONa
实验步骤如下:
①向如图所示装置中加入适量 NaOH、水和苯甲醛,混匀、加热,使反应充分进行。
②从冷凝管下口加入冷水,混匀,冷却。倒入分液漏斗,用乙醚萃取、分液。水层保留待用。将乙醚层依次用10%碳酸钠溶液、水洗涤。
③将乙醚层倒入盛有少量无水硫酸镁的干燥锥形瓶中,混匀、静置后将其转入蒸馏装置,缓慢均匀加热除去乙醚,收集198℃~204℃馏分得苯甲醇。
④将步骤②中的水层和适量浓盐酸混合均匀,析出白色固体。冷却、抽滤得粗产品,将粗产品提纯得苯甲酸。
(1)步骤②中,最后用水洗涤的作用是 。将分液漏斗中两层液体分离开的实验操作方法是:先 后 。
(2)步骤③中无水硫酸镁的作用是 。
(3)步骤④中水层和浓盐酸混合后发生反应的化学方程式为 ;将反应后混合物冷却的目的是 。
(4)抽滤装置所包含的仪器除减压系统外,还有 、 (填仪器名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
三苯甲醇( )是一种重要的化工原料和医药中间体,实验室合成三苯甲醇的合成流程如图1所示。
)是一种重要的化工原料和医药中间体,实验室合成三苯甲醇的合成流程如图1所示。
已知:i)格氏试剂容易水解,
ii)相关物质的物理性质如下:
| 物质 | 熔点(℃) | 沸点(℃) | 溶解性 |
| 三苯甲醇 | 164.2 | 380 | 不溶于水,溶于乙醇、乙醚等有机溶剂 |
| 乙醚 | —116.3 | 34.6 | 微溶于水,溶于乙醇、苯等有机溶剂 |
| 溴苯 | —30.7 | 156.2 | 不溶于水,溶于乙醇、乙醚等多数有机溶剂 |
| 苯甲酸乙酯 | —34.6 | 212.6 | 不溶于水 |
| Mg(OH)Br | 常温下为固体 | 能溶于水,不溶于醇、醚等有机溶剂 | |


查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列关于有机化合物的性质说法正确的是
| A.棉花和蛋白质都是高分子化合物,水解产物相同 |
| B.苯和乙烯都能使溴水褪色,均与溴水发生加成反应 |
| C.乙酸乙酯和油脂互为同系物 |
| D.甲烷和乙醇均能发生取代反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com