
【题目】如图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是( )

A.气态氢化物的稳定性:R>W
B.X与Y可以形成原子个数比为1:1和1:2的两种离子化合物
C.Y和Z两者最高价氧化物对应的水化物能相互反应
D.由X、Y、Z、W、R五种元素形成的简单离子中半径最小的是X2-
【答案】D
【解析】
由表中化合价可知,X的化合价为-2价,没有正化合价,X为O元素,Y的化合价为+1价,处于ⅠA族,原子序数大于O元素,Z为Na元素,Z为+3价,为Al元素,W的化合价为+6、-2价,W为S元素,R的化合价为+7、-1价,R为Cl元素,则
A.非金属性越强,氢化物的稳定性越强,非金属性Cl>S,氢化物稳定性HCl>H2S,选项A正确;
B.X、Y分别为O、Na,可形成Na2O、Na2O2两种离子化合物,原子个数比为1:1和1:2,选项B正确;
C.Y和Z两者最高价氧化物对应的水化物分别为NaOH、Al(OH)3 ,两者能相互反应,选项C正确;
D.X、Y、Z、W、R五种元素形成的简单离子分别为O2-、Na+、Al3+、S2-、Cl-,半径最小的是Al3+(Z3+),选项D不正确;
答案选D。


科目:高中化学 来源: 题型:
【题目】下列装置能达到实验目的的是
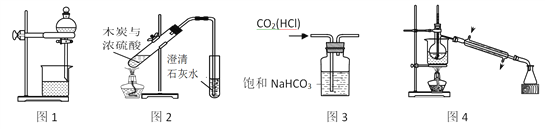
A. 图1用于分离酒精和水
B. 图2用于验证木炭与浓硫酸的反应产物中含有CO2
C. 图3用于除去CO2中的少量HCl
D. 图4用于制备蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气与氧气生成水的反应是氢能源应用的重要途径。下列有关说法正确的是
A.Al2O3(s)+AlCl3(g)+3C(s)=3AlCl(g)+3CO(g),常压下该反应在1900℃的高温下才能进行,说明该反应的ΔH<0
B.钢铁水闸可用牺牲阳极或外加电流的阴极保护法防止其腐蚀
C.将MgCl2·6H2O在坩埚中加热可获得MgCl2
D.反应2H2(g)+O2(g)![]() 2H2O(g)的ΔH可通过下式估算:ΔH=反应中形成新共价键的键能之和反应中断裂旧共价键的键能之和
2H2O(g)的ΔH可通过下式估算:ΔH=反应中形成新共价键的键能之和反应中断裂旧共价键的键能之和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2O、NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为________。
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为
NO+NO2+2OH![]() 2
2![]() +H2O
+H2O
2NO2+2OH![]()
![]() +
+![]() +H2O
+H2O
①下列措施能提高尾气中NO和NO2去除率的有________(填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是________(填化学式);吸收后排放的尾气中含量较高的氮氧化物是________(填化学式)。
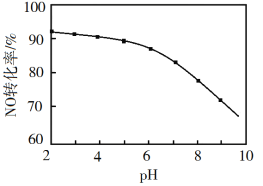
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为![]() 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
①在酸性NaClO溶液中,HClO氧化NO生成Cl和![]() ,其离子方程式为________。
,其离子方程式为________。
②NaClO溶液的初始pH越小,NO转化率越高。其原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合硫酸铁[Fe2(OH)6-2n(SO4)n]m广泛用于水的净化。以FeSO4·7H2O为原料,经溶解、氧化、水解聚合等步骤,可制备聚合硫酸铁。
(1)将一定量的FeSO4·7H2O溶于稀硫酸,在约70℃下边搅拌边缓慢加入一定量的H2O2溶液,继续反应一段时间,得到红棕色黏稠液体。该过程中反应温度不宜过高,原因是_______;H2O2氧化Fe2+的离子方程式为________。
(2)测定聚合硫酸铁样品中铁的质量分数:准确称取液态样品3.000g,置于250mL锥形瓶中,加入适量稀盐酸,加热,滴加稍过量的SnCl2溶液(Sn2+将Fe3+还原为Fe2+),充分反应后,除去过量的Sn2+。用5.000×102mol·L1K2Cr2O7溶液滴定至终点(滴定过程中![]() 与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00mL。
与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00mL。
①上述实验中若不除去过量的Sn2+,样品中铁的质量分数的测定结果将_______(填“偏大”或“偏小”或“无影响”)。
②计算该样品中铁的质量分数(写出计算过程)_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,将3molA和1molB两种气体混合于固定容积2L的密闭容器中,发生如下反应:3A(g)+B(g)xC(g)+2D(g)。经2min该反应达到平衡状态,生成0.8molD,测得C的浓度为0.8mol/L。则下列判断错误的是
A.x=4
B.2min内B的反应速率为0.1mol·L-1·min-1
C.B的转化率为40%
D.该温度下平衡常数的值为1.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中![]() 增大
增大
B.在0.1mol/LCH3COONa溶液中:n(OH﹣)+0.1mol>n(CH3COOH)+n(H+)+n(Na+)
C.在10mL0.1mol/L的AgNO3溶液中加入6mL等浓度的NaCl溶液,有白色沉淀产生,再加入6mL等浓度的Na2S溶液,溶液中又有黑色沉淀生成,说明Ksp(Ag2S)<Ksp(AgCl)
D.常温下,10mL0.02mol/LHCl溶液与10mL0.02mol/LBa(OH)2溶液充分混合,若混合后溶液的体积为20mL,则溶液的pH=12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用 0.1000mol/L NaOH溶液滴定 20.00mL0.1000mol/L某一元酸HA溶液,滴定曲线如图。下列说法正确的是
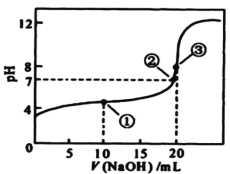
A.该滴定过程既能用甲基橙又能用酚酞作指示剂
B.点①所示溶液中:c(A-) >c(Na+)>c(H+) >c(OH-)
C.点②所示溶液中:c(Na+) =c(HA) +c(A-)
D.水的电离程度随着NaOH溶液的滴入不断增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究铜和浓硫酸的反应,下列装置或操作错误的是
甲 乙
乙  丙
丙
A.上下移动装置甲中的铜丝可控制SO2的生成
B.装置乙可用于收集SO2气体
C.为确认甲中有CuSO4生成,向甲中反应后的试管中直接加水稀释,观察溶液颜色
D.利用装置丙将硫酸铜溶液加热浓缩、冷却结晶,可析出CuSO4·5H2O晶体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com