
����Ŀ��PbO2��2PbCO3��Pb��OH��2����ʽ̼��Ǧ����������Ǧ������������ԭ�ϡ�
��1��PbO2����NaClO����Pb��NO3��2��Һ�õ���
��Pb��NO3��2������ΪPbO2�����ӷ���ʽΪ ��
��Pb��NO3��2��Һ��ͨ��H2S����Pb2+��aq��+H2S��aq��![]() PbS��s��+2H+��aq����ֱ��ƽ�⣬�÷�Ӧ��ƽ�ⳣ��ΪK= [��֪��Ksp��PbS��= 3.55��10��28��H2S���볣��Ka1=1.3��10��7��Ka2=7.1��10��15 ]��
PbS��s��+2H+��aq����ֱ��ƽ�⣬�÷�Ӧ��ƽ�ⳣ��ΪK= [��֪��Ksp��PbS��= 3.55��10��28��H2S���볣��Ka1=1.3��10��7��Ka2=7.1��10��15 ]��
��2���Ʊ���ʽ̼��Ǧ��ʵ�鲽�����£�

�١�̼����ʱ��������Ӧ�Ļ�ѧ����ʽΪ ��
�ڡ�ϴ�ӡ�ʱ����ˮϴ�Ӻ����þƾ�ϴ�ӵ�Ŀ���� ��
��3��Ϊȷ��2PbCO3��Pb��OH��2�����ʽ����775�����ȷֽ���̣���������ʵ�飺��ȡһ������2��ʵ���Ƶõ���Ʒ�������ط������У�����������ȷֽ⣬�����Ʒ�Ĺ����������������Ʒ��ʣ������/������Ʒ����ʼ������100%�����¶ȵı仯����ͼ��ʾ��
��A��B�����У�����ϵ���ݳ��ķֽ��������������Ϊ ���ѧʽ����C��D�����У�����ϵ���ݳ��ķֽ��������������Ϊ ���ѧʽ����
������ͼ��ʵ�����ݣ����㲢ȷ��E���������Ļ�ѧʽ��д�������������
���𰸡�
��1����Pb2++ClO��+H2O=PbO2��+Cl��+2H+��2.6��106
��2����31��CH3COO��2Pb��Pb��OH��2]+2CO2=3��CH3COO��2Pb+2PbCO3��Pb��OH��2��+2H2O
�ڳ�ȥ�������渽�ŵ�ˮ���ٽ�����ٸ���
��3����H2O��CO2
��1mol2PbCO3��Pb��OH��2������Ϊ775g��
![]() ��m1= 18g�����ٵ���H2O
��m1= 18g�����ٵ���H2O
![]() ��m2= 44g�����ٵ���CO2
��m2= 44g�����ٵ���CO2
![]() ��m3=44g�����ٵ���CO2
��m3=44g�����ٵ���CO2
2PbCO3��Pb��OH��2����ȥ1��H2O��2��CO2����E���������ΪPbO��
��������
�����������1����Pb��NO3��2������ΪPbO2�����ӷ���ʽΪPb2++ClO��+H2O = PbO2�� + Cl��+ 2H+���ʴ�Ϊ��Pb2++ClO��+H2O = PbO2�� + Cl��+ 2H+��
�ڸ���H2S���볣��Ka1=1.3��10��7��Ka2=7.1��10��15����Ka1=![]() �� Ka2=
�� Ka2=![]() �����Ka1��Ka2=
�����Ka1��Ka2=![]() ��
��![]() =
=![]() ������Ksp��PbS��= 3.55��10��28����c��Pb2+����c��S2-��= Ksp��PbS��= 3.55��10��28����Pb2+��aq�� + H2S��aq��
������Ksp��PbS��= 3.55��10��28����c��Pb2+����c��S2-��= Ksp��PbS��= 3.55��10��28����Pb2+��aq�� + H2S��aq��![]() PbS��s�� + 2H+��aq����ƽ�ⳣ��ΪK=
PbS��s�� + 2H+��aq����ƽ�ⳣ��ΪK=![]() =
=![]() =
=![]() =
=![]() =2.6��106���ʴ�Ϊ��2.6��106��
=2.6��106���ʴ�Ϊ��2.6��106��
��2���١�̼����ʱ��������Ӧ�Ļ�ѧ����ʽΪ31��CH3COO��2Pb��Pb��OH��2]+2CO2=3��CH3COO��2Pb + 2PbCO3��Pb��OH��2��+2H2O���ʴ�Ϊ��31��CH3COO��2Pb��Pb��OH��2]+2CO2=3��CH3COO��2Pb + 2PbCO3��Pb��OH��2��+2H2O��
�ڡ�ϴ�ӡ�ʱ����ˮϴ�Ӻ����þƾ�ϴ�ӿ��Գ�ȥ�������渽�ŵ�ˮ���ٽ�����ٸ���ʴ�Ϊ����ȥ�������渽�ŵ�ˮ���ٽ�����ٸ�����
��3��1mol2PbCO3��Pb��OH��2������Ϊ775g����A��B��B��D��D��E������ֱ�Ϊ��m1����m2����m3��
![]()
![]() m1= 18g�����ٵ���H2O��
m1= 18g�����ٵ���H2O��![]()
![]() m2= 44g�����ٵ���CO2��
m2= 44g�����ٵ���CO2��![]()
![]() m3=44g�����ٵ���CO2��
m3=44g�����ٵ���CO2��
2PbCO3��Pb��OH��2����ȥ1��H2O��2��CO2����E���������ΪPbO���ʴ�Ϊ����H2O��CO2����PbO��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������Ҫ������������Ʊ���
I��KAl(SO4)2��12H2O����������һ�ָ��Σ�����ֽ�ȷ���Ӧ�ù㷺��ʵ�����У����÷������ޣ���Ҫ�ɷ�ΪAl������������Fe��Mg���ʣ��Ʊ������Ĺ�������ͼ��ʾ��

�ش��������⣺
��1��Ϊ�����������ʣ��Լ���Ӧѡ��___________�����ţ���
a��HCl��Һ b��H2SO4��Һ c����ˮ d��NaOH��Һ
��2������B�Ļ�ѧʽΪ____________����������������ˮ����Һ�������ԣ���ԭ����______________��
II������������Ҫ�ɷ���Al2O3��������SiO2��Fe2O3����Ϊԭ���������ݶ�������Al2O3����������ͼ��ʾ��

��1��Al2O3�����ڵ����Al���䷴Ӧ�Ļ�ѧ����ʽ��______________________��
��2�����ط�Ӧ��������Ԫ��֮��һ��ʱ��Al2O3����NaOH��SiO2ת��Ϊ�������Ƴ�����Al2O3����NaOH�����ӷ���ʽ��_________________��
��3��������������������������X��
�� X ��Ϊ������CO2������ҺII����Ҫ��������____________��Ϊ��ʹ��ҺIIѭ�����ã�Ӧ�����������____________��ѡ����ĸ����
a��CaO b��HCl c��Na2CO3
�� X Ҳ��Ϊ����Al(OH)3���������ֿɼ��ٳ����������������ŵ���_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ܽ��ͷ�Ӧ����Ļ�ܵ��ǣ� ��
A. �����¶� B. ʹ�ô��� C. ����ѹǿ D. ����Ũ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ݡ��ο���Ϣ���������п�ѧ�����������21���͵���Դ����δ����ʯ�����Ĺ۵㡣
��1���������������ȼ�յ��Ȼ�ѧ����ʽΪSi(s)��O2(g)=SiO2(s) ��H����989.2 kJ��mol-1���йؼ����������±���
��ѧ�� | Si��O | O=O | Si��Si |
����(kJ/mol) | x | 498.8 | 176 |
��֪1 mol Si�к�2 mol Si��Si����1 mol SiO2�к�4 mol Si��O������x��ֵΪ____________��
��2���������Ϊһ���ձ�ʹ�õ�������Դ���������ã��������������ص�����˵���У�����Ϊ��������________________��
A����������䡢���棬�Ӱ�ȫ�Ƕȿ��ǣ�������ѵ�ȼ��
B�������Դ�ḻ�����ڿ��ɣ��ҿ�����
C����ȼ�շų�����������ȼ�ղ���Ի�����Ⱦ�̶ȵͣ�������Ч����
D��Ѱ�Ҹ�Ч�´�����ʹ����������ܺܵͣ��ǹ���Դ�������õĹؼ�����
��3����ҵ�Ʊ�����ķ�ӦΪ2H2(g)��SiCl4(g)=Si(s)��4HCl(g) ��H����240.4 kJ��mol-1��
���ɵ�HClͨ��100 mL 1 mol��L-1��NaOH��Һǡ�÷�Ӧ����Ӧ������__________(���������������ͷ���)������Ϊ________kJ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������ͭ����ᾧˮ�����IJⶨʵ���У�������Ϊ-2.7%��ԭ�������
A. ʵ��ʱ����δ��ȫ���� B. ���Ⱥ������ɫ���������
C. ���ȹ����о�����������ʧ D. ���Ⱥ����δ�������������ȴ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʵ��������ʵ��~ʵ����������ȷ���� �����������
����Һ����ʱ����Һ©�����²�Һ����¿ڷų����ϲ�Һ������ڵ���
������ڵ�NaOHϡ��Һ���μ�FeCl3������Һ�����Ʊ�Fe��OH��3����
��ʯ�͵ķ���ʵ���У��轫���ȼƵ�ˮ�������Һ�������Կ���Һ��
���ô������ۻ������ƵĻ�����
������Һ���µ�pH:�ò�����պȡ��Һ����ʪ����pH��ֽ���������ɫ������
����NaOH��Һ������Al2��SO4��3��Һ����Al2��SO4��3��Һ������NaOH��Һ����ͬ
�����ñ���̼��������Һ��ȥ������̼�����е�������������
����ij��ѧ�������ͼ��ʾ����ʵ��װ��������װ��δ���������Ʊ�SO2������ʵ�������� �����仹ԭ�ԣ��Ʊ�SO2ʱѡ�õ��Լ�ΪCu��ŨH2SO4���ش��������}��

��1��д����ȡSO2�Ļ�ѧ����ʽ��________________________��
��2���÷�Ӧ��ŨH2SO4���ֵĻ�ѧ������______________________��
��3����ͬѧ����ʵ������������SO2�Ļ�ԭ�ԣ���ѡ�õ��Լ�Ϊ___________��
A��˫��ˮ��H2O2��
B��Ʒ����Һ
C�����Ը��������Һ
����SO2��ԭ�Ե��Թ��е�����Ϊ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й����������ϸ��Ԫ�ص���������ȷ���ǣ� ��
A. �ڲ�ͬ�������ϸ���ڣ���ѧԪ�ص�������ȫ��ͬ
B. ���ϸ�������Ԫ����O
C. ��ͬһ������IJ�ͬϸ���ڣ����ֻ�ѧԪ�صĺ�����ͬ
D. ���������ϸ���Ļ�ѧԪ�أ�������Ȼ���ж����ҵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ű���ɴ���в�������ˮ�д�ϴ����������ɴ���ϵ������ʺ�ϴ���İ��������õ��Լ��ֱ���
A. ��Һ���յ���ȾҺ B. ��Һ������Լ�
C. ˫�����Լ�����Һ D. ˫�����Լ�������Լ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ʵ���������ȷ������ ��

A.��δ֪Һ����ζʱ��Ӧ�ý��Լ�ƿ�ھ���ڱ�ԶһЩ�����������ȶ�
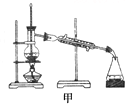
B�����ⵥ�ʴӵ��CCl4��Һ�з������������ͼ����ʾʵ��װ��
C��������ƿ���ƺ�һ��Ũ�ȵ�ij��Һ������ƿ����������ƿ�����ϱ�ǩ
D������500 mL 0.4 mol��L��1NaCl��Һ����Ҫ��������ͼ����ʾ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com