
【题目】下图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此,下列说法正确的是

A. 该硫酸的物质的量浓度为 9.2 mol/L
B. 1 mol Zn与足量的该硫酸反应产生2 g氢气
C. 配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50 mL
D. 该硫酸与等质量的水混合所得溶液的物质的量浓度大于9.2 mol/L
科目:高中化学 来源: 题型:
【题目】将粗硅转化成三氯硅烷(SiHCl3),进一步反应也可以制得粗硅。其反应为:SiHCl3(g)+H2(g)![]() Si(s)+3HCl(g)。不同温度下,SiHCl3的平衡转化率随反应物的投料比(反应初始时各反应物的物质的量之比)的变化关系如图所示。下列说法正确的是
Si(s)+3HCl(g)。不同温度下,SiHCl3的平衡转化率随反应物的投料比(反应初始时各反应物的物质的量之比)的变化关系如图所示。下列说法正确的是
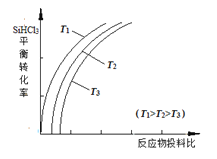
A. 该反应是放热反应
B. 横坐标表示的投料比应该是![]()
C. 该反应的平衡常数随温度升高而增大
D. 实际生产中为提高SiHCl3的利用率,可以适当增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作与装置均正确的是( )

A. 用甲装置从青蒿中提取对治疗疟疾有特效的青蒿素
B. 用乙装置配制酸碱中和滴定的标准液(0.1000mol/L HCl)
C. 用丙装置从海带灰中提取碘单质
D. 用丁装置将含等物质的量的K2SO4和Al2(SO4)3的混合溶液蒸干得到明矾晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中各微粒的浓度关系正确的是( )
A. pH相等的①NH4Cl②(NH4)2SO4③NH4HSO4溶液,c(NH4+)大小顺序为①=②>③
B. 0.2mol·L-1HCl与0.1 mol·L-1NaAlO2溶液等体积混合:c(Cl-)>c(Na+)>c(Al3+)>c(OH-)>c(H+)
C. 0.2 mol·L-1的Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3)
D. pH相等的NaF与CH3COOK溶液:[c(Na+)-c(F-)]>[c(K+)-c(CH3COO-)]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外小组设计了如图所示的装置制取乙酸乙酯(图中夹持仪器和加热装置已略去),请回答下列问题:
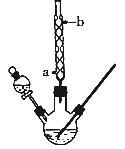
(1)球形冷凝管的作用是____________,冷凝水从____________(填“a”或“b”)处进入。
(2)已知下列数据:
乙醇 | 乙酸 | 乙酸乙酯 | 98%浓硫酸 | |
溶点/℃ | 117.3 | 16.6 | -83.6 | |
沸点/℃ | 78.5 | 117.9 | 77.5 | 338.0 |
又知温度高于140℃时发生副反应:2CH3CH2OH→CH3CH2OCH2CH3+H2O
①该副反应属于____________反应(填字母)。
a.加成反应 b.取代反应 c.酯化反应 d.消去反应
②考虑到反应速率等多种因素.用上述装置制备乙酸乙酯时,反应的最佳温度范围是____________(填字母)。
a.T<77.5℃ b.T>150℃ c.115℃<T<130℃
(3)反应结束后,欲从反应混合物中分离出乙酸乙酯,应使用的分离方法是____________(填操作方法名称,下同),所用到的主要仪器为____________,进行此步操作后,所得有机层中的主要无机物杂质是水,在不允许使用干燥剂的条件下,除去水可用____________的方法:在乙酸乙酯的同类物质的同分异构体中,有一种直链的酯在强碱条件下与新制氢氧化铜浊液混合加热一段时间后,发现生成了砖红色沉淀,请写出的化学方程式________________________。
(4)若实验所用乙酸质量为6.0g,乙醇质量为5.0g,得到纯净的产品质量为4.4g.则乙酸乙酯的产率是____________。
(5)乙二酸和乙二醇也能发生酯化反应,写出生成环酯的化学反应方程式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知下列各种共价键的键能:C—H:a kJ· mol-1、O—H:b kJ· mol-1、O=O:c kJ·mol-1、C=O:d kJ·mol-1。写出甲烷气体完全燃烧生成CO2气体和气体水的热化学方程式:_________________________________
(2)火箭中的主要燃料是“肼(也称为联氨)”的液体物质。此化合物的相对分子质量为32。其中,含N的质量分数为87.5%,其余为H元素。则:
①肼的化学式为__________________,其结构式为_____________________________
②此燃料的氧化剂是N2O4气体,若燃烧0.2 mol肼液体放出的热量为 400 kJ,燃烧的产物对大气都无污染(生成的水为液态),则肼与N2O4气体反应的热化学方程式为:__________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的氯气通入30 mL浓度为10.00 mol·L-1的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系。下列判断正确的是
A. 与NaOH反应的氯气一定为0.3 mol
B. n(Na+)∶n(Cl-)可能为7∶3
C. 若反应中转移的电子为n mol,则0.15<n<0.25
D. n(NaCl)∶n(NaClO)∶n(NaClO3)可能为11∶2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2.80 g含氧化镁的镁条完全溶于50.0 mL硫酸溶液后,滴加2.00 mol·Lˉ1氢氧化钠溶液,恰好完全沉淀时用去200.0 mL。将所得的沉淀灼烧、冷却后称量得固体质量为4.40 g。
(1)求上述硫酸的物质的量浓度c(H2SO4)=____________________________。
(2)镁条中氧化镁和镁的物质的量之比为n(MgO)︰n(Mg)=______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质分类的正确组合是( )
碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
A | 纯碱 | 硫酸 | 小苏打 | 氧化铝 | 干冰 |
B | 苛性钠 | 盐酸 | 食盐 | 氧化钠 | 一氧化碳 |
C | 熟石灰 | 冰醋酸(CH3COOH) | 胆矾CuSO4·5H2O | 三氧化硫 | 二氧化硫 |
D | 苛性钾 | HNO3 | 碳酸钙 | 生石灰 | SO3 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com