
����Ŀ����1��0.5 mol Na2CO3�к���_____��Na+��
��2����������HCl��NH3��CO2��O2�������壬����ͬ�¶Ⱥ���ͬѹǿ�����£����������_______��
��3��ʵ������Ҫ0.50mol��L��1NaCl��Һ480mL��
��������Һʱ����������У�������ƽ����ȷ��0.1����ҩ�ס��ձ�����������______����ͷ�ι��Լ��������ļ�Ƭ��ֽ��
�����Ƹ���Һ���ȡNaCl���������Ϊ_______��
�����в�����ʹ������ҺŨ��ƫ�͵���________��
A ����ƿϴ�Ӹɾ���δ����
B ���ݺ���ҡ�ȡ����ã�����Һ���½����ټ�����������ˮ
C ����ʱ���ӿ̶���
D �ձ��Ͳ�����δϴ��
���𰸡�NA��6. 02��1023 NH3 500 mL����ƿ 14.6 BD
��������
(1)1mol̼���ƺ���2mol�����ӣ�
(2)��n=![]() =
=![]() �������
�������
(3)�ٸ���ʵ��������輰������������ѡȡ������
�ڸ���m=cVM�������ʵ�������ͬʱ��������ƿ�Ĺ����ƽ�ľ�ȷ�������
�۷������������ʵ����ʵ�������Һ�����Ӱ�죬����c=![]() ������������
������������
(1)0.5molNa2CO3�к��������Ӹ���Ϊ��0.5mol��2��NA=NA��
(2)��֪��M(HCl)=36.5g/mol��M(NH3)=17g/mol��M(CO2)=44g/mol��M(O2)=32g/mol����n=![]() =
=![]() ������֪��ͬ����ʱ��Ħ������Խ����������ʵ���ԽС�����ԽС������ͬ�¶Ⱥ���ͬѹǿ�����£����������NH3��
������֪��ͬ����ʱ��Ħ������Խ����������ʵ���ԽС�����ԽС������ͬ�¶Ⱥ���ͬѹǿ�����£����������NH3��
(3)��ʵ������IJ��裺���㡢�������ܽ⡢��Һ��ϴ����Һ�����ݡ�ҡ�ȵȲ�������ʵ������Ҫ����ƽ��������ҩ��ȡҩƷ���ձ��ܽ�ҩƷ����Ҫ�������������������Ҫ500mL����ƿ������Һ����Ҫ��ͷ�ιܶ��ݣ�
��ʵ��������480mL1mol/L���Ȼ�����Һ��ʵ����û��480mL����ƿ��ֻ��ѡ��500mL����ƿ��������Ҫ����500mL��Һ��������500mL1mol/L���Ȼ�����Һ����Ҫ�Ȼ��Ƶ�����m=cVM=0.50mol/L��0.5L��58.5g/mol=14.625g��������ƽ��ȷ��Ϊ0.1g����������ƽ��������Ϊ14.6g��
��A������ƿϴ�Ӹɾ���δ��������ʵ����ʵ�������Һ�����������Ӱ�죬��ҺŨ����Ӱ�죬��A����
B�����ݺ���ҡ�ȡ����ã�����Һ���½����ټ�����������ˮ��������Һ���ƫ����ҺŨ��ƫ�ͣ���B��ȷ��
C������ʱ���ӿ̶��ߣ�������Һ���ƫС����ҺŨ��ƫ�ߣ���C����
D���ձ��Ͳ�����δϴ�ӣ������������ʵ���ƫС����ҺŨ��ƫ�ͣ���D��ȷ��
�ʴ�ΪBD��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ٵ����������̼���������ڴ����е��ŷ��ǻ�����������Ҫ����֮һ������Ӧ�úʹ���̼�������仯�������������������Ҫ���塣
(1)���������������̼���о�һֱ�ǿƼ����ע���ص㡣�ڴ�����������H2��ԭCO2 �ǽ������ЧӦ����Ҫ�ֶ�֮һ,��ط�Ӧ����:
��֪H2 ��CH4��ȼ���ȷֱ�Ϊ285.5kJ/mol ��890.0kJ/mol��
H2O(1) =H2O(g) ��H= +44 kJ/mol
��д��H2 ��ԭCO2 ����CH4��H2O(g)���Ȼ�ѧ����ʽ_____________��
(2)CO2��Cu-ZnO����,��ͬʱ�������µķ�ӦI��II�������Ϊ�������ЧӦ����Դ��ȱ����Ҫ�ֶΡ�
I.CO2(g) +3H2(g)![]() CH3OH(g) +H2O(g) ��H1=-57.8 kJ/mol
CH3OH(g) +H2O(g) ��H1=-57.8 kJ/mol
II.CO2(g) +H2(g)![]() CO(g) + H2O(g) ��H2 = +41.2 kJ/mol
CO(g) + H2O(g) ��H2 = +41.2 kJ/mol
��ij�¶�ʱ������ӦI���ٶ�v1���ڷ�ӦII���ٶ���v2,�����з�Ӧ���̵������仯��ȷ����_______(��ѡ��)��
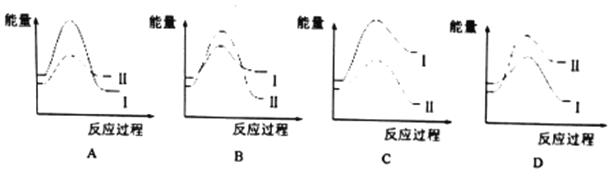
�ڶ�������μӵķ�Ӧ,����ʾƽ�ⳣ��Kpʱ,���������(B)��ƽ���ѹp(B)������������ʵ���Ũ��c(B)��
��֪:�������ֵķ�ѹp(B)��������ѹ���������������
��Cu-ZnO���ڵ������£������¶�Tʱ�����ݻ�������ܱ�������,����һ������CO2 ��H2����ʼ����ƽ��ʱ�������ڸ��������ʵ������±�:
CO2 | H2 | CH3OH | CO | H2O(g) | ��ѹ/kPa | |
��ʼ/mol | 5.0 | 7.0 | 0 | 0 | 0 | p0 |
ƽ��/mol | n1 | n2 | p |
����ӦI��II����ƽ��ʱ,P0=1.2p�������n1=____������ʱ
(3)����β���������γɵ�ԭ��֮һ���о���������Ĵ�����������Ч�����������γɣ��ɲ���������ԭ������:
4NO(g) +4NH3(g) +O2(g) ![]() 4N2(g) +6H2O(g) ��H <0
4N2(g) +6H2O(g) ��H <0
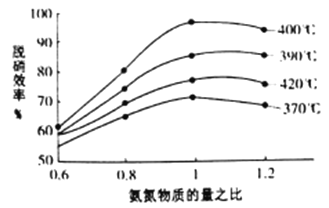
������ͼ�ж��������Ч�ʵ����������________;������һ��ʱ,��400��ʱ,����Ч�����,����ܵ�ԭ����______________��
(4)�û���̿��ԭ��Ҳ���Դ�����������,ij�о�С����ij�ܱ���������һ�����Ļ���̿��NO,������Ӧ:C(s) +2NO(g)![]() N2(g) +CO2(g) ��H>0
N2(g) +CO2(g) ��H>0
��T��ʱ,��Ӧ���е���ͬʱ���ø����ʵ���Ũ������:
ʱ��/min Ũ��/(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
30min��,ֻ�ı�ijһ����,�����ϱ��������жϸı������������_______��
A.ͨ��һ������CO2 B.������ʵĴ��� C.�ʵ���С���������
D.ͨ��һ������NO E.����һ�����Ļ���̿ F.�ʵ������¶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�ӦX(g)��Y(g)![]() 2Z(g) ��H��0������Ӧ��ʼ��t1��ﵽƽ�⣬�־�t2�����ڷ�Ӧ�����ĸı�ʹƽ���ƻ�����t3ʱ�ִ�ƽ��(��ͼ��ʾ)��t2��t3���߱仯��ԭ����
2Z(g) ��H��0������Ӧ��ʼ��t1��ﵽƽ�⣬�־�t2�����ڷ�Ӧ�����ĸı�ʹƽ���ƻ�����t3ʱ�ִ�ƽ��(��ͼ��ʾ)��t2��t3���߱仯��ԭ����
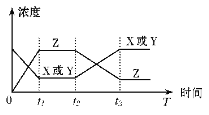
A. ������X��Y��Ũ��
B. ʹ���˴���
C. �����˷�Ӧ��ϵ��ѹǿ
D. �����˷�Ӧ���¶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I.ʵ���ҿ���KMnO4��Ũ���ᷴӦ��ȡ������
2KMnO4��16HCl(Ũ) ![]() 2KCl��2MnCl2��5Cl2����8H2O��
2KCl��2MnCl2��5Cl2����8H2O��
��1���õ����ű������ת�Ƶķ������Ŀ��____________________
��2����������ƽ�Ļ�ѧ����ʽ��дΪ���ӷ���ʽ__________________________________ ��
��3��Ũ�����ڷ�Ӧ����ʾ������������________________
��ֻ�л�ԭ�� ����ԭ�Ժ�����
��ֻ�������� �������Ժ�����
��4��������0.5molCl2����������HCl________mol��ת�Ƶĵ��ӵ���ĿԼΪ____________��
II�����ݷ�ӦCu+4HNO3(Ũ)![]() Cu(NO3)2+2NO2��+2H2O���ش���������:
Cu(NO3)2+2NO2��+2H2O���ش���������:
����ԭ������______��
����������������������ʵ���֮����____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Σ�ջ�ѧƷҪ�ڰ�װ��ӡ�Ͼ�ʾ�Ա�־�����л�ѧƷ�������뾯ʾ�Ա�־���ƶ�Ӧ��ȷ����
A. �ռ����ըƷ B. Ũ���ᡪ���綾Ʒ
C. ���͡�����ʴƷ D. �ƾ�������ȼƷ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ά�����������������������Ҫƽ��ϵͳ���ش��������⣺
��.����ѪҺ�д���ƽ�⣺H2CO3 (aq)![]() H+(aq)+HCO3-(aq) ��H����ƽ���ʹѪҺ��pHά����һ����Χ�ڡ�
H+(aq)+HCO3-(aq) ��H����ƽ���ʹѪҺ��pHά����һ����Χ�ڡ�
(1)��֪��
CO2(g)![]() CO2(aq) ��H1=akJ��mol-l��
CO2(aq) ��H1=akJ��mol-l��
CO2(aq)+H2O(l)![]() H2CO3 (aq) ��H2=bkJ mol-1��
H2CO3 (aq) ��H2=bkJ mol-1��
HCO3-(aq)![]() H+(aq)+CO32-(aq) ��H3=ckJ mol-1��
H+(aq)+CO32-(aq) ��H3=ckJ mol-1��
CO2(g)+H2O(l)![]() 2H+(aq)+CO32-(aq) ��H4=dkJ mol-1��
2H+(aq)+CO32-(aq) ��H4=dkJ mol-1��
���������뷽��ʽ�С�H =_____________(�ú�a��b��c��d�Ĵ���ʽ��ʾ)��
(2)��ij��ѪҺ��c(HCO3-)��c(H2CO3)=20��1��pKa1(H2CO3)=6.1�������ѪҺ��pH=_____________,pH���ߣ���![]() ___(�������С�����䡱)��
___(�������С�����䡱)��
(3)���������������ʽ���ѪҺ��ѪҺ��pH�仯������ƽ���ƶ�ԭ��������������_____________��
��.��ϸ��ʯ���������ͷ�������ʱ��������ƽ�⣺
Mb(aq)+O2(g)![]() MbO2(aq)��
MbO2(aq)��
���쵰�� ���ϼ��쵰��
(4)���ⶨ�����������ߣ������Ľ�϶�[��(MbO2)�����ϼ��쵰��Ũ��ռ���쵰�׳�ʼŨ�ȵİٷ���]���ͣ���÷�Ӧ�ġ�H_______________(�>����<��)0��
(5)�¶�Ϊ37 ��ʱ�������Ľ�϶�[��(MbO2)��������ƽ���ѹ[p(O2)]��ϵ����ͼ��ʾ��
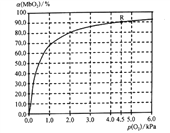
������R����ʾ���ݣ�����37 ��ʱ�÷�Ӧ��ƽ�ⳣ��K=_________________(������ƽ��Ũ�ȿ���������ƽ���ѹ��������)��
����֪37 ��ʱ���÷�Ӧ������Ӧ����v(��)=k1c(Mb)��p(O2)���淴Ӧ����v(��)=k2c(MbO2)����k2=60s-1����k1=___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ��С���о���Һ��AgNO3��Na2S�ķ�Ӧ��
ʵ�� | �Լ� | ���� | |
| �Թ� | �ι� | |
��pH = 4�� |
��pH = 9�� | ���ֺ�ɫ���� | |
��1�������ӷ���ʽ����Na2S��ҺpH > 7��ԭ��________��
��2��ʵ��С��ͬѧ��Ϊ��ɫ�����п��ܺ���Ag2O��Ag2S��Ag�����ʵ����֤��
��֪��i��Ũ�����ܽ�Ag2Sת��Ϊ![]() ��
��![]() ��
��
ii��Ag2O���ܽ���Ũ��ˮ���γ�������Һ����Ag2S��Ag�����ܡ�
�� ��Ʋ�ʵʩ����ʵ�飬֤ʵ�����к���Ag2S��

�Լ�1���Լ�2�ֱ���_________��_________��
����1������2�ֱ���_________��_________��
�� ��Ʋ�ʵʩ����ʵ�飬֤ʵ������������Ag2O����ʵ�����������������
ʵ����� | ʵ������ | |
����i | ȡ����������Һ�������еμ����� | ���ְ�ɫ���� |
����ii | ȡ����ϴ�Ӻ�ĺ�ɫ������____________ | ____________ |
�� �����飬����������Ag��

��3��ʵ��С��ͬѧ��ΪAgNO3��Һ���������ԣ���һ���������ܹ�����Na2S�����ʵ������о���ʵ��װ������ͼ��ʾ������õ�ѹΪa��![]() ����
����
��AgNO3��Һ������![]() �����ʽ����Ʋ⣺
�����ʽ����Ʋ⣺
����1�� ![]() ��AgNO3��Һ��
��AgNO3��Һ��![]() ������
������![]() ��
��
����2�� ![]() ��AgNO3��Һ��
��AgNO3��Һ��![]() ������
������![]() ��
��
������ͼװ�ü����о�����֪����ѹ��С��ӳ������������ԭ��ǿ���IJ��죻�����������뻹ԭ��ǿ������Խ��ѹԽ��
�� ��![]() ��AgNO3��Һ�滻Ϊ_______��Һ����¼��ѹΪb��
��AgNO3��Һ�滻Ϊ_______��Һ����¼��ѹΪb��![]() ����
����
�� ����ʵ��֤ʵ������![]() ��������һ������
��������һ������![]() ����֤����______��
����֤����______��
ʵ����ۣ�AgNO3��Һ��Na2S��Һ�ķ�Ӧ�����뷴Ӧ�����йء�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�þ���仯��������ӷ���ʽ��д��ȷ���ǣ� ��
A.MgCO3�����ᷴӦ��CO32-��2H��=CO2����H2O
B.Mg(OH)2��H2SO4��Ӧ��Mg2����2OH-��2H����SO42-=MgSO4����2H2O
C.þ����ᷴӦ��Mg��2H��=Mg2����H2��
D.�Ȼ�þ��Һ��AgNO3��Һ��Ӧ��Ag+��Cl-=AgCl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ��ֻ����Na+��Al3+��Cl��SO42�������ӣ���֪ǰ�������ӵĸ�����Ϊ5��2��1������Һ��Al3+��SO42�����Ӹ�����Ϊ
A. 1��2 B. 1��4 C. 3��4 D. 2��5
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com