

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
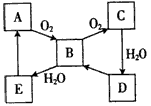
 ��2008?���ϣ���ͼ��ʾij��̬����A���仯����֮���ת����ϵ��ijЩ����ͷ�Ӧ��������ȥ����������B�ڳ��³�ѹ��Ϊ���壬B��C����Է�������֮��Ϊ4��5��������D����Ҫ�Ĺ�ҵԭ�ϣ�
��2008?���ϣ���ͼ��ʾij��̬����A���仯����֮���ת����ϵ��ijЩ����ͷ�Ӧ��������ȥ����������B�ڳ��³�ѹ��Ϊ���壬B��C����Է�������֮��Ϊ4��5��������D����Ҫ�Ĺ�ҵԭ�ϣ�
| ||
| ||
| ||
| ||
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
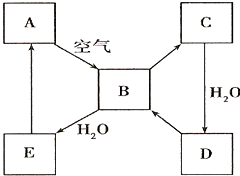 ��1�������ʽ��з��࣬����ʶ���ʵ���ɡ��ṹ�����ʺ���;�ı��;�������÷���ķ�������ʶ�������ʣ�����ţ�����NaCl���� �ڽ���ͭ ������ ��SO2 ������
��1�������ʽ��з��࣬����ʶ���ʵ���ɡ��ṹ�����ʺ���;�ı��;�������÷���ķ�������ʶ�������ʣ�����ţ�����NaCl���� �ڽ���ͭ ������ ��SO2 ������
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ���㽭ʡ��У������һ��������ѧ�Ծ��������棩 ���ͣ������
A��B��C��D��E��F��G����Ԫ�ؾ��Ƕ�����Ԫ�أ���ԭ��������������Aԭ�������ӣ� B��Gԭ�ӵ�������������Ϊ����Ӳ�����������D��GԪ��ԭ�ӵ�������������ȡ�X��Y��Z��W���ס����������ʾ�������Ԫ�ص����ֻ�����Ԫ����ɣ�Ԫ��B�γɵĵ���M��ס��ң��ס����Ǹ��г�����Ũ�ᣩ���ܷ�Ӧ����Է���������< �ң�ת����ϵ��ͼ����Ӧ������ȥ����ԭ��E����������������Ӳ�����ȡ�Ԫ��F�γɵĵ����� ��21���͵���Դ������ĿǰӦ�����İ뵼����ϡ���ش��������⣺

��1��A2D���۷е��A2G�ߵ�ԭ���� ��B��D��G��һ��ԭ�ӹ���ÿԭ�Ӿ�����8���ӵķ��ӣ������ʽ�� ��
��2��E4B3��ˮ��Ӧ�Ļ�ѧ����ʽ ��
��3��д��M���Ũ��Һ����ʱ��Ӧ�Ļ�ѧ����ʽ ��
��4��X��Y��Z��W����ͬһ�����ʣ���������̬ʱ�ľ�������Ϊ ��X��Y��W������Z��Ӧ����Z�ĽṹʽΪ ��
��5����֪CH4 ��g���� 2O2 ��g����CO2 ��g����2H2O ��l�� ��H1��a kJ/mol
�����㷴ӦCH4 ��g���� 4NO ��g����2N2 ��g����CO2 ��g����2H2O ��l�����ʱ��H2 �� ����Ҫ����ij���Ϸ�Ӧ���ʱ��H3������Ӧ�и����ʻ�ѧ������֮��Ϊ���������ʱ ��H3 = b kJ/mol����÷�Ӧ���Ȼ�ѧ����ʽΪ ��
�ݴ˼������H2 = kJ/mol���ú�a��b��ʽ�ӱ�ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
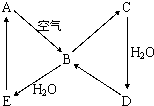 ��ͼ��ʾij��̬����A���仯����֮���ת����ϵ��ijЩ����ͷ�Ӧ��������ȥ����������B�ڳ��³�ѹ��Ϊ���壬B��C����Է�������֮��Ϊ4��5��������D����Ҫ�Ĺ�ҵԭ�ϣ�
��ͼ��ʾij��̬����A���仯����֮���ת����ϵ��ijЩ����ͷ�Ӧ��������ȥ����������B�ڳ��³�ѹ��Ϊ���壬B��C����Է�������֮��Ϊ4��5��������D����Ҫ�Ĺ�ҵԭ�ϣ��鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com