
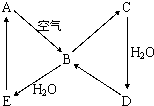
 如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料.
如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料. H2S,故答案为:H2+S
H2S,故答案为:H2+S H2S;
H2S; CO2↑+2SO2↑+2H2O或Cu+2H2SO4(浓)
CO2↑+2SO2↑+2H2O或Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O等,
CuSO4+SO2↑+2H2O等, CO2↑+2SO2↑+2H2O或Cu+2H2SO4(浓)
CO2↑+2SO2↑+2H2O或Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O等;
CuSO4+SO2↑+2H2O等;

科目:高中化学 来源: 题型:
 (2008?海南)如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料.
(2008?海南)如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料.
| ||
| ||
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
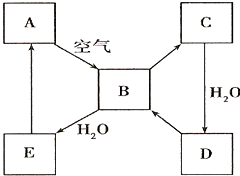 (1)把物质进行分类,是认识物质的组成、结构、性质和用途的便捷途径.请用分类的方法来认识以下物质(填序号):①NaCl晶体 ②金属铜 ③盐酸 ④SO2 ⑤蔗糖
(1)把物质进行分类,是认识物质的组成、结构、性质和用途的便捷途径.请用分类的方法来认识以下物质(填序号):①NaCl晶体 ②金属铜 ③盐酸 ④SO2 ⑤蔗糖
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2013-2014学年浙江省五校高三第一次联考化学试卷(解析版) 题型:填空题
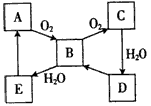
A、B、C、D、E、F、G七种元素均是短周期元素,且原子序数依次增大。A原子无中子, B、G原子的最外层电子数均为其电子层数的两倍,D、G元素原子的最外层电子数相等。X、Y、Z、W、甲、乙六种物质均由上述元素的两种或三种元素组成,元素B形成的单质M与甲、乙(甲、乙是高中常见的浓酸)均能反应(相对分子质量甲< 乙)转化关系如图(反应条件略去),原子E最外层电子数和其电子层数相等。元素F形成的单质是 “21世纪的能源”,是目前应用最多的半导体材料。请回答下列问题:

(1)A2D的熔沸点比A2G高的原因是 。B、D、G各一个原子构成每原子均满足8电子的分子,其电子式是 。
(2)E4B3和水反应的化学方程式 。
(3)写出M与甲的浓溶液加热时反应的化学方程式 。
(4)X、Y、Z、W属于同一类物质,这类化合物固态时的晶体类型为 ;X、Y、W都能与Z反应,则Z的结构式为 。
(5)已知CH4 (g)+ 2O2 (g)=CO2 (g)+2H2O (l) △H1=a kJ/mol
欲计算反应CH4 (g)+ 4NO (g)=2N2 (g)+CO2 (g)+2H2O (l)的焓变△H2 , 则还需要查找某化合反应的焓变△H3,当反应中各物质化学计量数之比为最简整数比时 △H3 = b kJ/mol,则该反应的热化学方程式为 。
据此计算出△H2 = kJ/mol(用含a和b的式子表示)。
查看答案和解析>>
科目:高中化学 来源:专项题 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com