
【题目】已知A是一种金属单质,B溶液能使酚酞试液变红,且焰色反应呈黄色;D、F相遇会产生白烟。A、B、C、D、E、F间有如下变化关系:

(1)写出A、B、C、E的化学式:
A__________,B__________,C__________,E__________。
(2)写出E→F反应的化学方程式_________;写出B→D反应的化学方程式_________。
(3)F在空气中遇水蒸气产生白雾现象,这白雾实际上是________。
【答案】Na NaOH NH4Cl H2 H2+Cl2![]() 2HCl NH4Cl + NaOH
2HCl NH4Cl + NaOH![]() NaCl +H2O +NH3 ↑ 盐酸小液滴
NaCl +H2O +NH3 ↑ 盐酸小液滴
【解析】
A是一种金属,该金属能和水反应生成溶液B和气体E,B溶液能使酚酞试液变红,说明B是碱,焰色反应呈黄色,说明含有钠元素,所以B是NaOH,根据元素守恒知A是Na,E是H2;氢气在氯气中燃烧生成HCl,则F是HCl,氢氧化钠溶液和C反应生成D,D、F相遇会产生白烟,氯化氢和氨气反应生成白烟氯化铵,则D是NH3,C是NH4Cl,据此分析解答。
(1)根据上面的分析可知,A是Na,B是NaOH,C是NH4Cl,E是H2;
(2) E→F为在点燃的条件下,氢气和氯气反应生成氯化氢,反应方程式为:H2+Cl2![]() 2HCl; B→D为在加热条件下,氯化铵和氢氧化钠反应生成氯化钠、氨气和水,反应方程式为:NH4Cl + NaOH
2HCl; B→D为在加热条件下,氯化铵和氢氧化钠反应生成氯化钠、氨气和水,反应方程式为:NH4Cl + NaOH![]() NaCl +H2O +NH3 ↑;
NaCl +H2O +NH3 ↑;
(3) F是HCl,HCl极易溶于水生成盐酸,所以氯化氢在空气中遇水蒸气生成盐酸小液滴而产生白雾。


 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】微生物燃料电池(MFC)是一种现代化氨氮去除技术。下图为MFC碳氮联合同时去除的转化系统原理示意图。下列说法正确的是
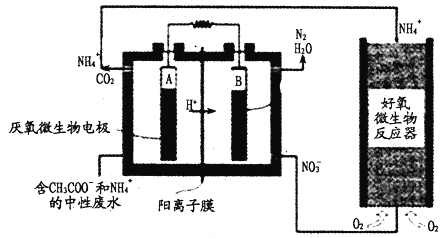
A. 好氧微生物反应器中反应为:NH4++2O2==NO3-+2H++H2O
B. B极电势比A极电势低
C. A极的电极反应式CH3COO-+8e-+2H2O==2CO2+7H+
D. 当电路中通过1mol电子时,理论上总共生成2.24LN2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
B元素原子的核外p电子数比s电子数少1个 |
C元素原子的第一至第四电离能分别是:I1=738 kJ·mol-1;I2=1 451 kJ·mol-1;I3=7 733 kJ·mol-1;I4=10 540 kJ·mol-1 |
D原子核外所有p轨道全满或半满 |
E元素的主族序数与周期数的差为4 |
F是前四周期中电负性最小的元素 |
G在周期表的第七列 |
(1)B基态原子中能量最高的电子,其电子云在空间有_____个方向,原子轨道呈___形
(2)某同学根据上述信息,推断C基态原子的核外电子排布图为![]()
![]() 该同学所画的电子排布图违背了____。
该同学所画的电子排布图违背了____。
(3)G位于______族______区,价电子排布式为______。
(4)检验F元素的实验方法是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图装置探究铁在海水中的电化学腐蚀与防护。下列说法不正确的是

A. 若X为锌棒,开关K置于M处,可减缓铁的腐蚀,采用了牺牲阳极的阴极保护法
B. 若X为锌棒,开关K置于N处,X极的反应:4OH--4e-=O2↑+2H2O
C. 若X为碳棒,开关K置于N处,可减缓铁的腐蚀,采用了外加电流的阴极保护法
D. 若X为碳棒,开关K置于M处,X极的反应:O2+4e-+2H2O=4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将一定量的固体 A 置于固定容积的密闭容器中发生分解反应,一段时间后达到平衡A(s) ![]() 2B(g)+C(g),以下可以作为平衡标志的是
2B(g)+C(g),以下可以作为平衡标志的是
A.2v正(B)=v逆(C)
B.气体 B 的体积分数不变
C.混合气体的平均摩尔质量不变
D.混合气体的密度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】10℃时加热![]() 饱和溶液,测得该溶液的pH发生如下变化:
饱和溶液,测得该溶液的pH发生如下变化:

(1)![]() 饱和溶液中存在三个平衡关系,写出三个平衡表达式 :________;_______;______。
饱和溶液中存在三个平衡关系,写出三个平衡表达式 :________;_______;______。
(2)甲同学认为,该溶液的pH升高的原因是![]() 的水解程度增大,故碱性增强。乙同学认为,溶液的pH升高的原因是
的水解程度增大,故碱性增强。乙同学认为,溶液的pH升高的原因是![]() 受热分解,生成了
受热分解,生成了![]() ,并推断
,并推断![]() 的水解程度________(填“大于”或“小于”)
的水解程度________(填“大于”或“小于”)![]() 。丙同学认为将加热后的溶液冷却到10℃,若溶液的pH等于8.3,则 ____________(填“甲”或“乙”)判断正确。
。丙同学认为将加热后的溶液冷却到10℃,若溶液的pH等于8.3,则 ____________(填“甲”或“乙”)判断正确。
(3)丁同学向饱和![]() 溶液中加入饱和
溶液中加入饱和![]() 溶液,观察到有白色沉淀和无色气体,经检验该白色沉淀为碳酸钙沉淀,试利用沉淀溶解平衡表达式和K、Q关系分析产生该沉淀的原因 ____________。
溶液,观察到有白色沉淀和无色气体,经检验该白色沉淀为碳酸钙沉淀,试利用沉淀溶解平衡表达式和K、Q关系分析产生该沉淀的原因 ____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某可逆反应aA + bB![]() cC + Q在某温度下的平衡常数为K(K≠1),反应热为Q。保持温度不变,将方程式的书写作如下改变,则Q和K数值的相应变化为( )
cC + Q在某温度下的平衡常数为K(K≠1),反应热为Q。保持温度不变,将方程式的书写作如下改变,则Q和K数值的相应变化为( )
A.写成2aA + 2bB![]() 2cC,Q值、K值均扩大了一倍
2cC,Q值、K值均扩大了一倍
B.写成2aA + 2bB![]() 2cC,Q值扩大了一倍,K值保持不变
2cC,Q值扩大了一倍,K值保持不变
C.写成cC![]() aA + bB,Q值、K值变为原来的相反数
aA + bB,Q值、K值变为原来的相反数
D.写成cC![]() aA + bB,Q值变为原来的相反数,K值变为倒数
aA + bB,Q值变为原来的相反数,K值变为倒数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环扁桃酯又名安脉生,在临床上主要用于治疗脑动脉硬化。环扁桃酯的一种合成路线如下所示:
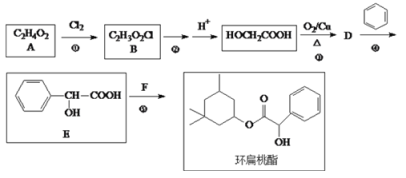
完成下列填空:
(1)写出反应类型。①_______________ ⑤ ___________________
(2)写出反应②的化学方程式________________________________________________________。
(3)反应⑤中另一反应物F的结构简式为_________________________。
(4)检验D是否已经完全转化E的操作是_______________________________________。
(5)写出一种满足下列条件E的同分异构体的结构简式。___________________________
i.能发生水解反应 ii.苯环上的一溴代物只有两种
(6)苯乙酮(![]() )是工业上合成E的原料之一。设计一条由苯乙酮为原料合成聚苯乙烯(
)是工业上合成E的原料之一。设计一条由苯乙酮为原料合成聚苯乙烯(![]() )的合成路线。_______________________________(合成路线常用的表示方式为:
)的合成路线。_______________________________(合成路线常用的表示方式为:![]() 目标产物)
目标产物)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据电化学知识回答下列问题。
Ⅰ、某小组同学设想用如图装置电解硫酸钾溶液来制取氧气、氢气、硫酸和氢氧化钾。
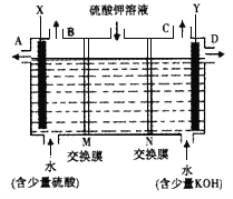
(1)X极与电源的_____(填正或负)极相连,氢气从____ (选填A、 B、C或D)口导出。
(2)离子交换膜只允许一类离子通过,则M为________(填阴离子或阳离子,下同)交换膜,N为________交换膜。
(3)若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池(石墨为电极),则电池正极的电极反应式为___________________
Ⅱ、铅蓄电池是常见的二次电池,其放电反应和充电反应表示如下:Pb(s)+PbO2(s)+2H2SO4(aq)![]() 2PbSO4(s)+2H2O(l)
2PbSO4(s)+2H2O(l)
写出它放电时正极的电极反应式______________________________________;
充电时阴极的电极反应式______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com