
下列有关化学用语表达正确的是
A.二氧化硅的分子式:SiO2
B.HClO的电子式: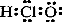
C.乙酸分子的球棍模型:
D.离子结构示意图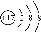 可以表示35Cl-,也可以表示37Cl-
可以表示35Cl-,也可以表示37Cl-
科目:高中化学 来源:2016届重庆市高三上学期第二次月考理综化学试卷(解析版) 题型:选择题
以下数值大于或等于阿伏加德罗常数的是
A.6g石墨中的共价键数目
B.常温常压下,17g ND3中所含分子数目
C.向0.2mol NH4Al(SO4)2溶液中滴加NaOH溶液至沉淀完全溶解,消耗的OH-数目
D.0.1mol羟基(—OH)中所含电子数目
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上学期第一次月考化学试卷(解析版) 题型:选择题
用下列实验装置进行相应实验,设计正确且能达到实验目的的是

A.用图1所示装置制取少量H2
B.用图2所示装置分离Na2CO3溶液和CH3COOC2H5的混合物
C.用图3所示装置验证Na和水反应的热效应
D.用图4所示装置蒸干A1Cl3溶液制备无水AlC13
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二9月月考化学试卷(解析版) 题型:实验题
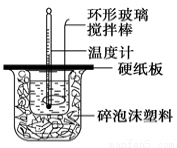
某实验小组设计用50 mL 1.0 mol/L盐酸跟50 mL 1.1 mol/L 氢氧化钠溶液在如图装置中进行中和反应。在大烧杯底部垫碎泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平。然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过。通过测定反应过程中所放出的热量可计算中和热。试回答下列问题:
(1)本实验中用稍过量的NaOH的原因是 。在大小烧杯中填充泡沫塑料的作用是 。
(2)该实验小组做了三次实验,每次取溶液各50 mL,并记录下原始数据(见下表)。
实验序号 | 起始温度t1/℃ | 终止温度(t2)/℃ | 温差 (t2-t1)/℃ | ||
盐酸 | NaOH溶液 | 平均值 | |||
1 | 25.1 | 24.9 | 25.0 | 31.6 | 6.6 |
2 | 25.1 | 25.1 | 25.1 | 31.8 | 6.7 |
3 | 25.1 | 25.1 | 25.1 | 31.9 | 6.8 |
已知盐酸、NaOH溶液密度近似为1.00 g/cm3,中和后混合液的比热容为:c=4.18×10-3kJ/(g·℃),则写出该反应的热化学方程式 (ΔH值保留到小数点后1位)。
(3)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热会比(2)测出的ΔH________(填“偏大”、“偏小”或“不变”),其原因是___________。
(4)在中和热测定实验中存在用水洗涤温度计上的盐酸后再用温度计测定NaOH溶液温度的步骤,若无此操作步骤,则测得的中和热ΔH会____________(填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省富阳市高三上学期第二次质量检测化学试卷(解析版) 题型:填空题
(10分)某研究小组以粗盐和碳酸氢铵(NH4HCO3)为原料,采用以下流程制备纯碱(Na2CO3)和氯化铵(NH4Cl)。
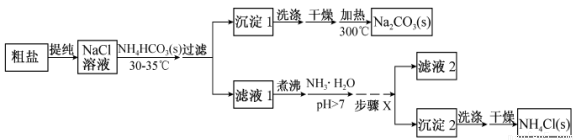
已知盐的热分解温度:NH4HCO3 36℃;NaHCO3 270℃;NH4Cl 340℃;Na2CO3>850℃
请回答:
(1)从NaCl溶液到沉淀1的过程中,需蒸发浓缩。在加入固体NH4HCO3之前进行蒸发浓缩优于在加入NH4HCO3固体之后,其原因是 。
(2)为提高NH4Cl产品的产率和纯度,需在滤液1中加入氨水,理由是 ;步骤X包括的操作有 。
(3)测定NH4Cl产品的纯度时,可采用的方法:在NH4Cl溶液中加入甲醛使之生成游离酸(4NH4Cl+6HCHO=(CH2)6N4+4HCl+6H2O),然后以酚酞为指示剂,用NaOH标准溶液(需用邻苯二甲酸氢钾基准物标定)进行滴定。
①下列有关说法正确的是 。
A.为了减少滴定误差,滴定管、锥形瓶均须用待装液润洗
B.标准NaOH溶液可以装入带有耐腐蚀旋塞的玻璃滴定管中
C.开始滴定前,不需擦去滴定管尖悬挂的液滴
D.三次平行测定时,每次需将滴定管中的液面调至“0”刻度或“0”刻度以下的附近位置
②若用来标定NaOH标准溶液的邻苯二甲酸氢钾基准物使用前未烘至恒重,则测得NH4Cl产品的含量比实际含量 (填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源:2016届江西省九江市七校高三第一次联考化学试卷(解析版) 题型:选择题
下列说法正确的个数是
①用四氯化碳萃取溴水中的溴,分液时有机层从分液漏斗的下端放出
②乙酸与乙醇的混合溶液可用分液漏斗进行分离
③在含FeCl2杂质的FeCl3溶液中通足量Cl2后,充分加热,除去过量的Cl2,即可得到较纯净的FeCl3溶液
④利用饱和Na2CO3溶液能够除去二氧化碳中的氯化氢
⑤加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铝粉
⑥用溶解、过滤的方法分离KNO3和NaCl固体的混合物
⑦将O2和H2的混合气体通过灼热的氧化铜,以除去其中的H2
A.2 B.3 C.4 D.5
查看答案和解析>>
科目:高中化学 来源:2016届河南省三门峡市高三上学期第一次精英对抗赛化学试卷(解析版) 题型:选择题
下列离子在指定条件下能大量共存的是 ( )
A.能使石蕊试液显红色的溶液中:NH4+、Fe 2+、Al3+、NO3-
B.加入NH4HCO3能产生气体的溶液中:K+、Na+、I-、SO42-
C.中性透明溶液中:K+、HCO3-、NO3-、Fe3+
D.常温下由水电离出的c(H+)•c(OH-)=10-20的溶液中:Na+、NH4+、Cl-、SiO32-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省邯郸市高一上第一次月考化学试卷(解析版) 题型:选择题
V L Fe2(SO4)3溶液中含Fe3+ m g,则溶液中SO42-的物质的量浓度为
A. mol·L-1 B.
mol·L-1 B. mol·L-1
mol·L-1
C.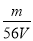 mol·L-1 D.
mol·L-1 D. mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源:2016届河北省冀州市高三复习班上第一次月考化学试卷A(解析版) 题型:选择题
下列有关物质的性质和该性质的应用均正确的是
A.晶体硅具有半导体性质,可用于生产光导纤维
B.H2O2是一种绿色氧化剂,可与酸性高锰酸钾作用产生O2
C.铜的金属活动性比铁弱,可用铜罐代替铁罐贮运浓硝酸
D.铝具有良好的导电性,钢抗拉强度大,钢芯铝绞线可用作远距离高压输电线材料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com