
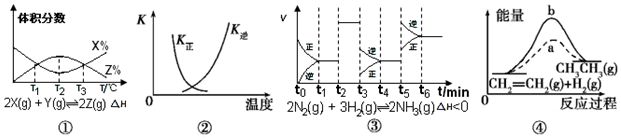
| A. | 由图①知,反应在T1、T3处达到平衡,且该反应的△H<0 | |
| B. | 图②中曲线表示反应2SO2(g)+O2(g)?2SO3(g),△H<0正、逆反应的平衡常数K随温度的变化 | |
| C. | 由图③知,反应在t6时,NH3体积分数最大,t3时采取降低反应温度的措施 | |
| D. | 图④中a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g)△H<0使用和未使用催化剂时,反应过程中的能量变化 |
分析 A、反应物和生成物的体积分数相同时,反应不一定达到平衡状态,升高温度平衡向吸热反应方向移动;
B、该反应为放热反应,温度升高,平衡向着逆向移动,K(逆)增大、K(正)减小;
C、t1时刻正逆反应速率相等,反应达到平衡状态;t2时刻正逆反应速率都增大且相等,改变的条件是加入催化剂;t3时刻正逆反应速率都减小,且逆反应速率大于正反应速率,改变的条件是减小压强;t5时刻正逆反应速率都增大,且逆反应速率大于正反应速率,改变的条件是升高温度;
D、图象中使用催化剂降低反应活化能,但反应是放热反应,反应物能量高.
解答 解:A、由图Ⅰ知,反应在T1、T3处反应物和生成物的体积分数相对但反应不一定达到平衡,T2-T3升高温度,反应物体积分数增大,生成物体积分数减小,平衡向逆反应方向移动,所以正反应是放热反应,△H<0,故A错误;
B、因反应为放热反应,则升高温度,平衡逆向移动,平衡后升温K(逆)会增大,而K(正)会减小,图象中变化与实际上的变化相符,故B正确;
C、由图Ⅱ知,t2时刻正逆反应速率都增大且相等,改变的条件是加入催化剂,平衡不移动;t3时刻正逆反应速率都减小,且逆反应速率大于正反应速率,改变的条件是减小压强,平衡向逆反应方向移动;t5时刻正逆反应速率都增大,且逆反应速率大于正反应速率,改变的条件是升高温度,平衡向逆反应方向移动,所以反应在t1时,NH3体积分数最大,故C错误;
D、图象中使用催化剂降低反应活化能,但反应是放热反应,反应物能量高,图象中表示的吸热反应,故D错误;
故选B.
点评 本题考查了化学反应能量变化,影响平衡因素的分析判断,图象分析方法和平衡移动原理的判断依据是解题关键,题目难度中等.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发操作时,应使混合物中的水分大部分蒸干后,停止加热,利用余热蒸干 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 浓硫酸稀释时,应该将水缓缓加入盛浓硫酸的烧杯中,边加边搅拌 | |
| D. | 萃取分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
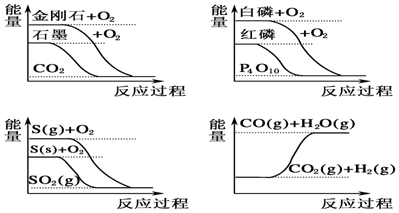
| A. | CO(g)+H2O(g)═CO2(g)+H2(g)△H>0 | |
| B. | S(g)+O2(g)═SO2(g)△H1,S(s)+O2(g)═SO2(g)△H2,则△H1>△H2 | |
| C. | 白磷比红磷稳定 | |
| D. | 石墨转变为金刚石是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
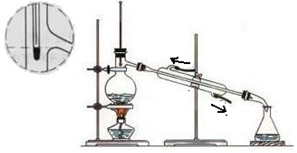
| A. | 冷凝水的进出口方向正确 | B. | 应选用20 mL的蒸馏烧瓶 | ||
| C. | 温度计液泡应插在混合液中 | D. | 锥形瓶中收集到的是甲苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol/L的(NH4)2SO4溶液:c(SO42-)>c(NH4+)>c(H+)>c(OH-) | |
| B. | 0.1 mol/L的NaHCO3溶液:c(Na+)=c(HCO3-)+c(H2CO3)+2c(CO32-) | |
| C. | 将0.2 mol/L NaA溶液和0.1 mol/L盐酸等体积混合所得溶液:c(Na+)+c(H+)=c(A-)+c(Cl-) | |
| D. | 0.02mol/L CH3COOH溶液和0.01 mol/L NaOH溶液等体积混合所得溶液:2c(H+)+c(CH3COOH)=c(CH3COO-)+2c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+ 1s22s22p63s2 | B. | F 1s22s22p5 | ||
| C. | O2- 1s22s22p6 | D. | Ar 1s22s22p63s23p6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 +
+ →
→ +H2O.
+H2O.| A. | 1molCPAE和1mol咖啡酸分别与足量的NaOH溶液反应,均最多消耗3molNaOH | |
| B. | 与苯乙醇互为同分异构体的酚类物质共有9种 | |
| C. | FeCl3溶液可区别咖啡酸和CPAE | |
| D. | 咖啡酸可发生聚合反应,并且其分子中含有3种官能团 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在受热条件下,HD能还原氧化铜 | |
| B. | HD能在氯气中燃烧生成HCl和DCl气体 | |
| C. | 是一种非金属单质 | |
| D. | 是一种化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com