
【题目】石油分馏的原理是利用物质的( )
A. 沸点差异 B. 密度差异 C. 溶解度差异 D. 化学性质差异
科目:高中化学 来源: 题型:
【题目】a、b、c、d、e、f是前四周期原子序数依次增大的6种元素,a元素的基态原子核外s能级上的电子数是p能级上电子数的2倍;c元素原子的最外层电子数是次外层电子数的3倍;d是地壳中含量最高的金属元素;e的正三价基态离子的d能级为半充满结构;f的基态原子最外层只有一个电子,且内层电子排布均为全充满结构。
(1)b元素基态原子的价电子排布图为________。
(2)a、b、c三种元素的第一电离能由大到小的顺序为_________。(用元素符号回答)
(3)b与c组成的一种分子甲中有16个价电子,甲分子与______(填写一种物质的分子式)是等电子体,甲分子中σ键和π键的数目比是______。
(4)c的氢化物中,电子总数为18的分子是乙,乙中c原子的杂化方式为_______。它是______分子(填“极性”或“非极性”)
(5)已知c、f能形成两种化合物,其晶胞如图所示,甲的化学式为_________。高温时,甲易转化为乙的原因为_________。

(6)e元素对应的单质在形成晶体时,采用如图所示的堆积方式_________。则这种堆积模型的配位数为,如果e的原子半径为 r pm;阿伏伽德罗常数的值为NA,计算此单质的密度表达式为_______g/cm3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是 ( )
①钠在空气中燃烧生成白色的氧化钠
②钠投入硫酸铜溶液中有红色粉末产生
③过氧化钠可在防毒面具中做供氧剂
④铁丝在氯气中燃烧生成红棕色的
A. ①② B. ②③ C. ③④ D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.2017年08月08日21时19分46秒在四川阿坝州九寨沟县发生7级地震。地震后,为防止疫病流行,全国各地向灾区运送了大量的消毒剂、漂白剂等。请回答下列相关问题:
(1)次氯酸盐是一些漂白剂和消毒剂的有效成分。84消毒液的有效成分是次氯酸钠,制取该消毒液的化学方程式为_______。
(2)二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3溶液在一定条件下与SO2反应制得。该反应的离子方程式为:_______。
(3)漂白剂亚氯酸钠(NaClO2)在常温黑暗处可保存一年,但亚氯酸不稳定可分解,反应的离子方程式为:HClO2→ClO2↑+H++Cl-+H2O(未配平)。
当1 molHClO2发生分解反应时,转移电子的物质的量是_________mo1。
Ⅱ.溴及其化合物广泛应用在有机合成、化学分析等领域。
(4)海水提溴过程中溴元素的变化如下:
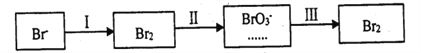
①过程Ⅰ,海水显碱性,调其pH<3.5后,再通入氯气。调海水PH可提高Cl2的利用率.用平衡原理解释其原因是______________。
②过程Ⅱ,用热空气将溴赶出,再用浓碳酸钠溶液吸收。完成并配平下列方程式。
_____Br2+_______Na2CO3 =______NaBrO3+_____CO2+____。
(5)NaBrO3是一种分析试剂。向硫酸酸化的NaI溶液中逐滴加入NaBrO3溶液,当加入2.6 mol NaBrO3时,测得反应后溶液中溴和碘的存在形式及物质的量分别为:
粒子 | I2 | Br2 | IO3- |
物质的量/mol | 0.5 | 1.3 |
则原溶液中NaI的物质的量是_______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中A与B反应生成C,其反应速率分别用v(A)、v(B)、v(C)表示。已知v(A)、v(B)、v(C)之间有以下关系:2v(A)=3v(B),v(C)=2v(B),则此反应可表示为( )
A. 3A+2B=4C B. 2A+3B=6C C. 3A+2B=C D. 2A+3B=4C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)原子序数为24的元素原子中有___________个电子层,___________个能级,_________个未成对电子,位于元素周期表的___________区。
(2)在下列物质中:①N2、②H2O、③NaOH、④MgCl2、⑤C2H4、⑥Na2O2(用序号填空)
其中只含有非极性键的是___________;只含有极性键的是___________;只含有离子键的是___________;既含有非极性键又含有极性键的是___________;含有非极性键的离子化合物是___________。
(3)N≡N的键能为942kJ·mol-1,N—N单键的键能为247kJ·mol-1,通过计算说明N2中的___________键更稳定(填“σ”或“π”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以软锰矿(主要成分为MnO2)和硫锰矿(主要成分为MnS)为原料(已知两种原料中均不含有单质杂质)制备高纯度硫酸锰的工艺流程如图所示。
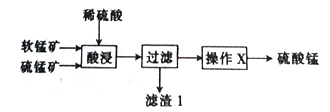
(1)已知滤渣1中含有一种非金属单质,该非金属单质的化学式为_____________________。
(2)已知二氧化锰与硫化锰的物质的量之比对酸浸时的浸出率有影响,相关实验数据如下表所示。当二氧化锰与硫化锰的物质的量之比为______________时,为最优反应配比。
号 | 二氧化锰与硫化锰的物质的量之比 | 浸出液的pH | 浸出率% |
1 | 1.25:1 | 2.5 | 95.30 |
2 | 1.75:1 | 2.5 | 97.11 |
3 | 2.25:1 | 2.5 | 99.00 |
4 | 2.5:1 | 2.5 | 98.40 |
(3)操作X为蒸发浓缩、______________、过滤,洗涤、烘干,在洗涤操作中,常用酒精洗涤MnSO4·H2O晶体,其主要目的是_________。
(4)现有10t锰矿,其中MnO2和MnS的含量均为29%,若流程中Mn的损耗率为10%,则最终制得硫酸锰(MnSO4·H2O)_________t。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com