
ijͬѧ��0.10 mol/L��HCl��Һ�ⶨδ֪Ũ�ȵ�NaOH��Һ����ʵ��������£�
| A������ʽ�ζ�����ȡ20.00mLHCl��Һע����ƿ��ͬʱ�μ�2-3�η�̪��Һ�� |
| B����0.10 mol/L��HCl��Һ��ϴ��ʽ�ζ��ܣ� |
| C���ѵζ���������ˮϴ���� |
| D��ȡ�¼�ʽ�ζ��ܣ��ô���NaOH��Һ��ϴ������NaOH��Һע���ʽ�ζ���������̶ȡ�0������2��3cm�����ٰѼ�ʽ�ζ��̶ܹ��ã�����Һ�棻 |

��1�� E  C
C D
D B
B A
A  G
G  F (˳�����һ�����÷֡�2��)
F (˳�����һ�����÷֡�2��)
��2�����ڹ۲���ƿ��ָʾ����ɫ�ı仯(����2��)
��3����0���̶Ȼ�0���̶����£�(����2��) ������Һ(��2��)
��4��ƫ�� ��ƫС����1�֣�
��5���ڢۢ�(����2��)
���������������1���к͵ζ����ռ�©��ϴ�ӡ���ϴ��װҺ��ȡ����Һ����ָʾ�����ζ���˳��������ʴ�Ϊ��E��C��D��B��A��G��F���ʴ�Ϊ��E��D��A��G��F����2������ƿ�µ�һ�Ű�ֽʹ�ζ��յ���ɫ�仯�����ԣ����ڷֱ棬�ʴ�Ϊ��ʹ�ζ��յ���ɫ�仯�����ԣ����ڷֱ棻��3��װҺ��Һ��Ӧ���ڵ���0���̶Ȼ�0���̶����£����첿��Ӧ������Һ���ʴ�Ϊ����0���̶Ȼ�0���̶����£�������Һ����4���ζ��յ����ʱ���������Һ�棬��������ֵƫ�����ζ�ǰƽ�Ӷ����������V���꣩ƫ����c���= 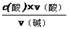 ����֪c���ƫ��5����Ͳû����̶ȣ��¶ȼ���̶����м䣬�ζ�����̶����Ϸ���
����֪c���ƫ��5����Ͳû����̶ȣ��¶ȼ���̶����м䣬�ζ�����̶����Ϸ���
���㣺�к͵ζ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����ʵ���Ũ�ȵ�����������Һ�У� Ũ�������ǣ� ��
Ũ�������ǣ� ��
| A��NH4Cl | B��NH4HCO3 | C��NH4NO3 | D��NH4HSO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������Һ�и�����Ũ�ȹ�ϵ��ȷ����
| A�����ʵ���Ũ����ȵĢ�(NH4)2CO3��(NH4)2SO4��(NH4)2Fe(SO4)2������Һ�� c (NH4+)�Ĵ�С˳��Ϊ����>��>�� |
| B��pH��ȵ�NaF��CH3COOK��Һ��c(Na��)��c(F ��)>c(K��)��c(CH3COO��) |
| C��0.2 mo1��L ��1��Na2CO3��Һ��c(OH��)��c(HCO3��)��c(H+)��2c(H2CO3) |
| D��0.2 mo1��L ��1 HCl��0.1 mo1��L ��1 NaAlO2��Һ�������ϣ�c(Cl��)> c(Na+)>c(Al3��)>c(H��)>c(OH��) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�ñ�����ζ�δ֪Ũ�ȵ�NaOH��Һ�����и������У���������ʵ��������
| A��������ˮ�����ζ��ܺ�װ���������еζ� |
| B��������ˮ������ƿ������NaOHҺ��ϴ������װ��һ�������NaOH��Һ |
| C���ü�����ָʾ��������Һ�ɻ�ɫ��ɳ�ɫ�����̶������������ |
| D���ü�ʽ�ζ���ȡ10.00 mLNaOH��Һ����������ˮϴ������ƿ�У��ټ�����������ˮ���еζ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����£������ʵ���Ũ�ȵ���������ҺNaX��NaY��NaZ������Һ��pH����Ϊ7��8��9�������й�˵����ȷ����( )
| A��HX��HY��HZ�������������ǿ������˳��ΪHZ��HY��HX |
| B��HX��ǿ�ᣬHY��HZ�����ᣬ��HY������ǿ��HZ |
| C��X-��Y-��Z-�����������ˮ�⣬��ˮ��̶�Z-��Y-��X- |
| D����������Һ��X-��Y-��Z-��Ũ�ȴ�С˳��Ϊc(Z-)��c(Y-)��c(X-) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����£���0.10mol/L������ζ�20.00mL 0.10mol/L��ij��BOH��Һ�õ��ĵζ��������£������жϲ���ȷ����( )
| A��a��ʱ����Һ�ʼ��ԣ���Һ��c(B+)>c(Cl-) |
| B��b��ʱ��Һ��pH=7 |
| C����c(Cl-)=c(B+)ʱ��V(HCl)<20mL |
| D��C��ʱ��Һ��c(H+)ԼΪ0.03mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
25�棬��ˮϡ��10mLpH=11�İ�ˮ�������ж���ȷ����
| A��ԭ��ˮ��Ũ��=10��3mol /L |
| B����ˮ�ĵ���̶�������Һ���������ӵ�Ũ�Ⱦ���С |
C����Һ�� ������ ������ |
| D���ټ���10mLpH=3�����ᣬ���ҺpH=7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���Ȼ�粒����ܽ���D2O����ˮ���У���Ӧ�����ӷ���ʽ��ȷ����
A��NH4+ + D2O  NH3��D2O + H+ NH3��D2O + H+ | B��NH4+ + D2O  NH3��HDO + D+ NH3��HDO + D+ |
C��NH4+ + 2D2O  NH3��HDO + D3O+ NH3��HDO + D3O+ | D��NH4+ + 2D2O  NH3��D2O + HD2O+ NH3��D2O + HD2O+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
ij��Һ��ֻ����Na+��H+��OH-��A-�������ӣ�����˵����ȷ����
A������Һ��c��A-����c��Na+��������Һһ��������
B����Һ�в����ܴ��ڣ�c��Na+��> c��A-��> c��OH-��> c��H+��
C����c��OH-��> c��H+������Һ�в����ܴ��ڣ�c��Na+��> c��OH-��> c��A-��> c��H+��
D��������ΪNaA��HA����һ�����ڣ�c��A-��> c��Na+��> c��H+��> c��OH-��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com