
【题目】下列关于常温下的溶液叙述正确的是
A.Mg(OH)2可溶于一定浓度的NH4Cl溶液
B.两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为u和u+1,则c1=10c2
C.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈蓝色
D.将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO![]() )>c(NH
)>c(NH![]() )
)
【答案】A
【解析】
试题分析:A.因为浓的NH4Cl溶液电离出铵根离子,结合氢氧化镁溶解时产生的氢氧根,从而促进氢氧化镁的溶解平衡向溶解方向移动,所以Mg(OH)2难溶于水,但可缓慢溶于浓的NH4Cl溶液,故A正确;B.对于pH分别为u和u+1强酸,则其物质的量浓度满足则c1=10c2,而醋酸为弱电解质,浓度越大,醋酸的电离程度越小,所以两种醋酸溶液的物质的量浓度分别为c1和c2,pH的别为u和u+1,则c1>10c2,故B错误;C.常温下,pH=11的NaOH溶液浓度与pH=3的盐酸溶液浓度相等,等体积混合,二者恰好反应生成强酸强碱盐氯化钠,溶液呈中性,滴入紫色石蕊试液溶液不变色,故C错误;D.混合溶液呈中性,则c(OH-)>c(H+),根据电荷守恒得2c(SO42-)=c(NH4+),所以c(SO42-)<c(NH4+),故D错误;答案为A。


科目:高中化学 来源: 题型:
【题目】向仅含Fe2+、I-、Br-的溶液中通入适量氯气,溶液中这三种离子的物质的量随消耗氯气物质的量的变化如图所示.下列说法中不正确的是( )

A. 线段Ⅲ代表Br-的变化情况
B. a值等于8
C. 线段I代表I-的变化情况
D. 原混合溶液中n(Fe2+)=4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,水溶液中H+和OH-的浓度变化曲线如图,下列说法正确的是( )

A. 升高温度,可能引起有c向b的变化
B. 该温度下,水的离子积常数为1.0×10-13
C. 该温度下,稀释溶液可能引起由c向d的变化
D. 该温度下,加入FeCl3可能引起由b向a的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A.NaOH+HCl=NaCl+H2O;B.Zn+H2SO4=ZnSO4+H2↑上述反应中能设计成原电池的是______。
(2)将纯锌片和纯铜片按图方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:

①下列说法正确的是____________。
A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲_______乙(填“>”、“<“或“=” )
③请写出图中构成原电池的负极电极反应式_________________________。
④当乙中产生1.12L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.1 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为____________________。
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,氢气为燃料,采用氢氧化钠溶液为电解液;则氢气应通入_____________极(填a或b),电子从 __________(填a或b)极流出。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的方程式不正确的是
A. 空气中加热钠生成淡黄色固体:2Na +O2![]() Na2O2
Na2O2
B. 铁与水蒸气反应生成黑色固体:3Fe +4H2O(g) ![]() Fe3O4 +4H2
Fe3O4 +4H2
C. 除去乙炔中的H2S气体:H2S +Cu2+= CuS↓+2H+
D. 实验室制备氨气:NH4 Cl![]() NH3↑+HCl↑
NH3↑+HCl↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是模拟电化学反应装置图。下列说法正确的是( )

A.开关K置于N处,则铁电极的电极反应式为:Fe-2e-=Fe2+
B.开关K置于N处,可以减缓铁的腐蚀
C.开关K置于M处,则铁电极的电极反应式为: 2Cl--2e-=Cl2↑
D.开关K置于M处,电子从碳棒经开关K流向铁棒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是
A. 蒸馏实验时,应将温度计水银球置于蒸馏烧瓶支管口处
B. 蒸馏实验时,冷水从冷凝管下口入,上口出
C. 萃取使用的主要仪器是分液漏斗,在使用前要先检验其是否漏液
D. 萃取实验时,应先后将上下两层液体从下口放出,并用不同烧杯盛放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组欲利用CuO与NH3反应,研究NH3的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题:
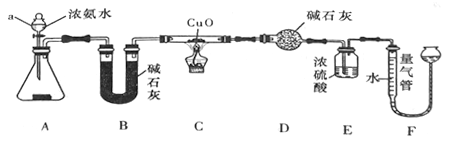
(1)仪器a的名称为______________。
(2)实验中观察到装置C中黑色CuO粉末变为红色固体,最气管中有无色无味的气体产生。上述现象证明NH3 具有______性,写出相应的化学方程式:______________。
(3)E装置中浓硫酸的作用是______________。
(4)实验完毕,若测得干燥管D增重mg,装置F测得气体的体积为VL(已折算成标准状况),则氨分子中氮、氢的原子个数比值为_____(用含m、V字母的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com