
【题目】下列各图均能表示甲烷的分子结构,按要求回答下列问题。
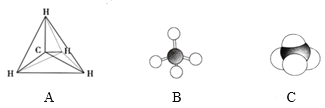
(1)甲烷的比例模型是______(填序号)。
(2)相对分子质量为100的烷烃的分子式是_____。
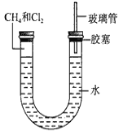
(3)甲烷与氯气的体积比为1:1,光照条件下在如图所示的装置中反应,则得到的产物为_____。
A.CH3Cl、HCl B.CCl4、HCl
C.CH3Cl、CH2Cl2 D.CH3Cl、CH2Cl2、CHCl3、CCl4、HCl
(4)甲烷最简单的同系物与氯气光照条件下反应,其生成物的化学式最多可能有_____种。
A.5 B.9 C.10 D.7
(5)经过几个小时的反应后,U形管右端的水柱变化是______。
A.升高 B.降低 C.不变 D.无法确定
(6)工业酒精含有甲醇,其结构简式为:CH3OH,可由甲烷经过一系列变化得到,写出甲醇与O2在铜作催化剂加热条件下的反应_______。
【答案】C C7H16 D D B 2CH3OH+O2![]() 2HCHO+2H2O
2HCHO+2H2O
【解析】
(1)比例模型能反应原子体积大小;
(2)根据烷烃分子通式计算其分子式;
(3)甲烷和氯气在光照条件下发生取代反应,甲烷的取代反应为逐步取代,但是多步取代反应是同时进行的,据此进行判断;
(4)甲烷最简单的同系物为乙烷,与氯气发生多步取代反应;
(5)根据大气压强原理来判断U型管右端的玻璃管中水柱变化;
(6)甲醇催化氧化得到甲醛。
(1)甲烷的比例模型是 ,故答案选C;
,故答案选C;
(2)烷烃的分子通式为:CnH2n+2,相对分子质量为100,则12n+(2n+2)=100,解得n=7,故该烷烃的分子式是C7H16;
(3)甲烷和氯气在光照条件下发生逐步取代反应,但是多步取代反应是同时进行且各步反应都是可逆反应,所有得到的产物与甲烷与氯气的物质的量之比无关,故得到的产物为CH3Cl、CH2Cl2、CHCl3、CCl4、HCl,D项正确;
答案选D;
(4)甲烷最简单的同系物乙烷与氯气发生多步取代反应,得到的生成物的化学式可以为:C2H5Cl、C2H4Cl2、C2H3Cl3、C2H2Cl4、C2HCl5、C2Cl6和HCl共7种,故D项正确,
答案选D;
(5)经过几个小时的反应后,消耗氯气, U型管左端气体的物质的量减少,生成的HCl极易溶于水,所以压强减小,U型管右端的玻璃管中水柱降低;
故答案为:B;
(6)甲醇与O2在铜作催化剂加热条件下发生反应生成甲醛与水,其化学方程式为:2CH3OH+O2![]() 2HCHO+2H2O。
2HCHO+2H2O。


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】甲醇水蒸气重整制氢(SRM)是用于驱动电动汽车的质子交换膜燃料电池的理想氢源,当前研究主要集中在提高催化剂活性和降低尾气中CO含量,以免使燃料电池Pt电极中毒。重整过程发生的反应如下:
反应I CH3OH(g)+H2O(g)![]() CO2(g)+3H2(g) ΔH1
CO2(g)+3H2(g) ΔH1
反应Ⅱ CH3OH(g)![]() CO(g)+2H2(g) ΔH2
CO(g)+2H2(g) ΔH2
反应Ⅲ CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH3
CO2(g)+H2(g) ΔH3
其对应的平衡常数分别为K1、K2、K3,其中K2、K3随温度变化如下表所示:
125℃ | 225℃ | 325℃ | |
K2 | 05535 | 1858 | 9939.5 |
K3 | 1577 | 137.5 | 28.14 |
请回答:
(1)反应Ⅱ能够自发进行的条件_______(填“低温”、“高温”或“任何温度”),ΔH1____ΔH3(填“>”、“<”或“=”)。
(2)相同条件下,甲醇水蒸气重整制氢较甲醇直接分解制氢(反应Ⅱ)的先进之处在于___________________________________________________________________。
(3)在常压、Cat.1催化下,CH3OH和H2O混和气体(体积比1∶1.2,总物质的量2.2mol)进行反应,tl时刻测得CH3OH转化率及CO、CO2选择性随温度变化情况分别如图所示(CO、CO2的选择性:转化的CH3OH中生成CO、CO2的百分比)。

注:曲线a表示CH3OH的转化率,曲线b表示CO的选择性,曲线c表示CO2的选择性
① 下列说法不正确的是__________。
A.反应适宜温度为300℃
B.工业生产通常在负压条件下进行甲醇水蒸气重整
C.己知Cat.2催化剂具有更高催化活性,可提高甲醇平衡转化率
D.添加CaO的复合催化剂可提高氢气产率
② 260℃时H2物质的量随时间的变化曲线如图所示。画出300℃时至t1时刻H2物质的量随时间的变化曲线。________________

(4)副产物CO2可以在酸性水溶液中电解生成甲酸,生成甲酸的电极反应式是:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下图所示的物质转化关系中,A是常见的气态氢化物,B是能使带火星的木条复燃的无色无味气体,E的相对分子质量比D大17,G是一种紫红色金属单质。(部分反应中生成物没有全部列出,反应条件未列出)

请回答下列问题:
(1)A的化学式为_____。B的化学式为________。
(2)反应①的化学方程式为_________。
(3)反应②的离子方程式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】流动电池是一种新型电池。其主要特点是可以通过电解质溶液的循环流动,在电池外部调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定。北京化工大学新开发的一种流动电池如图所示,电池总反应为Cu+PbO2+2H2SO4=CuSO4+PbSO4+2H2O。下列说法不正确的是
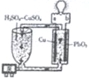
A.a为负极,b为正极
B.该电池工作时PbO2电极附近溶液的pH增大
C.a极的电极反应为Cu-2e-=Cu2+
D.调节电解质溶液的方法是补充CuSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种气体的摩尔质量为M g·mol-1,将标况下的该气体V L溶解在1000 g水中,该气体不与水反应,所得溶液密度为ρ g·cm-3,则所得溶液中溶质的物质的量浓度为 ( )mol·L-1
A.V/22.4B.V ρ/(MV+22400)
C.V ρ/22400D.1000V ρ/(MV+22400)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.实验室需要配制0.1 mol·L-1NaOH溶液500mL。
(1)根据计算用托盘天平称取的质量为__________g。在下图所示仪器中,配制上述溶液肯定不需要的是_________(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是________。
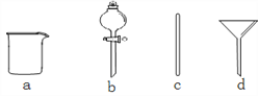
(2)配制时,其正确的操作顺序是(用字母表示,每个操作只用一次)__________。
A.用少量水洗涤烧杯2次~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1 cm~2 cm处
(3)下面操作造成所配NaOH溶液浓度偏高的是_____。
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
II.向浓度相等、体积均为100 mL的A、B两份NaOH溶液中,分别通入一定量的CO2后,再向所得溶液中滴加0.1 mol/L盐酸,产生CO2的体积(标准状况)与所加盐酸的体积关系如图所示。
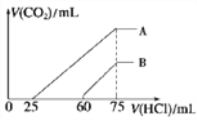
(4)①A曲线表明,原溶液通入CO2后,所得溶质与盐酸反应产生CO2的最大体积是________mL(标准状况)。
②B曲线表明,原溶液通入CO2后,所得溶液中溶质的化学式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生的实验报告所列出的下列数据中合理的是( )
A.用10mL量筒量取7.13mL稀盐酸
B.用pH计测得某稀盐酸的pH为1.54
C.用广泛pH试纸测得某溶液的pH为2.3
D.配制100mL1mol/L的NaCl溶液用托盘天平称取5.85gNaCl固体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com