
【题目】黄铜矿(主要成分为CuFeS2)是海洋矿物中的一种,它是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。请回答下列问题:
(1) 利用黄铜矿冶炼铜的反应为8CuFeS2+21O2![]() 8Cu+4FeO+2Fe2O3+16SO2。已知CuFeS2中Fe的化合价为+2,Cu的化合价为+2,
8Cu+4FeO+2Fe2O3+16SO2。已知CuFeS2中Fe的化合价为+2,Cu的化合价为+2,
① 反应中被还原的元素是________(填元素符号),
② 生成1 mol Fe2O3时转移电子的物质的量为________mol。
(2)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3,方法为:①用过量稀盐酸浸取炉渣,过滤。②先将滤液氧化,再向其中加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。据以上信息回答下列问题:
A.①中过滤的目的是____________________,
B.②中将滤液氧化常常选用H2O2,其反应的离子方程式为____________________。
C.只能选用提供的试剂,设计实验验证炉渣中含有FeO。提供的试剂:稀盐酸、稀硫酸、KSCN溶液、KMnO4溶液、NaOH溶液、碘水,
① 所选试剂为___________________
② 证明炉渣中含有FeO的实验现象为_____________________
【答案】 Cu、O 50 除去SiO2 H2O2+2Fe2++2H+===2Fe3++2H2O 稀硫酸、KMnO4溶液 稀硫酸浸取炉渣所得的溶液使KMnO4溶液褪色
【解析】(1)考查氧化还原反应中几组概念、转移电子物质的量计算,①氧化剂化合价降低,被还原,根据反应方程式,Cu和O2的化合价降低,因此被还原的元素为Cu和O;②根据反应生成方程式,生成2molFe2O3转移电子物质的量为100mol,因此生成1molFe2O3,转移电子物质的量为50mol;(2)考查实验方案设计与评价,A、炉渣的成分中,氧化铁、氧化亚铁为碱性氧化物,氧化铝为两性氧化物,都能与稀盐酸反应,SiO2为酸性氧化物,不与稀盐酸反应,因此过滤的目的是除去SiO2;B、利用H2O2的强氧化性,把Fe2+氧化成Fe3+,其离子反应方程式为H2O2+2Fe2++2H+=2Fe3++2H2O;C、检验滤渣中含有FeO,首先溶解FeO,需要加入盐酸或稀硫酸,利用Fe2+的还原性,因此需要加入高锰酸钾溶液,如果高锰酸钾溶液褪色,说明炉渣中含有FeO,因为酸性高锰酸钾能氧化HCl,因此需要的酸是稀硫酸,即所选试剂为稀硫酸和高锰酸钾溶液;②根据①的分析,实验现象是稀硫酸浸取炉渣所得的溶液使KMnO4溶液褪色。


科目:高中化学 来源: 题型:
【题目】下列正确的是( )
A.碳酸的电离:H2CO3?H++HCO ![]()
B.硫化钠水解:S2﹣+2H2O?H2S↑+2OH﹣
C.Na2CO3溶液中:c(HCO ![]() )>c(OH﹣)
)>c(OH﹣)
D.NH4Cl溶液中,c(NH ![]() )>c(Cl﹣)
)>c(Cl﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷化硼是一种超硬耐磨涂层材料.如图为其晶体结构中最小的重复结构单元,其中的每个原子均满足8电子稳定结构.下列有关说法正确的是( ) 
A.磷化硼晶体的化学式为BP,属于离子晶体
B.磷化硼晶体的熔点高,且熔融状态下能导电
C.磷化硼晶体中每个原子均形成4条共价键
D.磷化硼晶体结构微粒的空间堆积方式与氯化钠相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随lg ![]() 的变化如图所示,下列叙述错误的是( )
的变化如图所示,下列叙述错误的是( ) 
A.MOH的碱性强于ROH的碱性
B.ROH的电离程度:b点大于a点
C.若两溶液无限稀释,则它们的c(OH﹣)相等
D.当lg ![]() =2时,若两溶液同时升高温度,则
=2时,若两溶液同时升高温度,则 ![]() 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚.其反应原理如下:电池:Pb(s)+PbO2(s)+2H2SO4(aq)=2PbSO4(s)+2H2O(l);电解池:2Al+3H2O ![]() Al2O3+3H2↑,电解过程中,以下判断正确的是( )
Al2O3+3H2↑,电解过程中,以下判断正确的是( )
电池 | 电解池 | |
A | H+移向Pb电极 | H+移向Pb电极 |
B | 每消耗3molPb | 生成2molAl2O3 |
C | 正极:PbO2+4H++2e﹣=Pb2++2H2O | 阳极:2Al+3H2O﹣6e﹣=Al2O3+6H+ |
D |
|
|
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25%的酒精密度为0.96 g·cm-3,5%的酒精密度为0.99 g·cm-3。若将上述两溶液等体积混合,所得酒精溶液的质量分数是 ( )
A. 等于15% B. 大于15%
C. 小于15% D. 无法估算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于胶体和溶液的叙述中正确的是
A. 胶体带电荷,而溶液呈电中性
B. 胶体粒子的直径大小在1-100纳米之间
C. 胶体加入电解质可产生沉淀,而溶液不能
D. 从颜色上无法区别FeCl3溶液和Fe((OH)3胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是电解CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )
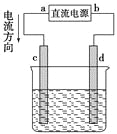
A. a为负极,b为正极
B. a为阳极,b为阴极
C. 电解过程中,d电极质量增加
D. 电解过程中,氯离子浓度不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com