
【题目】科学家提出“绿色自由”构想,把空气中的CO2转化为可再生能源甲醇(CH3OH).该反应的热化学方程式为:CO(g)+2H2(g)→CH3OH(g)+H2O(g)△H
(1)若在一个定温定容的容器中发生上述反应,反应达到平衡的标志是 .
A.CO2和CH3OH的浓度相等
B.H2的百分含量保持不变
C.容器内压强保持不变
D.3v正(H2)=v逆(H2O)
E.容器中混合气体的密度保持不变
(2)若将CO2和H2的混合气体分成五等份,将它们分别充入温度不同、容积相同的恒容容器中发生上述反应.反应相同时间后,测得甲醇的体积分数 (CH3OH)与反应温度T的关系如图1,则上述CO2转化为甲醇的反应的△H0(填“>”、“<”、“=”) 
(3)上述反应在实际生产中采用的温度是300℃,其目的是 .
(4)300℃时,将CO2与H2按1:3的体积比充入某密闭容器中,CO2的平衡转化率(a)与体系总压强(P)的关系如图2所示.回答问题: ①若其他条件不变,将A点的体积压缩至原来的一半,一段时间后反应再次达到平衡,与原平衡相比较下列说法正确的是 .
A.CO2的浓度减小
B.正反应速率增大,逆反应速率减小
C.CO2和H2的体积比仍然是1:3
D.H2的体积分数减小②B点平衡混合气体的平均摩尔质量为 22.7g/mol (保留一位小数).
【答案】
(1)BC
(2)<
(3)加快反应速率,使催化剂活性较高
(4)CD
【解析】解:(1)A.CO2和CH3OH的浓度相等,并不是不变,所以不能说明达平衡状态,故错误;
B.H2的百分含量保持不变,说明各物质的量不变,反应达平衡状态,故正确;
C.容器内压强保持不变,说明气体的总物质的量不变,反应达平衡状态,故正确;
D.达平衡时应有:v正(H2)=3v逆(H2O),故错误;
E.容器中混合气体的密度一直保持不变,故错误;
故选:BC;(2)由图可知最高点反应到达平衡,达平衡后,温度越高,φ(CH3OH)越小,平衡向逆反应进行,升高温度平衡吸热方向进行,逆反应为吸热反应,则正反应为放热反应,即△H<0,
所以答案是:<;(3)采用300℃的温度,可以加快反应速率,且催化剂活性较高,
所以答案是:加快反应速率,使催化剂活性较高;(4)①A.体积压缩,反应混合物各组分浓度均增大,故A错误;
B.体积压缩,压强增大,正、逆反应速率都增大,故B错误;
C.CO和H2按1:3的体积比投入,且二者按物质的量1:3反应,反应体系中CO2和H2的体积比始终为1:3,故C正确;
D.压缩体积,增大压强,平衡正向移动,H2的体积分数减小,故D正确,
故选:CD;
②由CO2与H2按1:3的体积比,设二氧化碳的物质的量为1mol,则氢气的物质的量为3mol,而平衡时CO2的平衡转化率90%,
CO2(g)+ | 3H2(g)→ | CH3OH(g)+ | H2O(g) | |
起始(mol) | 1 | 3 | 0 | 0 |
转化(mol) | 0.9 | 2.7 | 0.9 | 0.9 |
平衡(mol) | 0.1 | 0.3 | 0.9 | 0.9 |
所以B点平衡混合气体的平均摩尔质量为: ![]() =22.7g/mol,所以答案是:22.7g/mol.
=22.7g/mol,所以答案是:22.7g/mol.
【考点精析】本题主要考查了化学平衡状态本质及特征和化学平衡状态的判断的相关知识点,需要掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效);状态判断:①v(B耗)=v(B生)②v(C耗):v(D生)=x : y③c(C)、C%、n(C)%等不变④若A、B、C、D为气体,且m+n≠x+y,压强恒定⑤体系颜色不变⑥单位时间内某物质内化学键的断裂量等于形成量⑦体系平均式量恒定(m+n ≠ x+y)等才能正确解答此题.


科目:高中化学 来源: 题型:
【题目】乙烯的产量可用来衡量一个国家的石油化工发展水平。下列关于乙烯的说法正确的是
A.与苯互为同分异构体
B.分子中存在碳碳双键
C.能使溴的四氯化碳溶液褪色
D.能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在15mL0.1molL﹣1KOH溶液中逐滴加入0.2molL﹣1甲酸溶液,溶液pH和加入甲酸(弱酸)的体积关系曲线如图所示,下列关系正确的是( ) 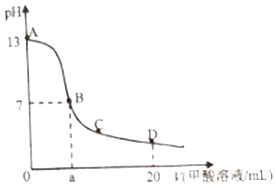
A.在B点:c(K+)=c(HCOO﹣)>c(OH﹣)=c(H+),且a=7.5
B.在A,B间任意一点,c(HCOO﹣)>c(K+)>c(OH﹣)>c(H+)
C.在D点:c(HCOO﹣)+c(HCOOH)>2c(K+)
D.B→C段:水的电离程度先增大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液体感科电池相比于气体燃料电池具有体积小,无需气体存储装置等优点。一种以肼(N2H4)为燃料的电池装置如图所示。该电池用空气中的氧气作为氧化剂,KOH为电解质。下列关于该燃料电池的叙述不正确的是

A. 电流从右侧电极经过负载流向左侧电极
B. 负极发生的电极反应式为N2H4+4OH--4e-=N2+4H2O
C. 该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触
D. 该燃料电池持续放电时,正极发生氧化反应,碱性减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从冬青中提取出的有机物A可用合合成抗结肠炎药物Y及其他化学品,合成路线如图:
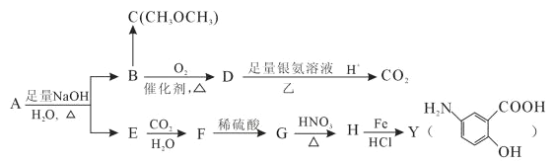
根据上述信息回答:
(1)请写出Y中含氧官能团的名称_________________________。
(2)写出反应③的反应类型:________________________________。
(3)写出反应①的化学方程式:_______________________________________。
(4)A的同分异构体I和J是重要的医药中间体,在浓硫酸的作用下I和J分别生成![]() 和
和![]() ,鉴别I和J的试剂为____________________。
,鉴别I和J的试剂为____________________。
(5)G的同分异构体中,满足下列条件的有_____________种。
①能发生银镜反应 ②能与氯化铁溶液发生显色反应
其中核磁共振氢谱显示四种不同类型的吸收峰。且其峰面积之比为1:2:2:1的结构简 式为____(写一种)。
(6)A的另一种同分异构体K用于合成高分子材料M(![]() ),K 可由L(
),K 可由L(![]() )制得。请写出以L为原料制得M 的合成路线流程图( 无机试剂任用)。流程图示例如下:
)制得。请写出以L为原料制得M 的合成路线流程图( 无机试剂任用)。流程图示例如下:![]() ___________________________
___________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:

(1)写出⑥元素的名称:______________。
(2)在以上元素的原子中,原子半径最大的是___________________(填元素符号)。
(3)地壳中含量居于第二位的元素位于元素周期表中的第___________周期,第_________族。
(4)⑦元素的气态氢化物化学式为___________________。
(5)⑤元素的最高价氧化物对应的水化物化学式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.2mol某烃A在氧气中完全燃烧后,生成CO2和H2O各1.2mol。
(1)烃A的分子式为_____.
(2)若烃A不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯取代物只有一种,则烃A的结构简式为_____.
(3)若烃A能使溴水褪色,在催化剂作用下,与H2发生加成反应,其加成产物B经测定分子中含有4个甲基,且其核磁共振氢谱图中有两组峰,则A可能有的结构简式为_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一个2L的密闭容器中加入4mol A和2mol B进行如下反应:3A(g)+2B(g)4C(s)+D(g),反应2min后达到平衡,测得生成1.6mol C,下列说法正确的是( )
A.前2 min D的平均反应速率为0.2 molL﹣1min﹣1
B.此时,B的平衡转化率是40%
C.增大该体系的压强,平衡不移动
D.增加B,平衡向右移动,B的平衡转化率增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com