
【题目】无水MgBr2可用作催化剂.实验室采用镁屑与液溴为原料制备无水MgBr2 , 装置如图1,主要步骤如下:
步骤1 三颈瓶中装入10g镁屑和150mL无水乙醚;装置B中加入15mL液溴.
步骤2 缓慢通入干燥的氮气,直至溴完全导入三颈瓶中.
步骤3 反应完毕后恢复至常温,过滤,滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤得三乙醚溴化镁粗品.
步骤4 室温下用苯溶解粗品,冷却至0℃,析出晶体,过滤,洗涤得三乙醚合溴化镁,加热至160℃分解得无水MgBr2产品.
已知:①Mg与Br2反应剧烈放热;MgBr2具有强吸水性.
②MgBr2+3C2H5OC2H5MgBr23C2H5OC2H5
请回答:
(1)仪器A的名称是 . 实验中不能用干燥空气代替干燥N2 , 原因是 .
(2)如将装置B改为装置C(图2),可能会导致的后果是 .
(3)步骤3中,第一次过滤除去的物质是 .
(4)有关步骤4的说法,正确的是 .
A.可用95%的乙醇代替苯溶解粗品
B.洗涤晶体可选用0℃的苯
C.加热至160℃的主要目的是除去苯
D.该步骤的目的是除去乙醚和可能残留的溴
(5)为测定产品的纯度,可用EDTA(简写为Y)标准溶液滴定,反应的离子方程式:
Mg2++Y4﹣═MgY2﹣
①滴定前润洗滴定管的操作方法是 .
②测定时,先称取0.2500g无水MgBr2产品,溶解后,用0.0500molL﹣1的EDTA标准溶液滴定至终点,消耗EDTA标准溶液26.50mL,则测得无水MgBr2产品的纯度是(以质量分数表示).
【答案】
(1)干燥管;防止镁屑与氧气反应,生成的MgO阻碍Mg和Br2的反应
(2)会将液溴快速压入三颈瓶,反应过快大量放热而存在安全隐患
(3)镁屑
(4)B,D
(5)从滴定管上口加入少量待测液,倾斜着转动滴定管,使液体润湿内壁,然后从下部放出,重复2﹣3次;97.5%
【解析】(1)仪器A为干燥管,本实验要用镁屑和液溴反应生成溴化镁,所以装置中不能有能与镁反应的气体,例如氧气,所以不能用干燥的空气代替干燥的氮气,所以答案是:防止镁屑与氧气反应生成的氧化镁阻碍Mg和Br2的反应,
所以答案是:干燥管;防止镁屑与氧气反应,生成的MgO阻碍Mg和Br2的反应;
(2)将装置B改为C装置,当干燥的氮气通入,会使气压变大,将液溴快速压入三颈瓶,反应过快大量放热存在安全隐患,装置B是利用干燥的氮气将溴蒸气带入三颈瓶中,反应可以容易控制防止反应过快,
所以答案是:会将液溴快速压入三颈瓶,反应过快大量放热而存在安全隐患;
(3)步骤3过滤出去的是不溶于水的镁屑,所以答案是:镁屑;
(4)A.95%的乙醇中含有水,溴化镁有强烈的吸水性,故A错误;B.加入苯的目的是除去乙醚和溴,洗涤晶体用0°C的苯,可以减少产品的溶解,故B正确;C.加热至160°C的主要目的是分解三乙醚合溴化镁得到溴化镁,不是为了除去苯,故C错误;D.该步骤是为了除去乙醚和溴,故D正确;故选BD;(5)①滴定前润洗滴定管是需要从滴定管上口加入少量待测液,倾斜着转动滴定管,使液体湿润内壁,然后从下步放出,重复2﹣3次,
所以答案是:从滴定管上口加入少量待测液,倾斜着转动滴定管,使液体润湿内壁,然后从下部放出,重复2﹣3次;
②依据方程式Mg2++Y4﹣═MgY2﹣分析,溴化镁的物质的量=0.0500mol/L×0.02650L=0.001325mol,则溴化镁的质量为0.001325mol×184g/mol=0.2438g,溴化镁的产品的纯度= ![]() ×100%=97.5%,
×100%=97.5%,
所以答案是:97.5%;


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
【题目】一同学欲从量筒中取出部分液体,他先俯视凹液面的最低处,读数为50mL,倒出液体后,他又仰视凹液面的最低处,读数为10mL他实际倒出液体的体积为
A. 40mL B. 大于40mL C. 小于40mL D. 不一定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在淀粉KI溶液中滴入少量NaClO溶液,并加入少量稀硫酸,溶液立即变蓝;在上述蓝色溶液中,滴加足量的Na2SO3溶液,蓝色逐渐消失.下列对该实验原理的解释和所得结论错误的是( )
A.第一步反应的离子方程式为ClO﹣+2I﹣+2H+═I2+Cl﹣+H2O
B.淀粉KI溶液变蓝是因为I﹣被氧化为I2 , 淀粉遇I2变蓝色
C.蓝色逐渐消失的原因是Na2SO3溶液具有漂白性
D.微粒的氧化性由强到弱的顺序是ClO﹣>I2>SO ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PTT是近几年来迅速发展起来的新型热塑性聚酯材料,具有优异性能,能作为工程塑料、纺织纤维和地毯等材料而得到广泛应用.其合成路线可设计为: 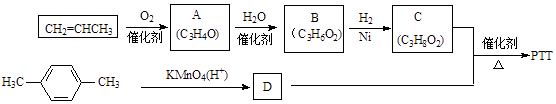
其中A、B、C均为链状化合物,A能发生银镜反应,B中不含甲基.请回答下列问题:
(1)A、B的结构简式分别为、
(2)写出一种满足下列条件的A的同系物的结构简式
①分子式为C4H6O ②含有1个﹣CH3
(3)1mol C可与足量钠反应生成L H2(标准状况).
(4)由物质C与D反应生成PTT的化学方程式为 , 反应类型为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式能表示可燃物燃烧热的是( )
A.H2(g)+Cl2(g)=2HCl(g)△H=﹣184.6 kJ?mol﹣1
B.CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=﹣802.3 kJ?mol﹣1
C.2H2(g)+O2(g)=2H2O(l)△H=﹣571.6 kJ?mol﹣1
D.CO(g)+ ![]() O2(g)=CO2(g)△H=﹣283 kJ?mol﹣1
O2(g)=CO2(g)△H=﹣283 kJ?mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下的定容密闭容器中,进行可逆反应:A(s)+2B(g)C(g)+D(g),当下列物理量不发生变化时:
①混合气体的密度
②容器内气体的压强
③混合气体的平均相对分子质量
④B的物质的量浓度
则能表明该反应一定已达到平衡状态的是( )
A.只有④
B.②③
C.②③④
D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种短周期主族元素,原子序数依次增大,A、B、F三者原子序数之和为25,且知B、F同主族,1.8g E与足量的盐酸反应生成ECl3和2.24L氢气(标准状况下),D+和E的离子具有相同的电子层结构,工业上用电解元素B和E能形成离子化合物的方法冶炼E单质,试判断:
(1)六种元素中非金属性最强的是(填代号),该元素在周期表中的位置
(2)由A、B、D三种元素形成化合物的电子式
(3)下列能够说明B、F非金属性强弱的方法有a.最高价氧化物对应水化物酸性
b.气态氢化物的热稳定性
c.气态氢化物的沸点B比F高
d.向F的气态氢化物溶液中通入B单质,有浑浊
(4)写出下列反应的离子方程式①由A、B、D、F四种元素可以组成两种酸式盐,写出这两种盐相反应的离子方程式
②写出足量D的最高价氧化物对应水化物与ECl3相互反应的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃与氢气发生反应后能生成(CH3)2CHCH2CH3 , 则该烃不可能是( )
A.2﹣甲基﹣2﹣丁烯
B.2,3﹣二甲基﹣1﹣丙烯
C.3﹣甲基﹣1﹣丁烯
D.2﹣甲基﹣1,3﹣丁二烯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com