
【题目】下列反应中,不属于四种基本反应类型,但属于氧化还原反应的是( )
A.2Na+2H2O═2NaOH+H2↑B.CaCO3+2HCl═CaCl2+H2O+CO2↑
C.2KClO3![]() 2KCl+3O2↑D.CH4+2O2
2KCl+3O2↑D.CH4+2O2![]() CO2+2H2O
CO2+2H2O
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
A.pH=1 的溶液中:HCO![]() 、SO
、SO![]() 、K+、Cl-
、K+、Cl-
B.遇酚酞变红的溶液中:NO![]() 、Na+、、SiO
、Na+、、SiO![]() 、K+
、K+
C.c(NO![]() ) = 1 mol·L -1 的溶液中:H+、Fe2+、Cl-、NH
) = 1 mol·L -1 的溶液中:H+、Fe2+、Cl-、NH![]()
D.无色透明溶液中: K+、SO![]() 、Na+、MnO
、Na+、MnO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)![]() 2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)放出热量99kJ,请回答下列问题:
2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)放出热量99kJ,请回答下列问题:
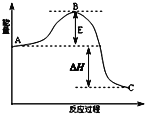
(1)图中A、C分别表示_____________、_____________.
(2)该反应通常用V2O5作催化剂,加V2O5会使图中B点_________(填“升高”,“降低”),△H_______(填“变大”,“变 小”或“不变”),理由是______________________.
(3)图中△H=________kJ/mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Y形管是一种特殊的仪器,与其他仪器组合可以进行某些实验探究。利用如图装置可以探究SO2与BaCl2反应生成BaSO3沉淀的条件。下列判断正确的是

A. e、f两管中的试剂可以分别是浓氨水和NaOH固体
B. 玻璃管的作用是连通大气,使空气中的氧气进入广口瓶,参与反应
C. c、d两根导管都必须插入BaCl2溶液中,保证气体与Ba2+充分接触
D. Y形管乙中产生的为氧化性气体,将BaSO3氧化为BaSO4沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,将两个铂电极插入一定量的饱和硫酸钠溶液中进行电解,通电一段时间后,阴极逸出a mol气体,同时有w g Na2SO4·10H2O晶体析出,若温度不变,剩余溶液中溶质质量分数是
A.w/(w+18a) ×100%
B.w/(w+36a) ×100%
C.7100w/[161(w+18a)] ×100%
D.7100w/[161(w+36a)] ×100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫是重要的化工原料,用途非常广泛。
实验一:SO2可以抑制细菌滋生,具有防腐功效。某实验小组欲用下图所示装置测定某品牌葡萄酒中(葡萄酒中含有乙醇、有机酸等)的SO2含量。
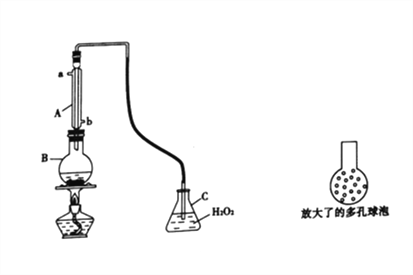
(1)仪器A的名称是________;使用该装置主要目的是____________________。
(2)B中加入 300.00 mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,C中化学方程式为_________________________________________。
(3)将输入C装置中的导管顶端改成具有多孔的球泡(如图15所示)。可提高实验的准确度,理由是_______________________________________。
(4)除去C中的H2O 然后用0.099mol·L-1NaOH标准溶液滴定。
①用碱式滴定管量取0.09mol·L-1NaOH标准溶液前的一步操作是___________________________;
②用该方法测定葡萄酒中SO2的含量偏高,主要原因是__________________________________,利用现有的装置,提出改进的措施是_______________________________________________。
(5)利用C中的溶液,有很多实验方案测定葡萄酒中SO2的含量。现有0.1mol·L-1BaCl2溶液,实验器材不限,简述实验步骤:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.标准状况下,11.2L三氯甲烷中含有氯原子的数目为1.5NA
B.90g葡萄糖中含氧原子数目为3NA
C.常温下,1L 0.5mol·L1醋酸铵溶液(pH=7)中CH3COO与![]() 数目均为0.5NA
数目均为0.5NA
D.1mol Na2O和1mol Na2O2组成的混合物中含有的离子总数为7NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓硫酸和木炭在加热时发生反应的化学方程式是2H2SO4(浓)+C![]() CO2↑+2H2O+2SO2↑。用如图所示装置设计一个实验,验证浓硫酸与木炭粉在加热条件下反应产生的各种产物。
CO2↑+2H2O+2SO2↑。用如图所示装置设计一个实验,验证浓硫酸与木炭粉在加热条件下反应产生的各种产物。
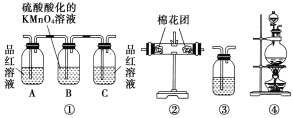
(1)这些装置的连接顺序(按产物气流从左到右的方向)是____→___→____→____。(填装置的序号)
(2)装置②中要检验产物中有水蒸气,则放入的药品是______;装置③中要检验产物中有二氧化碳气体,则放入的药品是___________;实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色,A瓶溶液的作用是_______,B瓶溶液的作用是_________,C瓶溶液的作用是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向50 mL 18 mol·L-1的H2SO4溶液中加入适量的铜片并加热。充分反应后,被还原的H2SO4的物质的量( )
A. 小于0.45 mol B. 等于0.45 mol
C. 在0.45~0.90 mol之间 D. 大于0.45 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com