
| A、25℃时,1 L pH=13的NaOH溶液中约含有6.02×1023个氢氧根离子 |
| B、1L 1 mol?L-1的盐酸中,所含氯化氢分子数为6.02×1023 |
| C、1 mol羟基(-OH)所含的电子数约为10×6.02×1023 |
| D、标准状况下,测得一定量的铜与硝酸反应后生成22.4 L NO、NO2、N2O4的混合气体,则被还原的硝酸的分子数大于6.02×1023 |


科目:高中化学 来源: 题型:
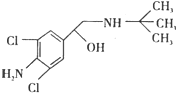 去年,某地区约 300 多人,因食用“瘦肉精”喂养的猪肉而中毒,己知瘦肉精的结构如如图,则它可能发生的化学反应有:①酯化反应 ②取代反应 ③氧化反应 ④消去反应( )
去年,某地区约 300 多人,因食用“瘦肉精”喂养的猪肉而中毒,己知瘦肉精的结构如如图,则它可能发生的化学反应有:①酯化反应 ②取代反应 ③氧化反应 ④消去反应( )| A、②④ | B、②③ |
| C、①②③ | D、①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4M mol |
| B、10M mol |
| C、10 M/3 mol |
| D、2 M/3 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化石能源物质内部贮存着大量的能量 |
| B、吸热反应是由于反应物总能量低于生成物总能量,因而没有利用价值 |
| C、由石墨制金刚石是吸热反应,故石墨能量比金刚石能量低 |
| D、化学物质中的化学能可以在一定条件下转化为热能、机械能、光能、电能为人类所利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、-67.7 KJ/mol |
| B、-43.5 KJ/mol |
| C、+43.5 KJ/mol |
| D、+67.7 KJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔质量 M g/mol |
| B、气体摩尔体积 Vm L/mol |
| C、溶解度 S g/100g |
| D、密度 ρ g/cm3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、德国从小学到高中很重视学生创新能力和实验能力的培养,在大学重视理工科的教学和研究,当时柏林大学教授的工资是第一线工人工资的50倍以上 |
| B、德国从小学到高中很重视学生解题能力的培养,每天都有大量的做不完的作业,所以,在以后的工作和科研中,遇到难题均能冥思苦想,得出正确的答案 |
| C、德国从小学到高中很重视学生数学能力的培养,为学生的发展打下了扎实的数学功底,使任何问题均能用数学方法解答出来 |
| D、德国从小学到高中很重视学生英语教学,为学生的国际交流打下了扎实的语言基础 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com