
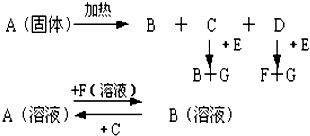
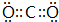 ,E为Na2O2,电子式为:
,E为Na2O2,电子式为: ,故答案为:
,故答案为: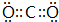 ;
; ;
;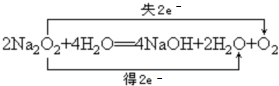 ,故答案为:
,故答案为: .
.


 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
| A、25℃时,1 L pH=13的NaOH溶液中约含有6.02×1023个氢氧根离子 |
| B、1L 1 mol?L-1的盐酸中,所含氯化氢分子数为6.02×1023 |
| C、1 mol羟基(-OH)所含的电子数约为10×6.02×1023 |
| D、标准状况下,测得一定量的铜与硝酸反应后生成22.4 L NO、NO2、N2O4的混合气体,则被还原的硝酸的分子数大于6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑤⑥ | B、②④⑤⑥ |
| C、①②④⑤ | D、①③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HX是强酸 |
| B、将两种一元酸均稀释100倍,稀释后两溶液的pH均为3 |
| C、酸性:HX<HY |
| D、两酸的浓度大小c(HX)<c(HY) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2SO4、NaOH--腐蚀品 |
| B、CH4、H2--易燃液体 |
| C、白磷--易燃固体 |
| D、KMnO4、H2O2--氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu、Fe3+ |
| B、Fe2+、Fe3+ |
| C、Cu、Cu2+、Fe |
| D、Cu、Fe2+、Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、生成一种强酸弱碱盐 |
| B、弱酸溶液和强碱溶液 |
| C、弱酸与弱碱溶液反应 |
| D、一元强酸溶液与一元强碱溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 阳离子 | H+、Na+、A13+、Ag+、Ba2+ |
| 阴离子 | OH-、C1-、CO32-、NO3-、SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com