
【题目】实验室可利用乙二醇、铜或铜的化合物制备乙二醛,下图是某兴趣小组设计的实验装置,右边的反应装置相同,而左边的气体发生装置不同,试管C中装有水(加热装置未画出)。试回答:
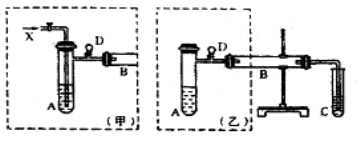
(1)两套装置中的A、B处都需加热,A处用水浴加热,A处用水浴加热的主要优点是 。
(2)若按甲装置进行实验,B管处装铜粉,通入A管的气体为X,B中反应的化学方程式为 。
(3)若按乙装置进行实验,则B管中应装 ,B中反应的化学方程式为 。
(4)实验完成时先打开D处的铁夹,再撤去酒精灯,这样做的目的是 。
【答案】(1)试管受热均匀,产生气体速度平稳
(2)HOCH2CH2OH+O2 ![]() OHC—CHO+2H2O
OHC—CHO+2H2O
(3)CuO HOCH2CH2OH +2CuO![]() OHC—CHO +2H2O+2Cu
OHC—CHO +2H2O+2Cu
(4)防止倒吸
【解析】
试题分析:(1)A处用水浴加热是为了得到乙二醇蒸气,醇通过固体铜或氧化铜加热反应生成乙二醛,所以A处用水浴加热,A处用水浴加热的主要优点是试管受热均匀,产生气体速度平稳。
(2)按甲装置进行实验,B管处装铜粉,则通入A管的X气体为空气或氧气,目的是为了生成氧化铜催化氧化乙二醇,所以反应的化学方程式为:HOCH2CH2OH+O2 ![]() OHC—CHO+2H2O。
OHC—CHO+2H2O。
(3)按乙装置进行实验无空气或氧气通入,根据醇催化氧化的实质是被氧化铜氧化得到醛,所以B管中应装入氧化铜,加热条件下反应生成乙二醛,反应的化学方程式为:HOCH2CH2OH +2CuO![]() OHC—CHO +2H2O+2Cu。
OHC—CHO +2H2O+2Cu。
(4)生成的乙二醛易溶于水,则实验完成时先打开D处的铁夹,再撤去酒精灯,可以防止装置内压强降低引起的倒吸。


科目:高中化学 来源: 题型:
【题目】(14分)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请用如图实验装置,选用适当的化学试剂和实验用品,设计并完成对过氧化钠这一性质的探究。
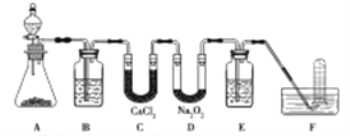
(1)A是实验室制取CO2的装置,其中发生反应的离子方程式是________;装置B的作用是____________。
(2)检验F中气体成分,即能说明过氧化钠可作潜水艇供氧剂,则实验操作的方法及现象是_______________。
(3)查阅有关资料表明:2H2O+2Na2O2=4NaOH+O2↑。某研究小组用同位素标记法对过氧化钠进行标记(![]() ),以探究这一反应的历程:_________________
),以探究这一反应的历程:_________________
①甲同学从电子转移角度得出其离子方程式为:_______________。
②乙同学发现:向Na2O2与水反应后的溶液中加入MnO2,又产生无色能使带火星的木条复燃的气体,从这个角度,写出其反应历程:___________________。
(4)设计并完成过氧化钠样品(已知所含杂质与酸碱均不反应)的纯度测定:
甲、乙两位同学各取了ag样品并分别配制成了100.00mL溶液进行实验,实验操作中甲同学是将样品直接溶于蒸馏水中;而乙同学却是将蒸馏水先加热煮沸,再把蒸馏水分成两份,一份中趁热加入样品溶解,待冷却到室温后再加人另一份水来进行配制。他们分别取出各自配制的溶液20.00mL,加入酚酞数滴后,用浓度为cmol/L的盐酸进行滴定;重复滴定操作2次,甲同学和乙同学分别计算出了所用盐酸的体积平均值,分别为VAmL和VWmL。
①在样品的溶解与配制中,你认为_______(填“甲”、“乙”)同学的操作是合理的,理由是:__________________。
②另一同学的操作将会使实验结果______(填“偏大”、“偏小”或“无影响”)。
③原过氧化钠样品的纯度是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(12分)甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究。
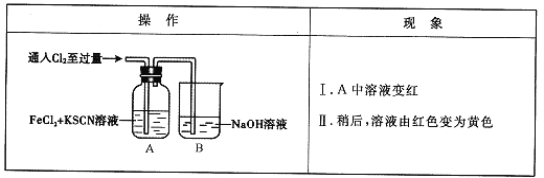
(1)B中反应的离子方程式是_ ___。
(2)A中溶液变红的原因是__ __。
(3)为了探究现象II的原因,甲同学进行如下实验。
①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在 。
②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液。
甲同学的实验证明产生现象Ⅱ的原因是SCN-与Cl2发生了反应。
(4)甲同学猜想SCN-可能被Cl2氧化了,他又进行了如下研究。
资料显示:SCN-的电子式为![]()
①甲同学认为SCN-中碳元素没有被氧化,理由是 。
②取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN—中被氧化的元素是 。
③通过实验证明了SCN-中氮元素转化为NO3-。
④若SCN-与Cl2反应生成1 mol CO2,则转移电子的物质的量是 mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据钠与水(滴有酚酞溶液)反应的实验现象,不能得出的结论是 ( )
A. 钠的密度比水小 B. 钠的硬度小
C. 钠很活泼,易与水反应生成碱性物质 D. 钠的熔点低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空气吹出法工艺是目前“海水提溴”的最主要方法之一。其工艺流程如下:
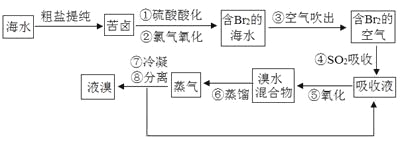
(1)步骤①中氯气氧化溴离子时在pH=3.5的酸性条件下效果最好,当使用精确pH试纸(能读数到0.1)检测步骤②氯气氧化的溶液的pH时,发现其颜色变化失常,则pH检测失败的原因是 。
(2)步骤④中反应的化学方程式为 ,该反应中体现了SO2的 性(填“氧化”或“还原”)。
(3)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,在实验室可用分液漏斗进行分离。分离时从分液漏斗的上口倒出的是 。
(4)步骤①、②之后并未直接用“含Br2的海水”进行蒸馏得到液溴,而是经过“空气吹出”、“SO2吸收”、“氧化”后再蒸馏,“空气吹出、SO2吸收、氧化”的过程实际上是一个Br2的 过程,与直接蒸馏含Br2的海水相比优点是消耗更少成本降低和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
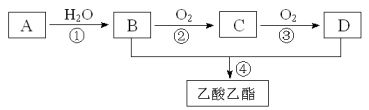
回答下列问题:
(1)写出A的电子式 ,其空间构型 。
(2)B、D分子中的官能团名称分别是 、 ;
(3)写出下列反应的反应类型:② ④ ;
(4)写出A→B反应的化学方程式: ;
(5)写出B与D反应生成乙酸乙酯的化学反应方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在C(s)+CO2(g)=2CO(g)的反应中,现采取下列措施:
①缩小体积,增大压强
②增加碳的量
③通入CO2
④恒容下充入N2
⑤恒压下充入N2
能够使反应速率增大的措施是
A.①④ B.②③⑤ C.①③ D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D为短周期元素,A的M电子层有1个电子,B的最外层电子数为内层电子数的2倍,C的最高化合价为最低化合价绝对值的3倍,C与D同周期,D的原子半径小于C。
(1)B位于元素周期表第____周期第____族。
(2)C2-离子的结构示意图为____。A+、C2-、D-中离子半径最小的是____。(用具体离子符号表示)
(3)BC2与二氧化碳的结构相似,其结构式为____。A2C的电子式为____。
(4)A、D元素最高价氧化物对应水化物相互反应的化学方程式为____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com