
����Ŀ��CO��H2�ǹ�ҵ����õĺϳ������úϳ������Ʊ������ܶ࣬����Ҳ�ܺϳ�������Ҫ���л���ش��������⣺
(1)�Ʊ��úϳ�����һ�ַ�������CH4��H2OΪԭ�ϣ��йط�Ӧ�������仯��ͼ��ʾ��
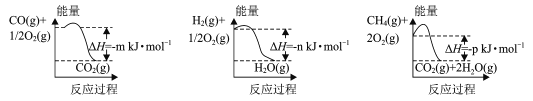
CH4 (g)��H2O(g)��Ӧ����CO(g)��H2 (g)���Ȼ�ѧ����ʽΪ____��
(2)��ҵ�Ҵ�Ҳ����CO��H2�ϳɣ�����һ�����״��������Ͻ�ʹ�óɱ������Ĺ�ҵ�ƾ�����ʳ�þƣ���һ�㶨�Եķ������Ѽ���ʳ�þ��еļ״������˾��������ữ�ij�ɫK2Cr2O7��Һ�����ⶨ������м״��ĺ������״�������K2Cr2O7��Һ��Ӧ����CO2��Cr2(SO4)3�����ʣ�д���仯ѧ����ʽ ___________��
(3)Ϊ�˼�����CO��H2�ϳ����ϳɵ�ij�л���M����ɣ����������²ⶨ����1.84gM�������г��ȼ�գ������ɵ���������ͨ�������ļ�ʯ�ң���ʯ�� ����4. 08 g����֪����CO2��H2O�����ʵ���֮��Ϊ3:4����M��̼���⡢��ԭ�Ӹ���֮��Ϊ____��
(4) CO2��H2�ϳɼ״��漰���·�Ӧ��CO2(g)+3H2(g)CH3OH(g)+H2O(g) H=-49.58kJ/mol���ڷ�Ӧ�����п����ں�ѹ���ܱ������У�����һ������CO2��H2����ò�ͬ�¶��£���ϵ��CO2��ƽ��ת������ѹǿ�Ĺ�ϵ������ͼ��ʾ��
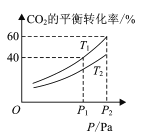
�ٷ�Ӧ�����У�������Ӧ�ﵽƽ��״̬�ı�־��______;
A.����3mol O-H����ͬʱ����3mol H-H�� B.�����������ѹǿ���ٱ仯
C.�����������ƽ��Ħ���������� D.CH3OH��Ũ�Ȳ��ٸı�
�ڱȽ�T1��T2�Ĵ�С��ϵ��T1 ___T2 (����<������=������>��)��
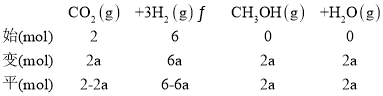
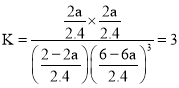
����T1��P2�������£����ܱ������г���1mol CO2��3mol H2���÷�Ӧ�ڵ�5 minʱ�ﵽƽ�⣬��ʱ�������ݻ�Ϊ2.4 L����÷�Ӧ�ڴ��¶��µ�ƽ�ⳣ��Ϊ____������T1�ʹ�ʱ�������ݻ����䣬�ٳ���1mol CO2��3mol H2����ﵽƽ��ʱCO2����ת����Ϊa��д��һ���ܹ����a�ķ��̻�ʽ�� ___(���ػ����Բ�����λ)��
���𰸡�CH4(g)+H2O(g)=CO(g)+3H2(g) ��H=+(-p+3n+m)kJ��mol��1 CH3OH+K2Cr2O7+4H2SO4=CO2+K2SO4+Cr2(SO4)3+6H2O 3:8:3 CD �� 3 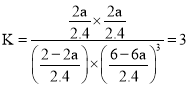
��������
(1)����ͼ����д�Ȼ�ѧ����ʽ����ϸ�˹���ɼ��㷴Ӧ�ȣ�
(2)����ṩ��Ϣ������������ԭ��Ӧ����غ�������غ���д����ʽ��
(3)�����л���ȼ��̼ԭ���غ㡢��ԭ���غ㣬�Լ�������ı�����ϵ�з��̼���M�е�̼���⡢����Ŀ��
(4)�ٸ���ƽ��״̬���ص㣬�Լ�������ɲ�����ʱ��Ӧ�ﵽƽ��ȷ����жϣ�
�ڶ�����̼��ת�������¶ȵ����߶����ͣ��ݴ˷�����
���С�����ʽ���������¶Ȳ��䣬ƽ�ⳣ������Ĺ�ϵ���н����㡣
(1)��������������ϵͼ��д����Ӧ���Ȼ�ѧ����ʽ��CO(g)��![]() O2(g)= CO2(g) ��H1����m kJ��mol��1��H2(g)��
O2(g)= CO2(g) ��H1����m kJ��mol��1��H2(g)��![]() O2(g)=H2O(g) ��H2����n kJ��mol��1��CH4(g)��2O2(g)=CO2(g)+ 2H2O(g)��H3����p kJ��mol��1���ɸ�˹���ɵã�CH4(g)+H2O(g)=CO(g)+3H2(g)��H����H3��3��H2����H1��+(��p+3��n+m)kJ��mol��1��
O2(g)=H2O(g) ��H2����n kJ��mol��1��CH4(g)��2O2(g)=CO2(g)+ 2H2O(g)��H3����p kJ��mol��1���ɸ�˹���ɵã�CH4(g)+H2O(g)=CO(g)+3H2(g)��H����H3��3��H2����H1��+(��p+3��n+m)kJ��mol��1��
(2)�״�������K2Cr2O7��Һ��Ӧ����CO2��Cr2(SO4)3��Cr�Ļ��ϼ۽���3��̼�Ļ��ϼ�����6�����ݵ���غ㣬�����غ�ɵ�CH3OH+K2Cr2O7+4H2SO4=CO2+K2SO4+Cr2(SO4)3+6H2O��
(3)����1.84g M�к�Cx mol����H y mol����������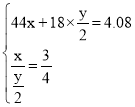 �����x=0.06 y=0.16����1.84g M�к������ʵ���z=
�����x=0.06 y=0.16����1.84g M�к������ʵ���z=![]() =0.06 mol��1mol M�к�C��H��O�ֱ�Ϊ3��8��3����M��̼���⡢��ԭ�Ӹ���֮��Ϊ3:8:3��
=0.06 mol��1mol M�к�C��H��O�ֱ�Ϊ3��8��3����M��̼���⡢��ԭ�Ӹ���֮��Ϊ3:8:3��
(4)��A������3 mol H��H������ζ��������3molH2��CH3OH��H2O�о���H��O��������Ӧ������3mol O-H��������������Ӧ���ʵı仯��ϵ�����Բ���˵��v��=v������A����
B�����ڷ�Ӧ������������ѹǿһֱ���ֲ��䣬����ѹǿ���ٱ�����ʱ��Ҳ����˵��v��=v������B����
C�������з�Ӧ��������Ϊ���壬����������mһֱ���ֲ��䣬����Ӧǰ���������ʵ������n��0����ֻ�е���Ӧ�ﵽƽ��״̬ʱ����ϵ�������ʵ���n�Ų��ٱ仯������M=![]() ֪��ƽ��Ħ�������������ܹ�������Ӧ�ﵽƽ��״̬����C��ȷ��
֪��ƽ��Ħ�������������ܹ�������Ӧ�ﵽƽ��״̬����C��ȷ��
D����CH3OH��Ũ�Ȳ��ٸı�����������λʱ�������ɺ����ĵ�CH3OH��Ũ����ȣ���v��=v������Ӧ�ﵽƽ��״̬����D��ȷ��
��ѡCD��
������H����49.58 kJ��mol��1��0��֪����ӦΪ���ȷ�Ӧ����ͬһѹǿ�£��¶����߿�ʹCO2��ת���ʽ��ͣ�����ͼ���֪T1��T2��
����ͼ1֪����T1��p2�������£�ƽ��ʱCO2��ת����Ϊ60%�����ĵ�CO2Ϊ1mol ��60%��0.6 mol���������¹�ϵ��

������������(2.4L)�У�ƽ����ϵ�и����ʵ�Ũ��Ϊc(CO2)=![]() mol��L��1��c(H2)=
mol��L��1��c(H2)=![]() mol��L��1��c(CH3OH)=
mol��L��1��c(CH3OH)=![]() mol��L��1��c(H2O)=
mol��L��1��c(H2O)=![]() mol��L��1����������µ�ƽ�ⳣ��Ϊ
mol��L��1����������µ�ƽ�ⳣ��Ϊ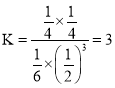 �������ٳ���ԭ����ʱ����Ӧ�¶�û�䣬��K���䡣��ﵽƽ��ʱCO2����ת����Ϊa�������������з�Ӧ��CO2Ϊ2a mol��ͬ�������¹�ϵ��
�������ٳ���ԭ����ʱ����Ӧ�¶�û�䣬��K���䡣��ﵽƽ��ʱCO2����ת����Ϊa�������������з�Ӧ��CO2Ϊ2a mol��ͬ�������¹�ϵ��
 ��
��


 ����ѵ�����⿼ϵ�д�
����ѵ�����⿼ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ��Ŵ��Ĵ���֮һ�ĺڻ�ҩ������Ƿۡ�����غ�ľ̿�۰�һ��������϶��ɵģ���ը�ķ�ӦΪ��S+2KNO3+3C![]() K2S+N2��+3CO2��������˵������ȷ���ǣ� ��
K2S+N2��+3CO2��������˵������ȷ���ǣ� ��
A.�÷�Ӧ�еĻ�ԭ��ΪKNO3
B.�÷�Ӧ��C����ԭ
C.������32g S���÷�Ӧת�Ƶ�����Ϊ4 NA
D.�����ɱ�״��������22.4L������0.75 mol���ʱ���ԭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС��Ϊ��̽��������ˮ������Ӧ�IJ����������ʵ�顣
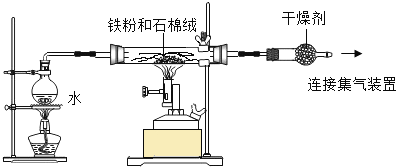
���ϣ��ڲ�ͬ�¶��£�������ˮ������Ӧ�IJ��ﲻͬ��
Fe +H2O![]() FeO+H2 3Fe + 4H2O
FeO+H2 3Fe + 4H2O![]() Fe3O4 + 4H2
Fe3O4 + 4H2
ʵ��һ��ij��ȤС������ͼ��ʾװ�ã�ʹ���������ˮ������ַ�Ӧ���������������ɡ�
(1)ʵ������У�Ӧ�ȵ�ȼ___________��ѡ�����ƾ����������ƾ����������Ŀ����__________________��װ����ʯ����������_____________________��
(2)����ʵ���е�ij��ʱ��������H2 0.2g�������ʱ���ڲμӷ�Ӧ����������������___________g��
ʵ�����������ȫ��Ӧ����ȤС���Ӳ�ʲ����������ɵ�FeO��Fe3O4���������вⶨ��ʵ����������ͼ��
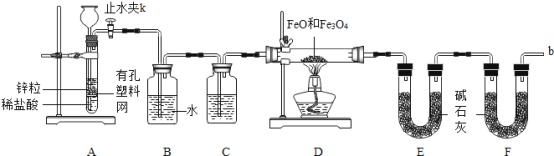
(1)ʵ��ǰ���װ��A�������ԣ��ر�ֹˮ��K���ӳ���©�����Թ��ڼ�ˮ��������©���й��ڵ�Һ����ڹ���Һ�棬����һ��ʱ�䣬��Һ��߶Ȳ�__________�������������á�
(2)װ��A�з����ķ�Ӧ����ʽ_______________________________________��
(3)Ϊ�˰�ȫ���ڵ�ȼ�ƾ���֮ǰ����Fװ�ó���b������______________________��
(4)װ��C�������Լ�Ϊ_________��װ��B��������_________________________��
(5)�����E�ұ������Ӹ����F��Ŀ����_________________________________��
�������F�����Fe3O4��������_______________������ƫ��������ƫС��������Ӱ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ�����
��1����Ȼ������Ҫ�ɷ���_____��д��ѧʽ��������ӿռ乹����_____��
��2������Һ��������Ϊ����ʱ������Ӧ�Ļ�ѧ����ʽ_____����Ӧ����Ϊ_____��
��3��д��Na��ˮ��Ӧ�����ӷ���ʽ_____��
��4��CH2��CH��CH��CH2��H2��һ�������·���1��4���ӳɷ�Ӧ�Ļ�ѧ����ʽ_____��
��5�����Ľṹ��ʽ��![]() �������ʽ_____��һ�ȴ�����_____�֡�
�������ʽ_____��һ�ȴ�����_____�֡�
��6��ijĦ������Ϊ42gmol��1������A��ʹ��ˮ��ɫ��A�Ľṹ��ʽΪ_____��A��һ�������¿��Է����Ӿ۷�Ӧ������Ľṹ��ʽΪ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ŀǰ�����ҵ�Ͷ�������ڽ������������ǧ��������Һ����ش���ʾ����վ��������Һ������ܷ�ӦΪFe3++Cr2+![]() Fe2++Cr3+������ʾ��ͼ��ͼ������˵���������
Fe2++Cr3+������ʾ��ͼ��ͼ������˵���������

A.�ŵ�ʱa�缫��ӦΪFe 3++e=Fe2+
B.���ʱb�缫��ӦΪCr3++e=Cr2+
C.�ŵ������H+ͨ����Ĥ��������������
D.�õ���ޱ�ը���ܣ���ȫ�Ըߣ����Ժ�ʴ����Խϵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������У����������Ȳ���������Ȼ��������ܽ⡱������ǣ� ��
A. ��ϡ��������μ��������![]() ��Һ
��Һ
B. ��![]() ��Һ����μ������ϡ
��Һ����μ������ϡ![]() ��Һ
��Һ
C. ��![]() ��Һ����μ���ϡ��ˮ
��Һ����μ���ϡ��ˮ
D. ������������Һ��ͨ�����![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������23V)���ҹ��ķ��Ԫ�أ��㷺���ڴ���������ҵ���ش��������⣺
��1������Ԫ�����ڱ��е�λ��Ϊ_______����۲�����Ų�ͼΪ____________��
��2������ij��������ľ����ṹ��ͼ1��ʾ��������ʵ��ӵ�е����������Ӹ����ֱ�Ϊ____��_____��
��3��V2O5������SO2ת��ΪSO3�Ĵ�����SO2������Sԭ�Ӽ۲���Ӷ�����__�ԣ����ӵ����幹��Ϊ___��SO3��̬Ϊ�����ӣ��÷�����Sԭ�ӵ��ӻ��������Ϊ____��SO3�������廷״�ṹ��ͼ2��ʾ���ýṹ��Sԭ�ӵ��ӻ��������Ϊ___���ýṹ��S��O���������࣬һ�����Լ140pm����һ�����ԼΪ160pm���϶̵ļ�Ϊ__����ͼ2����ĸ)���÷����к���___��������

��4��V2O5�ܽ���NaOH��Һ�У��ɵõ������ƣ�Na3VO4)�����������ӵ����幹��Ϊ___��Ҳ���Եõ�ƫ�����ƣ��������ӳ���ͼ3��ʾ��������״�ṹ����ƫ�����ƵĻ�ѧʽΪ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȫ��̬����������ܶȸߡ��ɱ��ͣ��乤��ԭ����ͼ��ʾ�����е缫 a���ò���ʯīϩ��S8���ϣ���ط�ӦΪ��16Li+xS8=8Li2Sx��2��x��8��������˵��������ǣ� ��

A. ��ع���ʱ�������ɷ�����Ӧ��2Li2S6+2Li++2e-=3Li2S4
B. ��ع���ʱ�����·������ 0.02 mol ���ӣ��������ϼ��� 0.14 g
C. ʯīϩ��������Ҫ����ߵ缫a�ĵ�����
D. ��س��ʱ��Խ���������Li2S2����Խ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڵ���ʵ�˵����ȷ����
A.���������ˮ��Һ�ܵ���,�ʶ��������ǵ����
B.![]() ��AgCl��ˮ���ܽ�Ⱥ�С,�������������
��AgCl��ˮ���ܽ�Ⱥ�С,�������������
C.�������Һͨ�����ܷ�������
D.��ˮ�еμ�������Ũ�ȵĴ�����Һ��,��Һ��������ǿ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com