
����Ŀ����Ҫ�����
��1����Ȼ������Ҫ�ɷ���_____��д��ѧʽ��������ӿռ乹����_____��
��2������Һ��������Ϊ����ʱ������Ӧ�Ļ�ѧ����ʽ_____����Ӧ����Ϊ_____��
��3��д��Na��ˮ��Ӧ�����ӷ���ʽ_____��
��4��CH2��CH��CH��CH2��H2��һ�������·���1��4���ӳɷ�Ӧ�Ļ�ѧ����ʽ_____��
��5�����Ľṹ��ʽ��![]() �������ʽ_____��һ�ȴ�����_____�֡�
�������ʽ_____��һ�ȴ�����_____�֡�
��6��ijĦ������Ϊ42gmol��1������A��ʹ��ˮ��ɫ��A�Ľṹ��ʽΪ_____��A��һ�������¿��Է����Ӿ۷�Ӧ������Ľṹ��ʽΪ_____��
���𰸡�CH4 ���������� 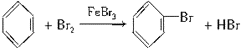 ȡ����Ӧ 2Na+2H2O��2Na++2OH��+H2 CH2��CH��CH��CH2+H2
ȡ����Ӧ 2Na+2H2O��2Na++2OH��+H2 CH2��CH��CH��CH2+H2![]() CH3��CH��CH��CH3 C10H8 2 CH2��CH��CH3
CH3��CH��CH��CH3 C10H8 2 CH2��CH��CH3 ![]()
��������
��1����Ȼ������Ҫ�ɷ�Ϊ���飬Ϊ��������ṹ���ʴ�Ϊ��CH4�����������ͣ�
��2������Һ��������Ϊ����ʱ����ȡ����Ӧ�����屽������ʽΪ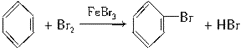 ��
��
�ʴ�Ϊ�� ��ȡ����Ӧ��
��ȡ����Ӧ��
��3���ƺ�ˮ��Ӧ�����������ƺ���������Ӧ�����ӷ���ʽΪ2Na+2H2O��2Na++2OH��+H2���ʴ�Ϊ��2Na+2H2O��2Na++2OH��+H2��
��4��CH2��CH��CH��CH2��H2��һ�������·���1��4���ӳɷ�Ӧ����CH3��CH��CH��CH3����Ӧ�ķ���ʽΪCH2��CH��CH��CH2+H2һ������CH3��CH��CH��CH3���ʴ�Ϊ��CH2��CH��CH��CH2+H2![]() CH3��CH��CH��CH3��
CH3��CH��CH��CH3��
��5��![]() �����к���10��C��8��Hԭ�ӣ�����ʽΪC10H8����������2��H����һ�ȴ�����2�֣�
�����к���10��C��8��Hԭ�ӣ�����ʽΪC10H8����������2��H����һ�ȴ�����2�֣�
�ʴ�Ϊ��C10H8 ��2��
��6��Ħ������Ϊ42gmol��1������A��ʹ��ˮ��ɫ������̼̼˫����ӦΪCH2��CH��CH3���ɷ����Ӿ۷�Ӧ���ɾ۱�ϩ������ʽΪCH2��CH��CH3![]()
![]() ���ʴ�Ϊ��CH2��CH��CH3 ��
���ʴ�Ϊ��CH2��CH��CH3 ��![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ��������������ȷ���ǣ� ��
A. ���³�ѹ�£�11.2L����������ԭ����ΪNA
B. 1.8g��NH4+�����к��е�������ΪNA
C. ���³�ѹ�£�46gNO2���е�ԭ������Ϊ3NA
D. ����£�4.48LH2O�к�����ԭ����Ϊ0.4NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£�ֻ�ı䷴Ӧ����n(SO2)�Է�Ӧ2SO2(g)+O2(g)2SO3(g)��Ӱ����ͼ��ʾ������˵����ȷ���ǣ�������
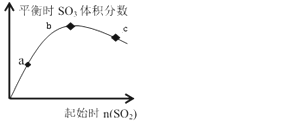
A. ��Ӧa��b��c���Ϊƽ��㣬��b��ʱSO2��ת�������
B. b��ʱSO2��O2 �����ʵ�֮��ԼΪ2��1
C. a��b��c ����ƽ�ⳣ���� Kb>Kc>Ka
D. a��b��c ���㷴Ӧ���ʴ�СΪ�� vb>vc>va
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�����һ��ԭ��ء�
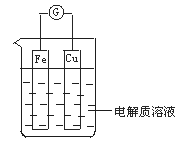
��1�����������ҺΪϡ����ʱ��
��Fe�缫��__(���������)������缫��ӦΪ___��
��Cu�缫��__������缫��ӦΪ___��
��2����ͭ��п��ϡ������ɵ�ԭ����У�ͭ��__�����缫��Ӧʽ��__��п��__�����缫��Ӧʽ��___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڴ�ʳ���г���ɳ�⣬����Na2SO4��MgCl2��CaCl2�����ʣ���ҵ�ƾ��γ���ʱ��������������ij��Ӽ������ṩ�����Լ���a.NaOH��Һ��b.���c.BaCl2��Һ��d.Na2CO3��Һ��������Լ��Ͳ�������ȷ���ǣ� ��
A.����![]() ����ˮ
����ˮ![]()
![]()
![]() ��Һ
��Һ![]() ����
����
B.����![]() ����ˮ
����ˮ![]()
![]()
![]() ��Һ
��Һ![]() ����
����
C.����![]() ����ˮ
����ˮ![]()
![]()
![]() ��Һ
��Һ![]() ����
����
D.����![]() ����ˮ
����ˮ![]()
![]()
![]() ��Һ
��Һ![]() ����
����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС�����û�ѧ��������һ���������������������40 g NaOH�����ձ��У�����һ����������ˮ����NaOH��ȫ�ܽ����Һȫ��ת�Ƶ������У�������ˮϡ������ȫ��������������ȡ����Һ100 mL������Һǡ����20mL 1mol/L CuSO4��Һ��ȫ��Ӧ��
(1)д��CuSO4��Ħ������______________��
(2)�����Ƶ�NaOH��Һ�����ʵ���Ũ��______________��
(3)�Լ�������������______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO��H2�ǹ�ҵ����õĺϳ������úϳ������Ʊ������ܶ࣬����Ҳ�ܺϳ�������Ҫ���л���ش��������⣺
(1)�Ʊ��úϳ�����һ�ַ�������CH4��H2OΪԭ�ϣ��йط�Ӧ�������仯��ͼ��ʾ��
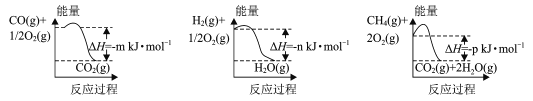
CH4 (g)��H2O(g)��Ӧ����CO(g)��H2 (g)���Ȼ�ѧ����ʽΪ____��
(2)��ҵ�Ҵ�Ҳ����CO��H2�ϳɣ�����һ�����״��������Ͻ�ʹ�óɱ������Ĺ�ҵ�ƾ�����ʳ�þƣ���һ�㶨�Եķ������Ѽ���ʳ�þ��еļ״������˾��������ữ�ij�ɫK2Cr2O7��Һ�����ⶨ������м״��ĺ������״�������K2Cr2O7��Һ��Ӧ����CO2��Cr2(SO4)3�����ʣ�д���仯ѧ����ʽ ___________��
(3)Ϊ�˼�����CO��H2�ϳ����ϳɵ�ij�л���M����ɣ����������²ⶨ����1.84gM�������г��ȼ�գ������ɵ���������ͨ�������ļ�ʯ�ң���ʯ�� ����4. 08 g����֪����CO2��H2O�����ʵ���֮��Ϊ3:4����M��̼���⡢��ԭ�Ӹ���֮��Ϊ____��
(4) CO2��H2�ϳɼ״��漰���·�Ӧ��CO2(g)+3H2(g)CH3OH(g)+H2O(g) H=-49.58kJ/mol���ڷ�Ӧ�����п����ں�ѹ���ܱ������У�����һ������CO2��H2����ò�ͬ�¶��£���ϵ��CO2��ƽ��ת������ѹǿ�Ĺ�ϵ������ͼ��ʾ��
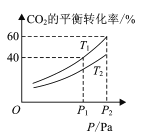
�ٷ�Ӧ�����У�������Ӧ�ﵽƽ��״̬�ı�־��______;
A.����3mol O-H����ͬʱ����3mol H-H�� B.�����������ѹǿ���ٱ仯
C.�����������ƽ��Ħ���������� D.CH3OH��Ũ�Ȳ��ٸı�
�ڱȽ�T1��T2�Ĵ�С��ϵ��T1 ___T2 (����<������=������>��)��
����T1��P2�������£����ܱ������г���1mol CO2��3mol H2���÷�Ӧ�ڵ�5 minʱ�ﵽƽ�⣬��ʱ�������ݻ�Ϊ2.4 L����÷�Ӧ�ڴ��¶��µ�ƽ�ⳣ��Ϊ____������T1�ʹ�ʱ�������ݻ����䣬�ٳ���1mol CO2��3mol H2����ﵽƽ��ʱCO2����ת����Ϊa��д��һ���ܹ����a�ķ��̻�ʽ�� ___(���ػ����Բ�����λ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ͻ�������Ͼ�����������������ܣ���������ܵĿ���������Ҫ���á�
��1��һ���¶��£�ij����Ͻ�M�������������ͼ��ʾ������Ϊƽ��ʱ������ѹǿ��p���������ʾ��������ԭ�������ԭ�ӵĸ����ȣ�H/M����
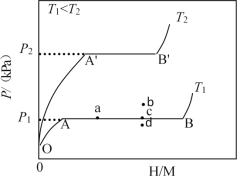
��OA�Σ����ܽ���M���γɹ�����MHx����������ѹǿ������H/M���������AB�Σ�MHx�����������⻯��Ӧ�����⻯��MHy���⻯��Ӧ����ʽΪ��zMHx(s)+H2(g)=ZMHy(s)��H(��)����B�㣬�⻯��Ӧ��������һ����������ѹǿ��H/M�������䡣��Ӧ������z=___���ú�x��y�Ĵ���ʽ��ʾ�����¶�ΪT1ʱ��2gij�Ͻ�4min����������240mL����������v=___mLg-1min����Ӧ���ʱ��H1__0������>����<������=������
��2������ʾ��λ��������Ͻ����⻯��Ӧ�ε����������ռ�����������ı��������¶�ΪT1��T2ʱ������T1��____����T2��������>����<������=����������Ӧ������ͼ��a��ʱ�������¶Ȳ��䣬�������ϵ��ͨ�������������ﵽƽ���Ӧ�����ܴ���ͼ�е�___�㣨����b����c������d������������Ͻ��ͨ��___��___�ķ�ʽ�ͷ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������ϢϢ��أ����й��������������Ļ�ѧ�������������ȷ���ǣ�������
A. ��������һʱ��DDT��±������һ��
B. ά�ڡ���֬����Ȼ����ȩ��֬�����ɸ߷��ӻ�������ɵ�����
C. ��ȩˮ��Һ���Է��������Dz�������ʳƷ��ı��ʼ�
D. ���Խ����ݹ����������Һ�Ĺ�������ˮ��һ�𱣴����ﵽˮ�����ʵ�Ŀ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com