
【题目】下列图象与对应实验操作相符合的是( )
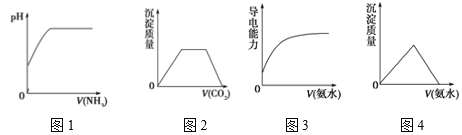
A. 图1 表示在水中慢慢通入氨气至过量
B. 图2表示在氢氧化钠和偏铝酸钠混合溶液中通入二氧化碳至过量
C. 图3表示在醋酸溶液中慢慢滴加同浓度的氨水至过量
D. 图4表示在氯化铝溶液中滴加氨水至过量
【答案】A
【解析】
A.氨气通入水中,氨气和水反应生成一水合氨,一水合氨电离出铵根离子和氢氧根离子,溶液中氨气饱和,PH不再变化;
B.向NaOH和Ca(OH)2的混合溶液中通入CO2,先发生Ca(OH)2+CO2═CaCO3↓+H2O,再发生CO2+NaOH═NaHCO3,最后发生CaCO3↓+H2O+CO2═Ca(HCO3)2;
C.溶液导电能力的强弱主要取决于阴、阳离子浓度的大小,离子浓度越大,导电能力越强,乙酸与氨水反应生成乙酸铵,乙酸铵属于强电解质,但氨水至过量,导电能力减弱;
D.向氯化铝溶液中滴加氨水,由于生成的氢氧化铝不溶于氨水弱碱,沉淀不溶解。
A.氨气通入水中,NH3+H2O![]() NH3·H2O
NH3·H2O![]() NH4++OH-,氨气未饱和前,溶液的PH在不断增大,当溶液饱和时,PH不再变化,故A正确;
NH4++OH-,氨气未饱和前,溶液的PH在不断增大,当溶液饱和时,PH不再变化,故A正确;
B.因向NaOH和Ca(OH)2的混合液中通入CO2,先发生Ca(OH)2+CO2═CaCO3↓+H2O,生成沉淀,再发生CO2+NaOH═NaHCO3,沉淀的量不变,最后发生反应:CaCO3↓+H2O+CO2═Ca(HCO3)2,沉淀溶解,且生成沉淀和沉淀溶解消耗的CO2相等,图象与反应不符合,故B错误;
C.醋酸是弱酸,导电能力不大,加入氨水后,离子方程式:NH3·H2O+CH3COOH═NH4++H2O+CH3COO-,生成醋酸铵是强电解质,导电能力增强,导电性变化大,至过量时,氨水溶液的体积占主导,离子浓度变小,导电能力降低,故C错误;
D.一水合氨不会溶解氢氧化铝,氯化铝与氨水反应的离子方程式为:Al3++3NH3·H2O═Al(OH)3↓+3NH4+,沉淀不溶解,故D错误;
故选:A。


科目:高中化学 来源: 题型:
【题目】有机物![]() 有多种同分异构体,其中属于酯类且氯原子直接连接在苯环上的同分异构体有多少种(不考虑立体异构)
有多种同分异构体,其中属于酯类且氯原子直接连接在苯环上的同分异构体有多少种(不考虑立体异构)
A.19种 B.9种 C.15种 D.6种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是某同学对相应反应的离子方程式所作的评价,其中评价合理的是()
编号 | 化学反应 | 离子方程式 | 评价 |
| 碳酸钙与醋酸反应 |
| 错误,碳酸钙是弱电解质,不应写成离子形式 |
| 向 |
| 错误,碱过量,应生成 |
|
|
| 正确 |
| 等物质的量的 |
| 正确 |
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)3.4gNH3中含有________molH。
(2)标准状况下,等体积的CO和CO2的质量比为________。
(3)100mLAl2(SO4)3溶液中c(Al3+)=0.20molLˉ1,则c(SO42-)=_______。
(4)物质的量浓度相同的NaCl、MgCl2、AlCl3溶液中分别加入足量的AgNO3溶液中,生成沉淀的质量相等,三种溶液的体积比为____________。
(5)标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,则该溶液的溶质的物质的量浓度为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CPAE是蜂胶的主要活性成分,它可由咖啡酸合成,其合成过程如下。下列说法不正确的是

A. CPAE存在顺反异构体
B. 可用金属Na检测上述反应结束后是否残留苯乙醇
C. 与苯乙醇互为同分异构体的酚类物质共有9种
D. 咖啡酸可发生聚合反应,并且其分子中含有3种官能团
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质所含原子数由多到少的顺序是( )
①24 g碳 ②0.7 mol NH3 ③4.6 g钠 ④0.2 mol H2SO4 ⑤4 g He
A. ①③②④⑤B. ②①④⑤③
C. ②④①⑤③D. ④⑤②①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列叙述不正确的是( )
A. 含有NA个氧原子的氧气在标准状况下的体积约为22.4 L
B. 2 L 0.3 mol·L-1的硫酸钾溶液中钾离子浓度为0.6 mol·L-1
C. 常温常压下,32 g O2和O3的混合气体所含原子数为2NA
D. 25 ℃,1.01×105 Pa,64 g SO2中含有的原子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列仪器:

(1)海水蒸馏是由海水获得淡水的常用方法之一,在实验室里组成一套蒸馏装置肯定 需要上述仪器中的一部分,按照实验仪器从下到上、从左到右的顺序,依次是__________ (填序号);仪器⑤的冷凝水应从________(填“a”或“b”)口进入。
(2)海带等藻类物质经过处理后,可以得到碘水,欲从碘水中提取碘,需要上述仪器 中的______(填序号),该仪器名称为__________,向该碘水中加入四氯化碳以提取碘 单质的实验操作叫做_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水FeCl3呈棕红色,极易潮解,100 ℃左右时升华,工业上常用作有机合成催化剂。实验室可用下列装置(夹持仪器略去)制备并收集无水FeCl3。
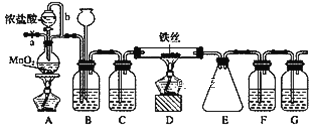
(1)装置A中反应的离子方程式为________________。
(2)装置C中所加的试剂为____________。
(3)导管b的作用为___________;装置G的作用为________。
(4)实验时应先点燃A处的酒精灯,反应一会儿后,再点燃D处的酒精灯,是因为_____。
(5)为检验所得产品为FeCl3,可进行如下实验:取E中收集的产物少许,加水溶解,向所得溶液中加入____________,___________(填试剂和现象)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com